
Welche chemischen Grundlagen können im Haushalt gefunden werden?
Das chemische Basen Sie sind in einer Vielzahl von Produkten für den täglichen Gebrauch zu Hause und in bestimmten Lebensmitteln enthalten, die Sie sich vielleicht gar nicht vorstellen können. Wissenschaft ist schließlich überall.
Als ich mein Chemiestudium an der Universität begann, forderte uns einer meiner Professoren auf, neugierig und recherchierend zu sein, Eigenschaften, die einen guten Wissenschaftler auszeichnen..

Inspiriert von seinen Worten nahm ich eine Rolle Lackmuspapier und begann, den pH-Wert von allem, was ich in meinem Haus hatte, zu messen. Die Wahrheit war, dass ich sehr überrascht war von der Menge an Dingen, die zu Hause einen basischen pH-Wert hatten.
Tatsächlich erinnere ich mich, dass das einzige, was das Lackmuspapier in Rot verwandelte, die Ketchup-Tomatensauce war (was Sinn macht, da die Zutaten Tomaten und Essig sind)..
Wie ich in anderen Artikeln erwähnt habe, ist eine Base eine chemische Verbindung mit der Fähigkeit, Protonen aufzunehmen, Hydroxyl zu spenden oder ein Paar freier Elektronen zu besitzen. Sie haben die Eigenschaft, Säuren zu neutralisieren, den pH-Wert einer Lösung zu erhöhen und Lackmuspapier blau zu färben..
Fundamente sind im täglichen Gebrauch sehr wichtig und bleiben oft unbemerkt. Ohne Basen würden sich keine anhaltenden Flecken auf der Kleidung lösen, Sie hätten schmutzige Spiegel und sogar Darmprobleme wie Magenrückfluss und Verstopfung könnten nicht gelindert werden (SPM Chemistry Form 4 Notes - Säuren und Basen (Teil 2), 2013)..
Im Folgenden gebe ich eine Liste der Grundlagen des täglichen Gebrauchs, die zu dieser Zeit Lackmuspapier eine blaue Farbe verliehen haben. Alle diese Basen sind in den Produkten des täglichen Gebrauchs und der Nahrung enthalten (Acids vs. Bases, S.F.).
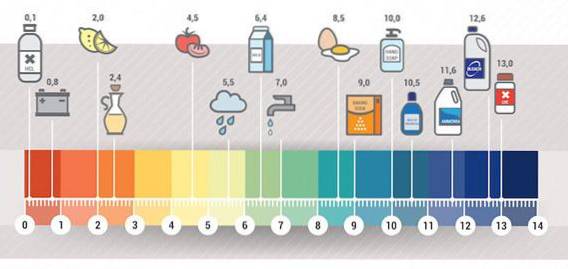
Beispiele für Basen, die wir zu Hause finden
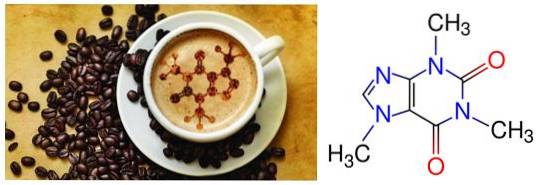
1- Kaffee und Tee: Das Koffeinmolekül (1,3,7-Trimethylxanthin) ist nach ihm benannt, weil es in Kaffeebohnen entdeckt wurde.
Später wurde entdeckt, dass es auch in Teeblättern in höherer Konzentration vorkommt. Dieses Molekül, ein Purin, das Adenin sehr ähnlich ist und wie es eine stickstoffhaltige Base ist.
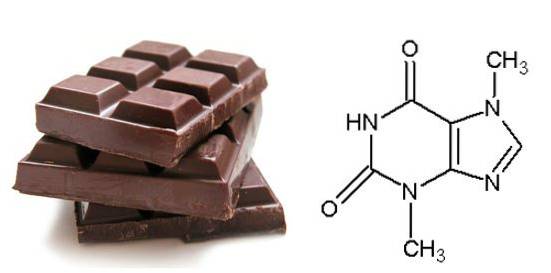
2- SchokoladeÄhnlich wie Kaffee enthält Schokolade eine Verbindung namens Theobromin, die eine Purin-Stickstoff-Base ist.
Diese Verbindung ist dafür verantwortlich, dass Schokolade so gut schmeckt. Katzen und Hunde metabolisieren jedoch kein Theobromin, wodurch das Herz und das Zentralnervensystem geschädigt werden. Geben Sie Ihrem Haustier niemals Schokolade (Reactions, 2016).
3- Chlor: Chlor ist tatsächlich Hypochlorit oder Natriumchlorit, je nachdem, ob es sich um Chlor aus Schwimmbädern oder um Chlor zum Waschen von Kleidung handelt.
Hypochlorit- und Chloritionen sind die konjugierten Basen von Hypochlor- bzw. Chlorsäuren, die in wässriger Lösung Protonen aus Wasser entnehmen können, wodurch die Hydroxylkonzentration im Medium erhöht wird (Säuren und Basen - Anwendungen im wirklichen Leben, S.F.).
ClO- + H.zweiO → HClO + OH-
ClOzwei- + H.zweiO → HClOzwei + Oh-
4- Bleichmittel: Die stärkste im Handel erhältliche Basis, reinigt Öfen und verstopft Rohre. Bleichmittel oder Natriumhydroxid (NaOH) ist eine Hauptkomponente in Abflussreinigern, die den Müll verflüssigen, damit er durch die Rohre gewaschen werden kann.
Ofenreiniger auf Basis von ätzendem Bleichmittel schneiden das im Ofen gekochte Material durch. Muss mit Vorsicht behandelt werden, da dies zu schweren Verätzungen führen kann.

Backpulver ist sicher zu berühren. Wenn Sie ein paar Prisen Backpulver in Wasser trinken, wird ein Teil der überschüssigen Säure in Ihrem Magen neutralisiert. Es macht auch ein leicht abrasives und ungiftiges Reinigungsmittel.
6- Borax: auch bekannt als Natriumtetraborat (NazweiB4O7 ● 10HzweiO) hat einmal geholfen, Mumien im alten Ägypten zu erhalten. Jetzt hält es die Kleidung frisch und tötet Schädlinge im Haushalt ab. Mit einem pH-Wert von 9,2 ist es 920-mal alkalischer als reines Wasser.
Borax trägt ein Sauerstoffion zum Wasser bei, um Wasserstoffperoxid (H) zu bildenzweiODERzwei) in Lösung, was es zu einem Desinfektionsmittel und einem milden Bleichmittel macht.
Vermeiden Sie den direkten oder zu langen Umgang mit Borax, da dies zu Hautreizungen führen kann. Borax ist bei Verschlucken leicht giftig. (Whitney, 2017).
7- Ammoniak: Der Begriff "Ammoniak" bezieht sich sowohl auf ein reizendes Gas (NH)3) sowie das Reinigungsmittel (NH4OH), das aus der Auflösung von Ammoniak in Wasser resultiert. Haushaltsammoniak hat einen pH-Wert von 11 oder 50-mal stärker als Magnesia-Milch.
Es ist ein leistungsstarker Haushaltsreiniger, der praktisch jede Oberfläche von Schmutz und Fett befreit (Cascio, 2017)..

9- Magnesia-Milch: Dieses übliche Antazida und Abführmittel erhielt seinen milchigen Namen für seine Opazität. Magnesiumhydroxid [Mg (OH)zwei] hat einen pH von 10,5. Kommerzielle Milch von Magnesia-Zubereitungen verwendet Minz- oder Fruchtaromen, um den bitteren Geschmack zu verbergen, der für alkalische Substanzen charakteristisch ist..
10- Antazida: Die Verwendung von schwachen Basen zur Linderung von Sodbrennen ist häufig. Verbindungen wie Natriumbicarbonat (NaHCO3), Magnesiumcarbonat (MgCO3), Calciumcarbonat (CaCO3) und Aluminiumhydroxid (Al (OH)3) sind die Wirkstoffe von Antazida.
11- Deodorants- Aluminiumhydroxid ist auch der Wirkstoff in Deodorants. Es wirkt als Bakterizid und eliminiert die Bakterien, die sich von den Proteinen und Fetten im Schweiß ernähren, die von den apokrinen Drüsen ausgeschieden werden (Reaktion, 2015)..
12- Seife: Seife ist das Produkt der Neutralisation von Natriumhydroxid und Stearinsäure. Letzteres ist eine gesättigte Fettsäure mit 18 Kohlenstoffatomen.

Das Produkt dieser Neutralisation ist Natriumstearat, das in wässriger Lösung das Stearation bildet.
Dieses Molekül enthält einen polaren und einen unpolaren Teil, weshalb es als amphipathisches Molekül bekannt ist und für die Entfernung von Fetten und anderen aliphatischen Verbindungen aus der Kleidung oder dem Körper verantwortlich ist.
Verweise
- Säuren und Basen - reale Anwendungen. (S.F.). Von scienceclarified.com wiederhergestellt.
- Säuren vs. Basen. (S.F.). Wiederhergestellt von acid-vs-bases.weebly.com.
- Cascio, C. (2017, 25. April). Beispiele für Säure und Base in der Praxis. Von sciencing.com wiederhergestellt.
- (2015, 21. September). Wie wirken Deodorants und Antitranspirantien?? . Von youtube.com wiederhergestellt.
- Reaktionen. (2016, 18. Januar). Warum ist Schokolade schlecht für Hunde?? . Von youtube.com wiederhergestellt.
- SPM Chemistry Form 4 Notes - Säuren und Basen (Teil 2). (2013, 2. März). Von berryberryeasy.com wiederhergestellt.
- Whitney, L. (2017, 25. April). Basen, die als übliche Haushaltsprodukte verwendet werden. Von sciencing.com wiederhergestellt.



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.