
Plastochinonklassifikation, chemische Struktur und Funktionen
Das Plastochinon ((PQ) ist ein organisches Lipidmolekül, insbesondere ein Isoprenoid der Chinonfamilie. Tatsächlich ist es ein mehrfach ungesättigtes Seitenkettenderivat von Chinon, das am Photosystem II der Photosynthese beteiligt ist..
Es befindet sich in der Thylakoidmembran von Chloroplasten, hat einen unpolaren Charakter und ist auf molekularer Ebene sehr aktiv. In der Tat leitet sich der Name Plastochinon von seiner Lage in den Chloroplasten höherer Pflanzen ab.
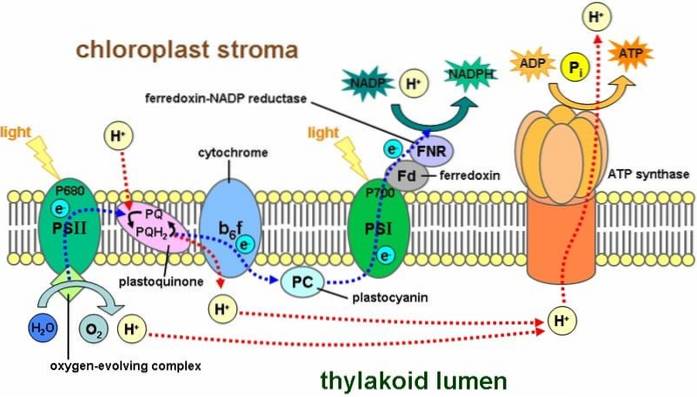
Während der Photosynthese wird Sonnenstrahlung im FS-II-System von Chlorophyll P-680 eingefangen und dann durch Freisetzung eines Elektrons oxidiert. Dieses Elektron steigt auf ein höheres Energieniveau an, das vom Wählerakzeptormolekül aufgenommen wird: Plastochinon (PQ)..
Plastochinone sind Teil der photosynthetischen Elektronentransportkette. Sie sind der Ort der Integration verschiedener Signale und ein Schlüsselelement in der Reaktion von RSp31 auf Licht. Es gibt ungefähr 10 PQs pro FS-II, die entsprechend dem Funktionszustand des Photosyntheseapparats reduziert und oxidiert werden..
Daher werden die Elektronen durch eine Transportkette übertragen, an der mehrere Cytochrome beteiligt sind, um später Plastocyanin (PC) zu erreichen, das die Elektronen an Chlorophyllmoleküle von FS-I abgibt.
Artikelverzeichnis
- 1 Klassifizierung
- 2 Chemische Struktur
- 2.1-Biosynthese
- 3 Funktionen
- 3.1 Lichtphase (PS-II)
- 4 Referenzen
Einstufung
Plastochinon (C.55H.80ODERzwei) ist ein Molekül, das mit einem Benzolring (Chinon) assoziiert ist. Insbesondere ist es ein Isomer von Cyclohexadion, das sich durch eine aromatische Verbindung auszeichnet, die sich durch ihr Redoxpotential auszeichnet.
Chinone werden nach ihrer Struktur und ihren Eigenschaften gruppiert. Innerhalb dieser Gruppe werden Benzochinone differenziert, die durch die Oxygenierung von Hydrochinonen erzeugt werden. Die Isomere dieses Moleküls sind die ortho-Benzochinon und damit-Benzochinon.
Andererseits ähnelt Plastochinon Ubichinon, weil es zur Benzochinonfamilie gehört. In diesem Fall dienen beide als Elektronenakzeptoren in Transportketten während der Photosynthese und der anaeroben Atmung..
In Verbindung mit seinem Lipidstatus wird es in die Terpenfamilie eingeteilt. Das heißt, jene Lipide, die pflanzliche und tierische Pigmente bilden und den Zellen Farbe verleihen.
Chemische Struktur
Plastochinon besteht aus einem aktiven Benzol-Chinon-Ring, der mit einer Seitenkette eines Polyisoprenoids assoziiert ist. Tatsächlich ist der hexagonale aromatische Ring über Doppelbindungen an den C-1- und C-4-Kohlenstoffen mit zwei Sauerstoffmolekülen verbunden..
Dieses Element hat die Seitenkette und besteht aus neun miteinander verbundenen Isoprenen. Folglich ist es ein Polyterpen oder Isoprenoid, dh Kohlenwasserstoffpolymere mit fünf Kohlenstoffatomen Isopren (2-Methyl-1,3-butadien).
Ebenso ist es ein prenyliertes Molekül, das die Anlagerung an Zellmembranen erleichtert, ähnlich wie Lipidanker. In dieser Hinsicht wurde eine hydrophobe Gruppe zu seiner Alkylkette hinzugefügt (Methylgruppe CH3, verzweigt in Position R3 und R4).
-Biosynthese
Während des Photosyntheseprozesses wird Plastochinon aufgrund seines kurzen Lebenszyklus kontinuierlich synthetisiert. Studien an Pflanzenzellen haben ergeben, dass dieses Molekül zwischen 15 und 30 Stunden aktiv bleibt.
In der Tat ist die Plastochinon-Biosynthese ein sehr komplexer Prozess, an dem bis zu 35 Enzyme beteiligt sind. Die Biosynthese besteht aus zwei Phasen: Die erste erfolgt im Benzolring und die zweite in den Seitenketten.
Anfangsphase
In der Anfangsphase wird die Synthese des Chinon-Benzol-Rings und der Prenylkette durchgeführt. Der aus Tyrosinen und Prenylseitenketten erhaltene Ring ist das Ergebnis von Glycerinaldehyd-3-phosphat und Pyruvat..
Basierend auf der Größe der Polyisoprenoidkette wird die Art des Plastochinons festgelegt.
Ringkondensationsreaktion mit Seitenketten
Die nächste Phase umfasst die Kondensationsreaktion des Rings mit den Seitenketten.
Homogentistische Säure (HGA) ist der Vorgänger des Benzol-Chinon-Rings, der aus Tyrosin synthetisiert wird. Dieser Prozess findet dank der Katalyse des Enzyms Tyrosin-Amino-Transferase statt.
Die Prenylseitenketten stammen ihrerseits aus dem Methylerythritphosphat (MEP) -Pfad. Diese Ketten werden durch das Enzym Solanesyldiphosphat-Synthetase unter Bildung von Solanesyldiphosphat (SPP) katalysiert..
Methylerythritphosphat (MEP) bildet einen Stoffwechselweg für die Biosynthese von Isoprenoiden. Nach der Bildung beider Verbindungen tritt die Kondensation von homogenistischer Säure mit der Solanesyldiphosphatkette auf, eine Reaktion, die durch das Enzym Homogentistat-Solanesyltransferase (HST) katalysiert wird..
2-Dimethylplastochinon
Schließlich entsteht eine Verbindung namens 2-Dimethylplastochinon, die später unter Intervention des Enzyms Methyltransferase als Endprodukt Plastochinon erhalten kann.
Eigenschaften
Plastochinone greifen in die Photosynthese ein, ein Prozess, bei dem Energie aus dem Sonnenlicht eingreift und bei der Umwandlung eines anorganischen Substrats energiereiche organische Stoffe entstehen.
Lichtphase (PS-II)
Die Funktion von Plastochinon hängt mit der Lichtphase (PS-II) des Photosyntheseprozesses zusammen. Die am Elektronentransfer beteiligten Plastochinonmoleküle heißen Q A und Q B..
In dieser Hinsicht ist das Photosystem II (PS-II) ein Komplex namens Wasser-Plastochinonoxid-Reduktase, bei dem zwei grundlegende Prozesse ausgeführt werden. Die Wasseroxidation wird enzymatisch katalysiert und es tritt eine Plastochinonreduktion auf. Bei dieser Aktivität werden Photonen mit einer Wellenlänge von 680 nm absorbiert..
Die Moleküle Q A und Q B unterscheiden sich in der Art und Weise, wie sie Elektronen übertragen, und in der Geschwindigkeit der Übertragung. Auch aufgrund der Art der Bindung (Bindungsstelle) mit Photosystem II. Q A soll das feste Plastochinon sein und Q B ist das mobile Plastochinon.
Immerhin ist Q A die Bindungszone des Photosystems II, die die beiden Elektronen in einer Zeitvariation zwischen 200 und 600 us akzeptiert. Stattdessen hat Q B die Fähigkeit, sich vom Photosystem II zu binden und zu lösen, indem es Elektronen aufnimmt und auf das Cytochrom überträgt..
Auf molekularer Ebene wird Q B, wenn es reduziert wird, gegen ein anderes der freien Plastochinone innerhalb der Thylakoidmembran ausgetauscht. Zwischen Q A und Q B befindet sich ein nichtionisches Fe-Atom (Fe+zwei), die am elektronischen Transport zwischen ihnen teilnehmen.
Kurz gesagt, Q B interagiert mit Aminosäureresten im Reaktionszentrum. Auf diese Weise erhalten Q A und Q B einen großen Unterschied in den Redoxpotentialen..
Da Q B lockerer an die Membran gebunden ist, kann es außerdem leicht durch Reduktion auf QH 2 getrennt werden. In diesem Zustand ist es in der Lage, von Q A empfangene hochenergetische Elektronen auf den Cytochrom-bc1-Komplex 8 zu übertragen.
Verweise
- González, Carlos (2015) Photosynthese. Wiederhergestellt unter: botanica.cnba.uba.ar
- Pérez-Urria Carril, Elena (2009) Photosynthese: Grundlegende Aspekte. Reduca (Biologie). Pflanzenphysiologie-Reihe. 2 (3): 1-47. ISSN: 1989-3620
- Petrillo, Ezequiel (2011) Regulierung des alternativen Spleißens in Pflanzen. Lichteffekte durch retrograde Signale und PRMT5-Proteinmethyltransferase.
- Sotelo Ailin (2014) Photosynthese. Fakultät für Exakte, Naturwissenschaften und Vermessung. Lehrstuhl für Pflanzenphysiologie (Studienführer).



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.