
GLUT 2 Eigenschaften, Struktur, Funktionen

GLUT2 Es ist ein Glukosetransporter mit niedriger Affinität, der in den Membranen von Pankreas-, Leber-, Nieren- und Darmzellen sowie in Astrozyten und Tanizyten exprimiert wird. Zusätzlich zur Vermittlung des Glukosetransports ist es auch am Transport von Fruktose, Galaktose und Glukosamin beteiligt. es ist also mehr als ein Glukosetransporter ein Hexosetransporter.
Seine geringe Affinität zu Glukose ermöglicht es ihm, als Sensorprotein für den Blutzuckerspiegel zu fungieren. Daher ist es an der regulatorischen Kontrolle vieler physiologischer Ereignisse beteiligt, die auf Schwankungen der Glukosekonzentration im Blut reagieren..
Unter den vielen Prozessen, die es reguliert, fallen folgende auf: 1) die Freisetzung von Insulin durch Pankreaszellen, die durch hohe Glukosekonzentrationen stimuliert werden; 2) Glukagonsekretion durch Hepatozyten zur Glukoseproduktion bei Hypoglykämie.
Artikelverzeichnis
- 1 Erleichterter Transport von Glukose in die Zelle
- 2 Funktionen von GLUT2
- 3 Struktur von GLUT2
- 4 GLUT2-Funktionen
- 4.1 Rolle von GLUT2 bei der Aufrechterhaltung der Zellhomöostase
- 5 Referenzen
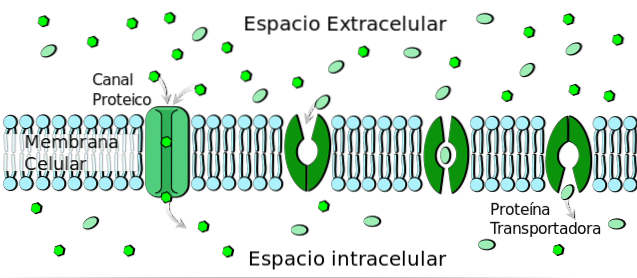
Erleichterter Glukosetransport in die Zelle
Ungefähr 75% der Glukose, die in die Zelle gelangt, um Stoffwechselwege für die Energieerzeugung anzutreiben, geschieht über einen passiven Transportmechanismus, der durch integrale Membranproteine, sogenannte Transporter, erleichtert wird..
Dieser Transportmechanismus ist allgemein als erleichterte Diffusion bekannt. Es ist kein Energiebeitrag erforderlich, und es wird zugunsten eines Konzentrationsgradienten angegeben. Das heißt, von einem Bereich hoher Konzentration zu einem Bereich niedriger Konzentration.
Bisher wurden mindestens 14 Isoformen von Glucose-erleichterten Diffusionstransportern, einschließlich GLUT2, identifiziert. Alle von ihnen gehören zur Hauptüberfamilie der Facilitators (MSF) und werden im Konsens GLUTs genannt (für das englische Akronym „Glucose Transporters“)..
Die verschiedenen GLUTs, die bisher charakterisiert wurden, werden von SLC2A-Genen codiert und zeigen deutliche Unterschiede in der Aminosäuresequenz, der Präferenz für den Transport von Substraten sowie der Zell- und Gewebeverteilung..
GLUT2-Funktionen
GLUT2 mobilisiert Glukose über einen Transportmechanismus in eine Richtung (Uniport). Diese Funktion wird auch von GLUT1 ausgeführt, dem in praktisch allen Säugetierzellen am häufigsten vorkommenden Glukosetransporter..
Im Gegensatz dazu weist es jedoch eine extrem geringe Affinität zu Glucose auf, was bedeutet, dass es nur dann transportiert werden kann, wenn die Konzentrationen dieses Zuckers dazu neigen, in der extrazellulären Umgebung sehr hohe Werte zu erreichen..
Trotz seiner geringen Affinität zu Glucose weist es eine hohe Transportkapazität auf, was bedeutet, dass es große Mengen dieser Hexose mit hoher Geschwindigkeit transportieren kann. Diese beiden Eigenschaften scheinen mit der Rolle dieses Transporters bei der Reaktion auf subtile Änderungen der Glukosekonzentration in Zusammenhang zu stehen..
Molekulare Charakterisierungsstudien dieses Transporters haben gezeigt, dass er keine eindeutige Spezifität für Glucose aufweist. Im Gegenteil, es ist in der Lage, den passiven Transport von Fructose, Galactose, Mannose und Glucosamin zu vermitteln. Niedrige Affinität für die ersten drei und hohe Affinität für Glucosamin.
Da alle diese Moleküle Zucker mit sechs Kohlenstoffatomen sind, kann sie eher als Hexosetransporter als als Glucosetransporter betrachtet werden..
GLUT2-Struktur
GLUT2 hat eine Peptidsequenz, die zu 55% mit der des Transporters mit hoher Affinität für Glucose-GLUT1 identisch ist.
Trotz dieses geringen Prozentsatzes an Ähnlichkeit zwischen den Sequenzen beider Transporter haben durch Röntgenkristallographie durchgeführte Studien gezeigt, dass sie eine ähnliche Struktur aufweisen..
Diese Struktur entspricht der eines α-Helix-Multipass-Transmembranproteins. Das heißt, es durchquert die Membran mehrmals durch Transmembransegmente, die eine α-Helix-Konfiguration aufweisen..
Wie bei allen Mitgliedern der Haupt-Superfamilie der Moderatoren (MSF), zu der es gehört, kreuzen 12 Helixsegmente die Membran. Sechs davon ordnen sich räumlich neu an und bilden eine hydrophile Pore, durch die Zucker mobilisiert werden..
Es sollte beachtet werden, dass die Hexosebindungsstelle durch die Orientierung und Pseudopsymmetrie definiert ist, die durch die Carboxyl- und Amino-terminalen Enden des Proteins präsentiert werden. Beide, die derselben Seite der Membran ausgesetzt sind, erzeugen einen Hohlraum, in dem die Anordnung der sechs Zuckeratome erkannt wird, was ihre Vereinigung erleichtert..
Eine Änderung der Struktur des Transporters hängt mit dem Mechanismus zusammen, mit dem Zucker von einer Seite der Membran zur anderen transportiert wird. Diese strukturelle Verformung ermöglicht es, die Bindungsstelle zur zytoplasmatischen Seite hin zu mobilisieren, wo die Freisetzung des transportierten Moleküls schnell erfolgt..
GLUT2-Funktionen
Zusätzlich zur Vermittlung der Sequestrierung von Glucose, Mannose, Galactose und Glucosamin innerhalb der Zelle wurden der Expression dieses Transporters in verschiedenen Zelltypen zahlreiche physiologische Funktionen zugeschrieben..
Viele dieser Funktionen wurden unter Verwendung von Gensuppressionstechniken bestimmt. Letztere bestehen darin, die Expression des Gens zu verhindern, dessen Funktion in den Zellen eines bestimmten Gewebes oder eines vollständigen Organismus untersucht werden soll..
In diesem Sinne hat die Blockierung der Expression von GLUT2 in Mäusen gezeigt, dass dieses Protein das Hauptmittel des Glukosetransports sowohl in Nieren- als auch in Leberzellen darstellt. Darüber hinaus hängt der Transport von Galactose und Fructose nicht mit der Erzeugung von Glucose aus diesen Zuckern über die Gluconeogenese zusammen..
Zusätzlich wurde gezeigt, dass es eine regulatorische Rolle bei verschiedenen physiologischen Funktionen ausübt, da es aufgrund seiner geringen Affinität für Glucose erkennen kann, wann die Konzentrationen dieses Zuckers hoch sind..
Rolle von GLUT2 bei der Aufrechterhaltung der Zellhomöostase
Da es eine entscheidende Funktion bei der Energieerzeugung durch alle Zellen, insbesondere Nervenzellen, erfüllt, muss seine Konzentration im Blut nahe einem Wert von 5 mmol / l gehalten werden. Variationen in dieser Konzentration werden immer von regulatorischen Proteinen durch "Glukose-Nachweis" -Mechanismen überwacht..
Diese Mechanismen bestehen aus molekularen Strategien, die eine schnelle Reaktion auf plötzliche Schwankungen der Glukosekonzentration ermöglichen. In diesem Sinne verleiht ihm die Expression von GLUT2 in der Membran von Zellen, deren Funktionen durch Hyperglykämie aktiviert werden, eine regulatorische Rolle..
Tatsächlich wurde gezeigt, dass die Insulinsekretion durch Pankreaszellen durch den Nachweis von Glucose durch GLUT2 ausgelöst wird..
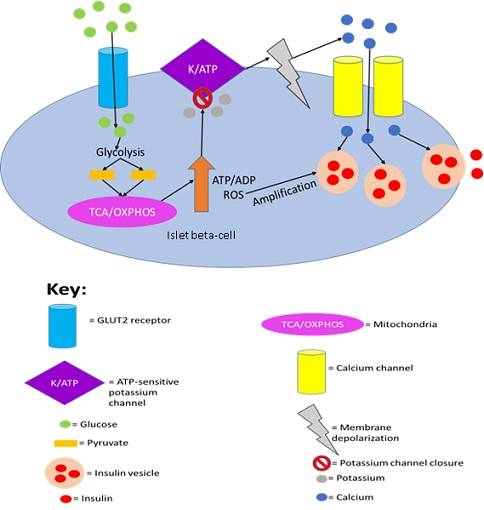
Die Insulinsekretion durch Pankreaszellen wird durch den Nachweis von Glucose durch GLUT2 ausgelöst. Von Joshua J. Reed [CC BY-SA 4.0 (https://creativecommons.org/licenses/by-sa/4.0)] aus Wikimedia Commons.
Zusätzlich vermittelt es die autonome Nervenkontrolle der Fütterung, Thermoregulation und der Funktion von Pankreaszellen, die durch den Nachweis von Glukose stimuliert werden..
Wenn die GLUT2-Spiegel in Nervenzellen abnehmen, erzeugen sie ein positives Signal, um die Glucagonsekretion auszulösen. Denken Sie daran, dass Glukagon ein Hormon ist, das die Glukoseproduktion der Leber aus Glykogenspeichern fördert.
Verweise
- Burcelin R, Thorens B. Hinweise darauf, dass extrapankreatische GLUT-abhängige Glukosesensoren die Glukagonsekretion steuern. Diabetes. 2001; 50 (6): 1282 & ndash; 1289.
- Kellett GL, Brot-Laroche E, Mace OJ, Leturque A. Zuckeraufnahme im Darm: die Rolle von GLUT2. Annu Rev Nutr. 2008; 28: 35-54.
- Lamy CM, Sanno H., Labouèbe G., Picard A., Magnan C., Chatton JY, Thorens B. Hypoglykämie-aktivierte GLUT2-Neuronen der Nucleus Tractus Solitaries stimulieren die vagale Aktivität und die Glucagonsekretion. Cell Metab. 2014; 19 (3): 527 & ndash; 538.
- Mückler M, Thorens B. Die SLC2 (GLUT) -Familie von Membrantransportern. Mol Aspects Med. 2013; 34 (2-3): 121-38.
- Tarussio D., Metref S., Seyer P., Mounien L., Vallois D., Magnan C., Foretz M., Thorens B. Die nervöse Glukoseerfassung reguliert die postnatale Proliferation von β-Zellen und die Glukosehomöostase. J Clin Invest. 2014; 124 (1): 413 & ndash; 424.
- B. GLUT2 beim Pankreas- und Extra-Pankreas-Gluko-Nachweis (Übersicht). Mol Membr Biol. 2001; 18 (4): 265 & ndash; 273.
- Thorens B, Mückler M. Glukosetransporter im 21. Jahrhundert. Am J Physiol Endocrinol Metab. 2010; 298 (2): E141-E145.
- Thorens B. GLUT2, Glukoseerfassung und Glukosehomöostase. Diabetologie. 2015; 58 (2): 221 & ndash; 232.


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.