
Anomere Kohlenstoffmerkmale und Beispiele
Das anomerer Kohlenstoff Es ist ein Stereozentrum, das in den cyclischen Strukturen von Kohlenhydraten (Mono- oder Polysacchariden) vorhanden ist. Da es sich um ein Stereozentrum handelt, genauer gesagt um ein Epimer, werden daraus zwei Diastereoisomere abgeleitet, die mit den Buchstaben α und β bezeichnet sind. Dies sind die Anomere und Teil der umfangreichen Nomenklatur in der Welt der Zucker.
Jedes Anomer, α oder β, unterscheidet sich in der Position der OH-Gruppe des anomeren Kohlenstoffs relativ zum Ring; In beiden Fällen ist der anomere Kohlenstoff jedoch derselbe und befindet sich an derselben Stelle im Molekül. Anomere sind cyclische Halbacetale, das Produkt einer intramolekularen Reaktion in der offenen Kette von Zuckern; ob Aldosen (Aldehyde) oder Ketosen (Ketone).
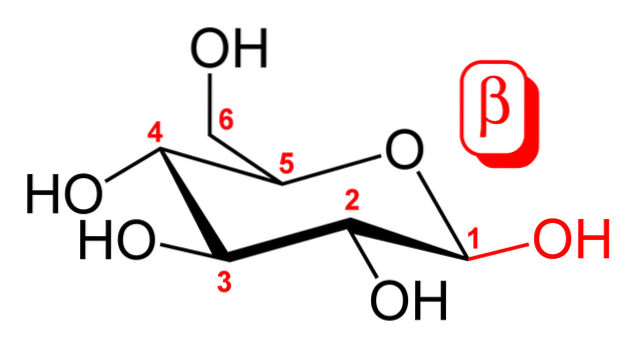
Das obere Bild zeigt die Stuhlkonformation für β-D-Glucopyranose. Wie zu sehen ist, besteht es aus einem sechsgliedrigen Ring, der ein Sauerstoffatom zwischen den Kohlenstoffen 5 und 1 enthält; Letzteres bzw. das erste ist der anomere Kohlenstoff, der mit zwei Sauerstoffatomen zwei einfache Bindungen eingeht.
Wenn Sie genau hinschauen, ist die an Kohlenstoff 1 gebundene OH-Gruppe ebenso wie die CH-Gruppe über dem hexagonalen Ring ausgerichtetzweiOH (Kohlenstoff 6). Dies ist das β-Anomer. Das α-Anomer würde sich dagegen nur in dieser OH-Gruppe unterscheiden, die sich im Ring befinden würde, als wäre es ein trans-Diastereoisomer..
Artikelverzeichnis
- 1 Halbacetale
- 1.1 Zyklisches Halbacetal
- 2 Eigenschaften von anomerem Kohlenstoff und wie man ihn erkennt
- 3 Beispiele
- 3.1 Beispiel 1
- 3.2 Beispiel 2
- 3.3 Beispiel 3
- 4 Referenzen
Hemiacetals
Es ist notwendig, etwas tiefer in das Konzept der Halbacetale einzusteigen, um anomeren Kohlenstoff besser zu verstehen und zu unterscheiden. Halbacetale sind das Produkt einer chemischen Reaktion zwischen einem Alkohol und einem Aldehyd (Aldosen) oder einem Keton (Ketosen)..
Diese Reaktion kann durch die folgende allgemeine chemische Gleichung dargestellt werden:
ROH + R'CHO => ROCH (OH) R '
Wie zu sehen ist, reagiert ein Alkohol mit einem Aldehyd unter Bildung des Halbacetals. Was würde passieren, wenn sowohl R als auch R 'zur selben Kette gehören? In diesem Fall hätten Sie ein cyclisches Halbacetal, und die einzige Möglichkeit, wie es gebildet werden kann, besteht darin, dass beide funktionellen Gruppen, -OH und -CHO, in der Molekülstruktur vorhanden sind..
Zusätzlich muss die Struktur aus einer flexiblen Kette bestehen und Bindungen aufweisen, die den nukleophilen Angriff des OH auf den Carbonylkohlenstoff der CHO-Gruppe erleichtern können. In diesem Fall schließt sich die Struktur zu einem fünf- oder sechsgliedrigen Ring..
Zyklisches Halbacetal
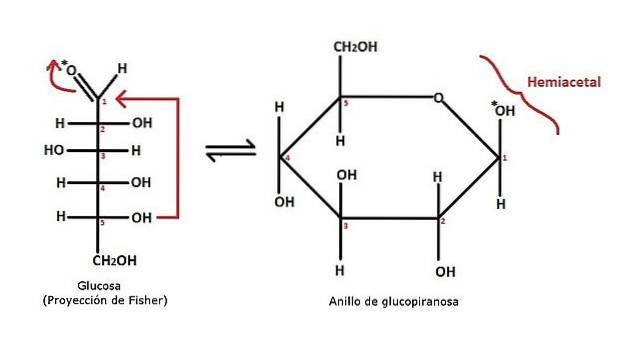
Ein Beispiel für die Bildung eines cyclischen Halbacetals für Glucosemonosaccharid ist im obigen Bild gezeigt. Es ist ersichtlich, dass es aus einer Aldose mit einer Aldehydgruppe CHO (Kohlenstoff 1) besteht. Dies wird von der OH-Gruppe von Kohlenstoff 5 angegriffen, wie durch den roten Pfeil angezeigt.
Die Struktur geht von einer offenen Kette (Glucose) zu einem pyranen Ring (Glucopyranose) über. Zunächst besteht möglicherweise keine Beziehung zwischen dieser Reaktion und der gerade für Hemiacetal erklärten. aber wenn Sie sich den Ring genau ansehen, insbesondere in Abschnitt C.5-O-C1(OH) -Czwei, Es versteht sich, dass dies dem erwarteten Skelett für ein Halbacetal entspricht.
Die Kohlenstoffe 5 und 2 repräsentieren R bzw. R 'der allgemeinen Gleichung. Da diese Teil derselben Struktur sind, handelt es sich dann um ein cyclisches Halbacetal (und der Ring reicht aus, um offensichtlich zu sein)..
Eigenschaften von anomerem Kohlenstoff und wie man ihn erkennt
Wo ist der anomere Kohlenstoff? In Glucose ist dies die CHO-Gruppe, die entweder von unten oder von oben einen nukleophilen Angriff durch OH erfahren kann. Abhängig von der Ausrichtung des Angriffs werden zwei verschiedene Anomere gebildet: α und β, wie bereits erwähnt..
Daher ist ein erstes Merkmal, das dieser Kohlenstoff besitzt, dass er in der offenen Zuckerkette den nukleophilen Angriff erleidet; das heißt, es ist die CHO-Gruppe für die Aldosen oder die R-GruppezweiC = O für Ketosen. Sobald jedoch das cyclische Halbacetal oder der Ring gebildet ist, scheint dieser Kohlenstoff verschwunden zu sein..
Hier gibt es andere spezifischere Eigenschaften, um es in einem Pyran- oder Furanosering aller Kohlenhydrate zu lokalisieren:
-Der anomere Kohlenstoff befindet sich immer rechts oder links vom Sauerstoffatom, aus dem der Ring besteht.
-Noch wichtiger ist, dass es nicht nur an dieses Sauerstoffatom gebunden ist, sondern auch an die OH-Gruppe, die von CHO oder R stammtzweiC = O..
-Es ist asymmetrisch, dh es hat vier verschiedene Substituenten.
Mit diesen vier Eigenschaften ist es leicht, anomeren Kohlenstoff anhand einer "süßen Struktur" zu erkennen..
Beispiele
Beispiel 1
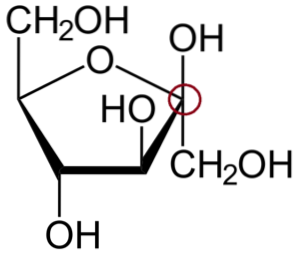
Oben ist β-D-Fructofuranose, ein cyclisches Halbacetal mit einem fünfgliedrigen Ring..
Um den anomeren Kohlenstoff zu identifizieren, müssen Sie zuerst die Kohlenstoffe auf der linken und rechten Seite des Sauerstoffatoms betrachten, aus dem der Ring besteht. Dann ist derjenige, der an die OH-Gruppe gebunden ist, der anomere Kohlenstoff; was in diesem Fall bereits rot eingekreist ist.
Dies ist das β-Anomer, da sich das OH des anomeren Kohlenstoffs ebenso wie die CH-Gruppe über dem Ring befindetzweiOh.
Beispiel 2
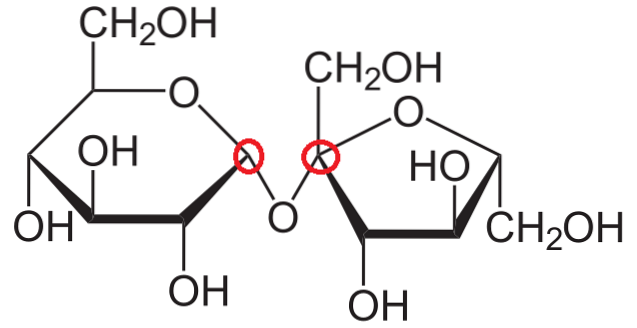
Nun versuchen wir zu erklären, was die anomeren Kohlenstoffe in der Struktur von Saccharose sind. Wie zu sehen ist, besteht es aus zwei Monosacchariden, die kovalent durch eine glykosidische Bindung -O verbunden sind-.
Der Ring auf der rechten Seite ist genau der gleiche, der gerade erwähnt wurde: β-D-Fructofuranose, nur dass er nach links „umgedreht“ ist. Der anomere Kohlenstoff bleibt für den vorherigen Fall derselbe und erfüllt alle Eigenschaften, die von ihm erwartet würden.
Andererseits ist der Ring links α-D-Glucopyranose.
Wenn man das gleiche Verfahren zur Erkennung anomerer Kohlenstoffe wiederholt und die beiden Kohlenstoffe auf der linken und rechten Seite des Sauerstoffatoms betrachtet, stellt man fest, dass der rechte Kohlenstoff derjenige ist, der an die OH-Gruppe gebunden ist; welches an der glykosidischen Bindung beteiligt ist.
Daher sind beide anomeren Kohlenstoffe durch die -O- Bindung verbunden und daher in roten Kreisen eingeschlossen..
Beispiel 3
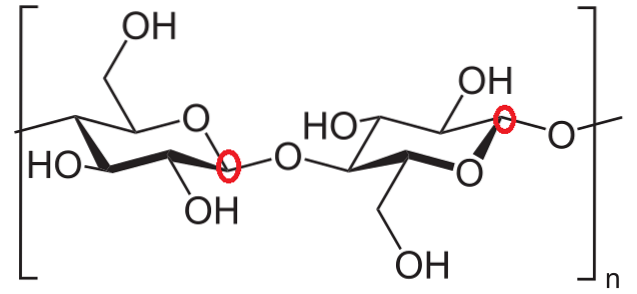
Schließlich wird vorgeschlagen, die anomeren Kohlenstoffe von zwei Glucoseeinheiten in Cellulose zu identifizieren. Wiederum werden die Kohlenstoffe um den Sauerstoff innerhalb des Rings beobachtet, und es wird festgestellt, dass im Glucosering links der anomere Kohlenstoff an der glycosidischen Bindung beteiligt ist (eingeschlossen im roten Kreis)..
Im Glucosering rechts befindet sich der anomere Kohlenstoff jedoch rechts von Sauerstoff und ist leicht zu identifizieren, da er mit dem Sauerstoff der glycosidischen Bindung verbunden ist. Somit sind beide anomeren Kohlenstoffe vollständig identifiziert.
Verweise
- Morrison, R. T. und Boyd, R., N. (1987). Organische Chemie. 5ta Auflage. Editorial Addison-Wesley Interamericana.
- Carey F. (2008). Organische Chemie. (Sechste Ausgabe). Mc Graw Hill.
- Graham Solomons T. W., Craig B. Fryhle. (2011). Organische Chemie. Amine. (10th Auflage.). Wiley plus.
- Rendina G. (1974). Angewandte Biochemietechniken. Interamericana, Mexiko.
- Chang S. (s.f.). Ein Leitfaden zum anomeren Kohlenstoff: Was ist ein anomerer Kohlenstoff? [PDF]. Wiederhergestellt von: chem.ucla.edu
- Gunawardena G. (13. März 2018). Anomere Kohle. Chemie LibreTexts. Wiederhergestellt von: chem.libretexts.org
- Foist L. (2019). Anomerer Kohlenstoff: Definition & Überblick. Studie. Wiederhergestellt von: study.com


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.