
Calciumsilicateigenschaften, Struktur, Gewinnung, Verwendung
Das Calciumsilicat ist die Bezeichnung für eine Gruppe chemischer Verbindungen, die aus Calciumoxid (CaO) und Siliciumdioxid (SiO) gebildet werdenzwei). Die allgemeine Formel dieser Verbindungen lautet xCaO • ySiOzwei• zHzweiODER.
Sie sind weiße oder gelblich weiße Feststoffe. Sie können wasserfrei sein, dh ohne Wasser (H.zweiO) in seiner Struktur oder kann es enthalten. Sie sind Teil verschiedener Arten von Mineralien in der Natur.

Calciumsilikate sind wasserunlöslich, aber wenn sie sich damit verbinden, bilden sie hydratisierte Gele (Materialien wie Gelatine), die beim Abbinden sehr hart, widerstandsfähig und nahezu wasserdicht sind.
Dies hat zu ihrer Verwendung in der Bauindustrie geführt, da sie in Zement, Ziegeln und feuchtigkeitsisolierenden Platten verwendet werden. Sie sind auch Teil von Materialien zur Heilung von Perforationen in den Zähnen, und es wurde sogar untersucht, sie bei der Regeneration von Knochen, dh als Biomaterial, zu verwenden.
Sie wurden vorgeschlagen, um die durch einige metallurgische Industrien verursachte Verschmutzung zu verringern. Sie werden auch als Reibungsgeneratoren in Fahrzeugbremsen und -kupplungen eingesetzt..
Artikelverzeichnis
- 1 Struktur
- 2 Nomenklatur
- 3 Eigenschaften
- 3.1 Physikalischer Zustand
- 3.2 Molekulargewicht
- 3.3 Schmelzpunkt
- 3.4 Dichte
- 3.5 Löslichkeit
- 3,6 pH
- 3.7 Andere Eigenschaften
- 4 Erhalten
- 5 Verwendungen
- 5.1 Bei der Beschaffung von Ziegeln
- 5.2 In Portlandzement
- 5.3 Radioaktive Abfälle immobilisieren
- 5.4 Als Dämmung für Gebäude
- 5.5 Verringerung der Umweltverschmutzung in der metallurgischen Industrie
- 5.6 In Biomaterialien
- 5.7 In Biodentin
- 5.8 Andere Anwendungen
- 6 Referenzen
Struktur
Calciumsilicat kann eine variable Menge an Calciumoxid (CaO) und Silica (SiO) enthaltenzwei). Die allgemeine Formel lautet:
xCaO • ySiOzwei• zHzweiODER
Dabei sind x, y und z Zahlen, die verschiedene Werte haben können.
Die Menge an CaO muss zwischen 3% und 35% (bezogen auf das Gewicht auf Trockenbasis) und dem SiO-Gehalt liegenzwei Es sollte 50-95 Gew .-% betragen (bezogen auf das Gewicht auf Trockenbasis). Sie können wasserfrei sein (ohne Wasser in seiner Struktur, dh z = 0 in der Formel) oder sie können hydratisiert sein (mit Wasser ist seine Konformation).
Nomenklatur
- Calciumsilicat
- Kieselsäure-Calciumsalz
- Calciumoxid und Silizium
Eigenschaften
Körperlicher Status
Sehr feiner weißer oder cremefarbener Feststoff.
Molekulargewicht
Calciummetasilicat CaO • SiOzwei oder CaSiO3 = 116,16 g / mol
Schmelzpunkt
CaSiO Calcium Metasilicate3 = 1540 ° C.
Dichte
CaSiO Calcium Metasilicate3 = 2,92 g / cm³
Löslichkeit
Unlöslich in Wasser und Ethanol.
pH
Ein mit 5% Calciumsilicat hergestellter Schlamm kann einen pH-Wert von 8,4-12,5 haben.
Andere Eigenschaften
Calciumsilicat kann mit verschiedenen Anteilen an Calcium in Form von Calciumoxid CaO und Siliciumdioxid in Form von Siliciumdioxid SiO hydratisiert (mit Wasser im Molekül) oder wasserfrei (ohne Wasser im Molekül) seinzwei.
Es hat eine hohe Wasseraufnahmefähigkeit. Calciummetasilikat (CaO • SiOzwei oder CaSiO3) zeichnet sich durch Brillanz und Weißgrad, geringe Luftfeuchtigkeit, geringen Flüchtigkeitsgehalt und gute Ölaufnahme aus.

Unter den Hydraten von Calciumsilicat befinden sich diejenigen, die durch Zugabe von Wasser zu Ca gebildet werdenzweiJa5 und zu Ca.3Ja5. Die Hydratationsprodukte dieser beiden Verbindungen kommen bei bestimmten Zementsorten am häufigsten vor..
Erhalten
Calciumsilicat wird auf verschiedene Weise durch Umsetzen von siliciumhaltigem Material (wie Kieselgur) und Calciumverbindungen (wie Calciumhydroxid (Ca (OH)) erhalten.zwei).
Calciumsilicat kann beispielsweise durch Kalzinieren von Calciumoxid (CaO) mit Siliciumdioxid (SiO) hergestellt werdenzwei) bei erhöhten Temperaturen.
Wenn die Reaktion in einem Molverhältnis von 1: 1 durchgeführt wird (dies bedeutet, dass es die gleiche Anzahl von CaO-Molekülen wie SiO gibtzwei) führt zu Calciummetasilikat CaSiO3 o CaO • SiOzwei::
CaO + SiOzwei + Wärme → CaSiO3
Anwendungen
Bei der Beschaffung von Ziegeln
Mit Kalziumsilikat werden Einheiten oder Ziegel für den Bau hergestellt. Sie werden mit feinem siliciumhaltigem Material und Branntkalk oder Kalkhydrat erhalten. Inerte Pigmente können hinzugefügt werden, um dem Ziegel eine andere Farbe zu verleihen.
Die Einheiten werden unter Druck geformt und in einem Autoklaven (Dampfofen) bei 170 ° C für 4-6 Stunden gehärtet. Während des Aushärtens reagiert ein Teil des Kalks mit dem siliciumhaltigen Material unter Bildung eines Calciumsilicathydrats, das den Ziegel zusammenhält..

Kalziumsilikatsteine neigen jedoch dazu, sich stärker auszudehnen und zu schrumpfen als Tonsteine, was manchmal zu Rissen im Mauerwerk führen kann..
Dies hat Aufmerksamkeit erregt und sie wurden als potenziell gefährlich angesehen.
In Portlandzement
Calciumsilikate sind Teil von Portlandzement, einem in der Bauindustrie weit verbreiteten Material.
Portlandzement ist ein hydraulischer Zement, der durch Pulverisieren von Materialien hergestellt wird, die hauptsächlich aus hydratisierten Calciumsilikaten und Calciumsulfat-CaSO bestehen4 (Besetzung).

Es härtet aufgrund der Hydratationsreaktion, die ein hydratisiertes Calciumsilikatgel erzeugt, schnell aus. Dies führt zu einem starken, dichten und wenig durchlässigen Material (das kein Wasser durchlässt).
Die darin enthaltenen Silikate sind Tricalciumsilikat Ca.3Ja5 o 3CaO.SiOzwei und Dicalciumsilicat Ca.zweiJa4 oder 2CaO.SiOzwei.
Radioaktiven Müll immobilisieren
Calciumsilikate in Zement können in ihrem Gewichtsprozentsatz variieren. Die Zusammensetzung von Portlandzement kann sich je nach Art der Baukonstruktion, für die er bestimmt ist, ändern..
Einige Arten dieses Zements werden verwendet, um radioaktive Abfälle zu immobilisieren, damit sie weder Menschen noch die Umwelt schädigen..
Als Dämmung für Gebäude
Calciumsilikat wird verwendet, um Mineralschaumplatten oder isolierende Mineralplatten zu erhalten.

Diese dienen dazu, die Wände vor Feuchtigkeit zu schützen. CaO und SiO werden gemischtzwei mit Wasser und 3-6% Cellulose wird hinzugefügt, was die Flexibilität und Stabilität der Kanten verbessert.
Der resultierende Schlamm wird in Formen gegossen und dann mit Dampf auf hohen Druck und hoher Temperatur in einem speziellen Dampfofen erhitzt, der als Autoklav bezeichnet wird..
Das Ergebnis ist ein starrer, sehr feinporiger Schaum, der in Platten oder Bretter geschnitten und mit speziellen Additiven behandelt wird, damit er Wasser abweisen kann..
Kalziumsilikatschaum wird im Bausektor verwendet, insbesondere um Wände zu isolieren und den Feuchtigkeitsschutz zu verbessern. Dies ist insbesondere bei der Renovierung von Altbauten nützlich.
Verringerung der Umweltverschmutzung in der metallurgischen Industrie
Dicalciumsilikat Ca.zweiJa4 oder 2CaO.SiOzwei gefunden in Schlacke oder Abfällen aus der Stahlherstellung wurde verwendet, um gelöste Metalle in sauren Abwässern aus anderen metallurgischen Prozessen auszufällen.
Ausfällen bedeutet, dass das gelöste Metall Teil einer festen Verbindung wird, die zum Boden des Behälters gelangt und gesammelt werden kann.

Die ca.zweiJa4 in Stahlschlacke vorhanden reagiert mit Wasser und erzeugt Ca (OH)zwei welches die Fähigkeit hat, den Säuregehalt von sauren Lösungen von Metallen aus anderen Prozessen zu neutralisieren:
2 Ca.zweiJa4 + 4 hzweiO → 3CaO.2SiOzwei.3HzweiO + Ca (OH)zwei
Zusätzlich zur Neutralisation kann die Calciumsilikatverbindung einen Teil der Metallionen M adsorbierenzwei+ durch Austausch mit dem Calciumion Ca.zwei+. Hier ist eine Übersicht:
≡Si-O-Ca + M.zwei+ → ≡Si-O-M + Ca.zwei+
Die feste Verbindung, die das Metall enthält, kann dann für einen anderen Zweck verwendet werden und wird nicht verworfen. Dies ist ein Beispiel für industrielle Ökologie.
In Biomaterialien
Kalziumsilikatkeramiken wurden seit 1990 als Biomaterialien getestet. Sie wurden aufgrund ihrer Bioaktivität, die anderen Materialien überlegen ist, auf ihre mögliche Verwendung bei der Regeneration von Knochengewebe untersucht..
Dies wird auf die Tatsache zurückgeführt, dass sie Silizium (Si) enthalten, das eine wesentliche Rolle bei den Mechanismen spielt, die zur Bildung von neuem Knochen führen..
Zemente auf Kalziumsilikatbasis können beim Eintauchen in biologische Flüssigkeiten die Bildung einer Kalziumphosphat / Apatit-Beschichtung induzieren und die Geweberegeneration fördern..
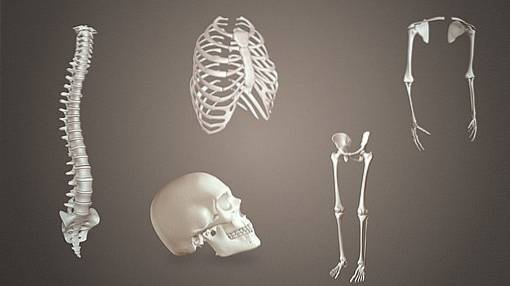
Aus diesen Gründen wird es als geeignetes Material für die Knochenreparatur angesehen..
Im Biodentin
Calciumsilikat ist Teil von Biodentin. Dies ist ein Material, das zur Reparatur von Zahnperforationen, Knochenresorptionen und als Füllung für das Ende der Zahnwurzeln verwendet wird..
Biodentin ist ein bioaktiver Zement mit geringer Porosität, der eine größere mechanische Festigkeit oder Härte als andere Materialien aufweist und Dentin ähnelt.
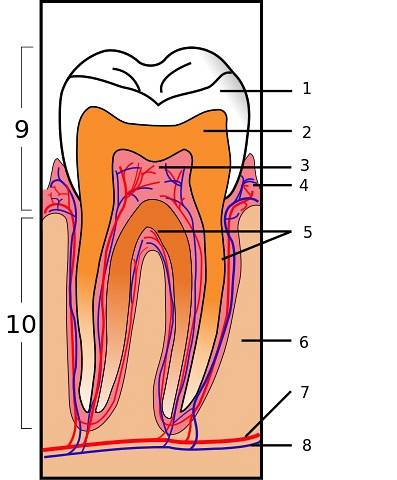
Es besteht aus Tricalciumsilikat (Ca.3Ja5), Dicalciumsilicat (Ca.zweiJa5), Calciumcarbonat (CaCO3) und Zirkonoxid. Kalziumsilikate bilden beim Mischen mit Wasser ein klebriges hydratisiertes Gel, das sich nach einiger Zeit verfestigt und eine harte Struktur bildet..
Es wirkt sich positiv auf die Zellen der Zahnpulpa aus und beschleunigt die Bildung von Brücken im Dentin, wo die Stärke seiner Bindungen, seine Mikrohärte und seine Beständigkeit gegen Kompression hervorgehoben werden..
Andere Apps
Calciumsilikate werden auch als Antibackmittel und Filterhilfsmittel verwendet..
Calciummetasilicat CaSiO3 Verwendung in Keramik, in Vorrichtungen, bei denen Reibung erforderlich ist, wie Fahrzeugbremsen und -kupplungen, und bei der Gewinnung von Metallen.
Aufgrund seiner hohen Helligkeit und Weißheit ist CaSiO3 Es wird zum Befüllen von Farben und Kunststoffen verwendet.
Verweise
- Ropp, R.C. (2013). Erdalkaliverbindungen der Gruppe 14 (C, Si, Ge, Sn und Pb). Calciumsilikate. In der Enzyklopädie der Erdalkaliverbindungen. Von sciencedirect.com wiederhergestellt.
- FAO (2015). Calciumsilicat. Spezifikationen erstellt am 80th JECFA (2015) und veröffentlicht in FAO JECFA Monographs 17. Abgerufen von fao.org.
- Harrisson, A.M. (2019). Aufbau und Spezifikation von Portlandzement. Calciumsilicathydrat. In Leas Chemie von Zement und Beton (5. Auflage). Von sciencedirect.com wiederhergestellt.
- Gellert, R. (2010). Anorganische Mineralstoffe zur Dämmung von Gebäuden. Calciumsilikatschaum und Mineralschaum. In Materialien für Energieeffizienz und thermischen Komfort in Gebäuden. Von sciencedirect.com wiederhergestellt.
- Goudouri, O-M. et al. (2016). Charakterisierung des Abbauverhaltens von biokeramischen Gerüsten. Apatit / Wollastonit-Gerüste. Bei der Charakterisierung und Gestaltung von Gewebegerüsten. Von sciencedirect.com wiederhergestellt.
- Rani, P. et al. (2019). Dental Pulp Capping Nanocomposites. Biodentin. In Anwendungen von Nanokompositmaterialien in der Zahnmedizin. Von sciencedirect.com wiederhergestellt.
- Ingham, J.P. (2013). Betonprodukte. Calciumsilicat-Einheiten. In Geomaterialien unter dem Mikroskop. Von sciencedirect.com wiederhergestellt.
- Ojovan, M.I. und Lee, W.E. (2005). Immobilisierung radioaktiver Abfälle in Zement. Hydraulikzemente. In einer Einführung in die Immobilisierung nuklearer Abfälle. Von sciencedirect.com wiederhergestellt.
- Ramachandra Rao, S. (2006). Rückgewinnung und Recycling von Ressourcen aus metallurgischen Abfällen. Calciumsilikat als Fällungsmittel für gelöste Metalle. In der Abfallwirtschaftsreihe. Von sciencedirect.com wiederhergestellt.
- Prati, C. und Gandolfi, M.G. (2015). Bioaktive Calciumsilikat-Zemente: Biologische Perspektiven und klinische Anwendungen. Dent Mater, 2015 Apr; 31 (4): 351 & ndash; 70. Von ncbi.nlm.nih.gov wiederhergestellt.


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.