
Benedikts Reagenz, wofür es ist, Komponenten, Vorbereitung
Das Benedikts Reagenz ist eine bläuliche Kupferlösung, mit der das Vorhandensein von reduzierenden Zuckern nachgewiesen wird: Aldehyde, Alpha-Hydroxyketone und Hemicetale. Es wurde von Stanley R. Benedict (1884-1936) entwickelt.
Alpha-Hydroxy-Keton-Zucker zeichnen sich durch eine Hydroxylgruppe in der Nähe des Ketons aus. Inzwischen ist ein Hemiketal eine Verbindung, die aus der Zugabe eines Alkohols zu einem Aldehyd oder Keton resultiert. Benedikts Reagenz reagiert wahllos mit all diesen reduzierenden Zuckern.
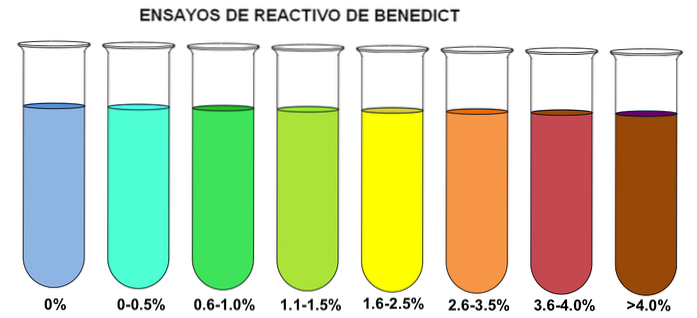
Benedikts Methode basiert auf der reduzierenden Wirkung von Zuckern auf Cuzwei+, von blauer Färbung, die es in Cu umwandelt+. Die CU+ bildet einen ziegelroten Niederschlag aus Kupferoxid. Abhängig von der Zuckerkonzentration erscheint jedoch ein Farbspektrum (oberes Bild).
Beachten Sie, dass wenn Benedict's Reagenz in ein Reagenzglas gegeben wird, ohne Zucker zu reduzieren (0%), sich seine bläuliche Farbe nicht ändert. Wenn die Konzentration höher als 4% ist, wird das Reagenzglas daher braun gefärbt..
Artikelverzeichnis
- 1 Geschichte
- 2 Wofür ist Benedikts Reagenz??
- 2.1 Nachweis von Glukose im Urin
- 2.2 Färben der Lösung
- 2.3 Nachweis verschiedener Monosaccharide und Disaccharide
- 3 Komponenten
- 4 Gebrauchsanweisung
- 5 Benedikts Testreaktion
- 6 Herstellung von Benedikts Reagenz
- 7 Referenzen
Geschichte
Das Reagenz wurde 1909 vom amerikanischen Chemiker Stanley Rossiter Benedict entwickelt, der seine wissenschaftliche Arbeit veröffentlichte Ein Reagenz zum Nachweis von reduzierenden Zuckern, in der Zeitschrift J. Biol. Chem.
Darüber hinaus veröffentlichten Lewis und Benedict (1915) eine Methode zur Bestimmung der Zuckerreduktion im Blut unter Verwendung von Pikrat als Indikator; wurde jedoch aufgrund mangelnder Spezifität nicht mehr verwendet.
Benedikts Reagenz ist Fehlings sehr ähnlich. Sie unterscheiden sich darin, dass Benedict das Citrat-Ion und das Natriumcarbonat-Salz verwendet; während Fehling das Tartration und Natriumhydroxid verwendet.
Der Benedict-Test ist qualitativ, dh er erkennt nur das Vorhandensein von reduzierenden Zuckern. Das Reagenz von Benedict kann jedoch quantitativ sein, wenn es Kaliumthiocyanat in Lösung enthält, das einen weißen Niederschlag von Kupferthiocyanat bildet, der unter Verwendung von Glucosestandards titriert werden kann..
Wofür ist Benedikts Reagenz??
Nachweis von Glukose im Urin
Das Benedict-Reagenz wird weiterhin zum Nachweis des Vorhandenseins von Glukose im Urin verwendet und ist ein Hinweis auf eine Diabeteserkrankung des Patienten, dessen Urin dem Benedict-Test oder -Test unterzogen wird. Es kann jedoch nicht ausgeschlossen werden, dass die Glukosurie einen anderen Ursprung hat.
Beispielsweise findet sich eine erhöhte Glykosurie bei Erkrankungen wie Schwangerschaft, primärer Nierenglykosurie, renaler tubulärer Azidose, primärem oder sekundärem Fanconi-Syndrom, Hyperaldosteronismus und akuter Pankreatitis oder Pankreaskrebs..
Benedikts Reagenz ist aufgrund der Anwesenheit von Cu blauzwei+, welches zu Cu reduziert wird+ durch die Wirkung der Reduzierung von Zuckern; in diesem Fall fällt Glucose unter Bildung eines ziegelroten Kupfer (I) -oxid-Niederschlags aus.
Lösungsfärbung
Die Färbung und Bildung des Niederschlags im Benedict-Test für Urin variiert in Abhängigkeit von der Konzentration des reduzierenden Zuckers. Wenn die Glukosekonzentration im Urin weniger als 500 mg / dl beträgt, wird die Lösung grün und es bildet sich kein Niederschlag.
Eine Uringlukosekonzentration von 500 - 1.000 mg / dl verursacht im Benedict-Test einen grünen Niederschlag. Bei einer Konzentration von mehr als 1.000 bis 1.500 mg / dl bildet sich ein gelber Niederschlag.
Wenn die Glukosekonzentration 1.500 - 2.000 mg / dl beträgt, ist ein orangefarbener Niederschlag zu sehen. Schließlich ist eine Glukosekonzentration im Urin größer als 2.000 mg / dl, was zur Bildung eines ziegelroten Niederschlags führt..
Dies zeigt an, dass der Benedict-Test einen semi-quantitativen Charakter hat und das Ergebnis unter Verwendung von Kreuzen angegeben wird. So entspricht beispielsweise die Bildung eines grünen Niederschlags einem Kreuz (+); und die Bildung eines ziegelroten Niederschlags entspricht vier Kreuzen (++++).
Nachweis verschiedener Monosaccharide und Disaccharide
Das Reagenz von Benedict erkennt das Vorhandensein von reduzierenden Zuckern, die als Teil ihrer Molekülstruktur eine freie funktionelle Gruppe oder eine freie funktionelle Ketongruppe aufweisen. Dies ist der Fall bei Glucose, Galactose, Mannose und Fructose (Monosaccharide) sowie Lactose und Maltose (Disaccharide)..
Saccharose und Stärke reagieren nicht mit Benedikts Reagenz, da sie freie reduzierende Gruppen aufweisen. Darüber hinaus gibt es Verbindungen, die den Benedict-Test im Urin stören und zu einer falschen Positivität führen. Dies ist der Fall bei Salicylat, Penicillin, Streptomycin, Levodopa, Nalidixinsäure und Isoniazid.
Im Urin sind Chemikalien vorhanden, die die Benedict-Reaktion reduzieren können. Zum Beispiel: Kreatinin, Urat und Ascorbinsäure.
Komponenten (bearbeiten)
Die Komponenten von Benedict's Reagenz sind wie folgt: Kupfersulfatpentahydrat, Natriumcarbonat, Trinatriumcitrat und destilliertes Wasser..
Kupfersulfatpentahydrat, CuSO45HzweiO, enthält Cuzwei+: ist die Verbindung, die Benedikts Reagenz seine blaue Farbe verleiht. Reduzierende Zucker wirken auf Cuzwei+, Herstellung seiner Reduktion zu Cu+ und die Bildung eines Niederschlags von Kupferoxid (CuzweiO) ziegelrot.
Natriumcarbonat erzeugt ein alkalisches Medium, das für die Reduktion von Kupfer erforderlich ist. Natriumcarbonat reagiert mit Wasser unter Bildung von Natriumbicarbonat und dem Hydroxylion OH-, verantwortlich für die Alkalität des Mediums, die für den Reduktionsprozess erforderlich ist.
Natriumcitrat bildet mit Kupfer (II) einen Komplex, der verhindert, dass es während der Lagerung zu Cu (I) reduziert wird.
Verwendungsverfahren
5 ml Benedict's Reagenz werden in ein 20 x 160 mm Reagenzglas gegeben und mit 8 Tropfen Urin versetzt. Das Reagenzglas wird vorsichtig geschüttelt und 5-10 Minuten in einen Behälter mit kochendem Wasser gestellt..
Nach dieser Zeit wird das Röhrchen aus dem Heißwasserbad entfernt und seine Oberfläche mit fließendem Wasser gekühlt, um schließlich das Ergebnis des Benedict-Tests (die Farben) abzulesen..
Benedikts Testreaktion
Die Reduktion von Cu (II) während des Benedict-Tests kann wie folgt umrissen werden:
RCHO + 2 Cuzwei+ (im Komplex) + 5 OH- => RCOO- + CuzweiO + 3 H.zweiODER
RCHO = Aldehyd; RCOO- = (Carboxylation); CuzweiO = Kupferoxid, ein ziegelroter Niederschlag.
Herstellung von Benedikts Reagenz
173 g Natriumcitrat und 100 g Natriumcarbonat werden abgewogen und zusammen in 800 ml warmem destilliertem Wasser gelöst. Wenn Spuren von ungelösten Substanzen beobachtet werden, muss die Lösung filtriert werden.
Andererseits werden 17,3 g Kupfersulfatpentahydrat in 100 ml destilliertem Wasser gelöst..
Anschließend werden die beiden wässrigen Lösungen vorsichtig gemischt und unter ständigem Rühren fortgesetzt, wobei mit destilliertem Wasser bis zu 1000 ml aufgefüllt werden..
Verweise
- Graham Solomons T. W., Craig B. Fryhle. (2011). Organische Chemie. Amine. (10th Auflage.). Wiley plus.
- Clark J. (2015). Oxidation von Aldehyden und Ketonen. Wiederhergestellt von: chemguide.co.uk
- Wikipedia. (2020). Benedikts Reagenz. Wiederhergestellt von: en.wikipedia.org
- Redaktion. (9. Januar 2019). Benedikt-Test: Prinzip, Reagenzienvorbereitung, -verfahren und -interpretation. Wiederhergestellt von: laborinfo.com
- Dr. Whitson. (s.f.). Benedikts Reagenz: Ein Test zur Reduzierung von Zucker. Wiederhergestellt von: nku.edu

Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.