
Kalorimeterverlauf, Teile, Typen und deren Eigenschaften
Das Kalorimeter ist ein Gerät zur Messung der Temperaturänderung einer Stoffmenge (normalerweise Wasser) mit bekannter spezifischer Wärme. Diese Temperaturänderung ist auf die Wärme zurückzuführen, die im untersuchten Prozess absorbiert oder freigesetzt wird. chemisch, wenn es sich um eine Reaktion handelt, oder physikalisch, wenn es sich um eine Phasen- oder Zustandsänderung handelt.
Im Labor ist das einfachste Kalorimeter, das gefunden werden kann, das des Kaffeeglases. Es wird verwendet, um die Wärme zu messen, die bei einer Reaktion bei konstantem Druck in wässriger Lösung absorbiert oder freigesetzt wird. Die Reaktionen werden so ausgewählt, dass keine Reagenzien oder gasförmigen Produkte eingreifen.
Wärmemenge, die bei der Reaktion abgegeben wird = vom Kalorimeter aufgenommene Wärmemenge + von der Lösung aufgenommene Wärmemenge
Die vom Kalorimeter aufgenommene Wärmemenge wird als Kalorimeterkapazität des Kalorimeters bezeichnet. Dies wird bestimmt, indem dem Kalorimeter eine bekannte Wärmemenge mit einer gegebenen Wassermasse zugeführt wird. Dann wird der Temperaturanstieg des Kalorimeters und der Lösung enthaltend.
Mit diesen Daten und der Verwendung der spezifischen Wasserwärme (4,18 J / g.ºC) kann die Kalorienkapazität des Kalorimeters berechnet werden. Diese Kapazität wird auch als Kalorimeterkonstante bezeichnet.
Andererseits ist die durch die wässrige Lösung gewonnene Wärme gleich m · ce · Δt. In der Formel m = Wassermasse, ce = spezifische Wasserwärme und Δt = Temperaturschwankung. Wenn Sie dies alles wissen, können Sie die Wärmemenge berechnen, die durch die exotherme Reaktion freigesetzt wird.
Artikelverzeichnis
- 1 Geschichte des Kalorimeters
- 2 Teile
- 3 Typen und ihre Eigenschaften
- 3.1 Das Glas Kaffee
- 3.2 Die kalorimetrische Bombe
- 3.3 Das adiabatische Kalorimeter
- 3.4 Das Isoperibol-Kalorimeter
- 3.5 Das Durchflusskalorimeter
- 3.6 Das Kalorimeter für die Differentialscanningkalorimetrie
- 4 Anwendungen
- 4.1 In der Physikochemie
- 4.2 In biologischen Systemen
- 4.3 Sauerstoffpumpenkalorimeter und Kalorienleistung
- 5 Referenzen
Geschichte des Kalorimeters
Im Jahr 1780 verwendete der französische Chemiker A. L. Lavoisier, der als einer der Väter der Chemie gilt, ein Meerschweinchen, um die Wärmeerzeugung anhand seiner Atmung zu messen.
Wie? Verwendung eines kalorimeterähnlichen Geräts. Die vom Meerschweinchen erzeugte Wärme wurde durch das Schmelzen des Schnees, der die Apparatur umgab, nachgewiesen.
Die Forscher A. L. Lavoisier (1743-1794) und P. S. Laplace (1749-1827) entwarfen ein Kalorimeter, mit dem die spezifische Wärme eines Körpers nach der Methode des Eisschmelzens gemessen wurde.
Das Kalorimeter bestand aus einem zylindrischen, lackierten Zinnbecher, der von einem Stativ getragen und innen mit einem Trichter abgeschlossen wurde. Darin befand sich ein weiteres Glas, ähnlich dem vorherigen, mit einem Rohr, das die äußere Kammer kreuzte und mit einem Schlüssel versehen war. Im zweiten Glas befand sich ein Gitter.
Das Wesen oder Objekt, dessen spezifische Wärme bestimmt werden sollte, wurde auf dieses Gitter gelegt. Eis wurde wie im Korb in die konzentrischen Gläser gegeben.
Die vom Körper erzeugte Wärme wurde vom Eis absorbiert und schmolz. Und das flüssige Wasserprodukt des Schmelzens des Eises wurde gesammelt, wodurch der innere Glashahn geöffnet wurde.
Und schließlich wog das Wasser, die Masse des geschmolzenen Eises war bekannt.
Teile
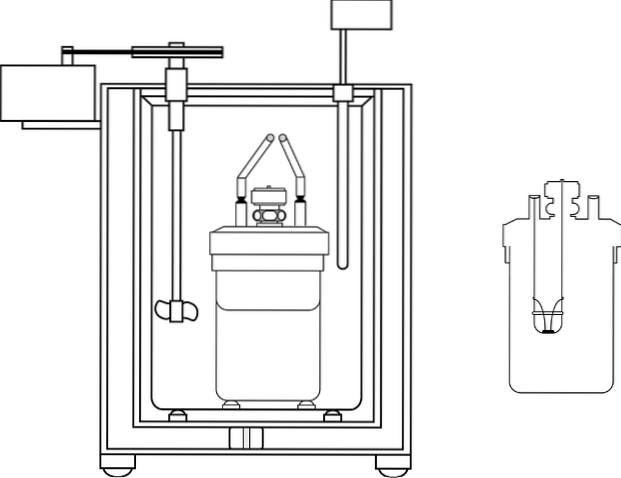
Das in Chemie-Lehrlabors am häufigsten verwendete Kalorimeter ist das sogenannte Kaffeetassenkalorimeter. Dieses Kalorimeter besteht aus einem Becher oder stattdessen einem Behälter mit Anime-Material, der bestimmte Isoliereigenschaften aufweist. In diesem Behälter befindet sich die wässrige Lösung mit dem Körper, der Wärme erzeugen oder absorbieren wird.
Ein Deckel aus Isoliermaterial mit zwei Löchern wird auf den oberen Teil des Behälters gelegt. In einem ist ein Thermometer eingesetzt, um Temperaturänderungen zu messen, und in dem anderen ein Rührer, vorzugsweise aus Glasmaterial, der die Funktion erfüllt, den Inhalt der wässrigen Lösung zu bewegen..
Das Bild zeigt die Teile eines Bombenkalorimeters; Es ist jedoch ersichtlich, dass das Thermometer und der Rührer gemeinsame Elemente in mehreren Kalorimetern haben.
Typen und ihre Eigenschaften
Die Tasse Kaffee
Es ist dasjenige, das zur Bestimmung der durch eine exotherme Reaktion freigesetzten Wärme und der bei einer endothermen Reaktion absorbierten Wärme verwendet wird..
Darüber hinaus kann es zur Bestimmung der spezifischen Wärme eines Körpers verwendet werden; das heißt, die Wärmemenge, die ein Gramm der Substanz aufnehmen muss, um ihre Temperatur um ein Grad Celsius zu erhöhen. .
Die kalorimetrische Bombe
Es ist ein Gerät, bei dem die Wärmemenge gemessen wird, die bei einer Reaktion mit konstantem Volumen abgegeben oder absorbiert wird.
Die Reaktion findet in einem stabilen Stahlbehälter (der Pumpe) statt, der in ein großes Wasservolumen eingetaucht ist. Dies hält die Wassertemperaturänderungen klein. Daher wird angenommen, dass die mit der Reaktion verbundenen Änderungen bei konstantem Volumen und konstanter Temperatur gemessen werden..
Das Obige zeigt an, dass keine Arbeit erledigt wird, wenn eine Reaktion in einem Bombenkalorimeter durchgeführt wird.
Die Reaktion beginnt mit der Stromversorgung über an die Pumpe angeschlossene Kabel.
Das adiabatische Kalorimeter
Es zeichnet sich durch eine isolierende Struktur aus, die als Abschirmung bezeichnet wird. Die Abschirmung befindet sich um die Zelle herum, wo Wärme- und Temperaturänderungen auftreten. Ebenso ist es an ein elektronisches System angeschlossen, das seine Temperatur sehr nahe an der der Zelle hält, um eine Wärmeübertragung zu vermeiden..
In einem adiabatischen Kalorimeter wird der Temperaturunterschied zwischen dem Kalorimeter und seiner Umgebung minimiert; sowie Minimierung des Wärmeübergangskoeffizienten und der Zeit für den Wärmeaustausch.
Seine Teile bestehen aus:
-Die Zelle (oder der Behälter), die in ein Isolationssystem integriert ist, mit dessen Hilfe versucht wird, Wärmeverluste zu vermeiden.
-Das Thermometer zur Messung von Temperaturänderungen.
-Eine Heizung, die an eine steuerbare elektrische Spannungsquelle angeschlossen ist.
-Und der Schild, schon erwähnt.
Bei diesem Kalorimetertyp können Eigenschaften wie Entropie, Debye-Temperatur und Zustandselektronendichte bestimmt werden..
Das Isoperibol-Kalorimeter
Es ist eine Vorrichtung, bei der die Reaktionszelle und die Pumpe in eine Struktur eingetaucht sind, die als Mantel bezeichnet wird. In diesem Fall besteht der sogenannte Mantel aus Wasser, das auf einer konstanten Temperatur gehalten wird.
Die Zellen- und Pumpentemperaturen steigen, wenn während des Verbrennungsprozesses Wärme freigesetzt wird. Die Wassermanteltemperatur wird jedoch auf einer festen Temperatur gehalten.
Ein Mikroprozessor steuert die Temperatur der Zelle und des Mantels und nimmt die erforderlichen Korrekturen für die Leckwärme vor, die sich aus den Unterschieden zwischen den beiden Temperaturen ergibt..
Diese Korrekturen werden kontinuierlich und mit einer endgültigen Korrektur basierend auf Messungen vor und nach dem Test angewendet..
Das Durchflusskalorimeter
Es wurde von Caliendar entwickelt und verfügt über eine Vorrichtung zum Bewegen eines Gases in einem Behälter mit konstanter Geschwindigkeit. Durch Wärmezufuhr wird der Temperaturanstieg in der Flüssigkeit gemessen.
Das Durchflusskalorimeter zeichnet sich aus durch:
- Eine genaue Messung der Geschwindigkeit des konstanten Durchflusses.
- Genaue Messung der Wärmemenge, die durch eine Heizung in die Flüssigkeit eingeleitet wird.
- Eine genaue Messung des Temperaturanstiegs im Gas, der durch den Energieeintrag verursacht wird
- Ein Entwurf zur Messung der Kapazität eines unter Druck stehenden Gases.
Das Kalorimeter für die Differentialscanningkalorimetrie
Es zeichnet sich durch zwei Behälter aus: In einem wird die zu untersuchende Probe platziert, während der andere leer gehalten wird oder ein Referenzmaterial verwendet wird..
Die beiden Gefäße werden mittels zweier unabhängiger Heizgeräte mit konstanter Energierate beheizt. Wenn sich die beiden Gefäße zu erwärmen beginnen, zeichnet der Computer die Differenz des Wärmeflusses von den Heizgeräten gegen die Temperatur auf, wodurch der Wärmefluss bestimmt werden kann..
Weiterhin kann die Variation der Temperatur als Funktion der Zeit bestimmt werden; und schließlich die Kalorienkapazität.
Anwendungen
In der Physikochemie
-Mit den Basiskalorimetern vom Typ Kaffeetasse kann die Wärmemenge gemessen werden, die ein Körper abgibt oder aufnimmt. In ihnen kann festgestellt werden, ob eine Reaktion exotherm oder endotherm ist. Zusätzlich kann die spezifische Wärme eines Körpers bestimmt werden.
-Mit dem adiabatischen Kalorimeter konnten die Entropie eines chemischen Prozesses und die elektronische Dichte des Zustands bestimmt werden.
In biologischen Systemen
-Mikrokalorimeter werden verwendet, um biologische Systeme zu untersuchen, die Wechselwirkungen zwischen Molekülen sowie die auftretenden molekularen Konformationsänderungen umfassen. zum Beispiel bei der Entfaltung eines Moleküls. Die Linie umfasst sowohl Differential-Sweep als auch isotherme Titration.
-Das Mikrokalorimeter wird bei der Entwicklung von niedermolekularen Arzneimitteln, Biotherapeutika und Impfstoffen eingesetzt.
Sauerstoffpumpenkalorimeter und Kalorienleistung
Im Sauerstoffbombenkalorimeter findet die Verbrennung zahlreicher Substanzen statt und deren Kalorienwert kann bestimmt werden. Zu den mit diesem Kalorimeter untersuchten Substanzen gehören: Kohle und Koks; schwere und leichte Speiseöle; Benzin und alle Kraftstoffe.
Sowie die Arten von Brennstoffen für Flugzeugreaktoren; Kraftstoffabfälle und Abfallentsorgung; Lebensmittel und Nahrungsergänzungsmittel für die menschliche Ernährung; Futterpflanzen und Ergänzungsmittel für Tierfutter; Baumaterialien; Raketentreibstoffe und Treibmittel.
Ebenso wurde die Kalorienleistung durch Kalorimetrie in thermodynamischen Studien an brennbaren Materialien bestimmt; bei der Untersuchung der Energiebilanz in der Ökologie; in Sprengstoffen und thermischen Pulvern und in der Vermittlung grundlegender thermodynamischer Methoden.
Verweise
- Whitten, Davis, Peck & Stanley. Chemie. (8. Aufl.). CENGAGE Lernen.
- González J., Cortés L. und Sánchez A. (s.f.). Adiabatische Kalorimetrie und ihre Anwendungen. Wiederhergestellt von: cenam.mx
- Wikipedia. (2018). Kalorimeter. Wiederhergestellt von: en.wikipedia.org
- Helmenstine, Anne Marie, Ph.D. (22. Juni 2018). Kalorimeter Definition in der Chemie. Wiederhergestellt von :oughtco.com
- Gillespie, Claire. (11. April 2018). Wie funktioniert ein Kalorimeter? Wissenschaft. Wiederhergestellt von: sciencing.com



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.