
Guanin Eigenschaften, Struktur, Bildung und Funktionen
Das Guanin Es ist eine stickstoffhaltige Base, die zur Biosynthese von Guanylat-5'-monophosphat und Desoxyguanylat-5'-monophosphat dient. Beide Substanzen sind Teil von RNA bzw. DNA, die die genetische Information von Zellen speichern.
Ribonukleinsäure (RNA) und Desoxyribonukleinsäure (DNA) bestehen aus Nukleotiden, die aus einer stickstoffhaltigen Base bestehen, die an eine Zucker- und eine Phosphatgruppe gebunden ist.
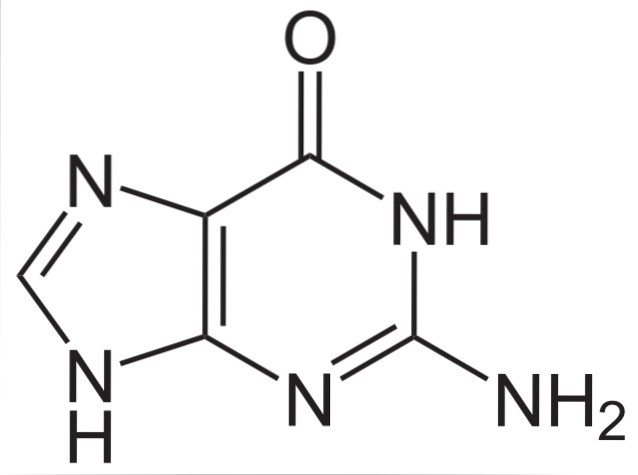
Guanin ist nicht nur Teil von Nukleinsäuren, sondern in seinen Formen der Nukleoside Monophosphat, Diphosphat und Triphosphate (GMP, GDP und GTP) auch an Prozessen wie dem Energiestoffwechsel, der Translation des intrazellulären Signals, der Physiologie von Photorezeptoren und der Vesikelfusion beteiligt.
Artikelverzeichnis
- 1 Chemische Struktur
- 2 Funktionen
- 3 Biosynthese
- 4 Funktion
- 5 Verwandte Krankheiten
- 5.1 Lesch-Nyhan-Syndrom
- 5.2 Erhöhte PRPP-Synthase-Aktivität
- 5.3 von Gierke-Syndrom
- 6 Referenzen
Chemische Struktur
Die chemische Struktur von Guanin (2-Amino-6-hydroxypurin) ist ein heterocyclischer Purinring, der aus einem System von zwei verbundenen Ringen besteht: Ein Ring ist Pyrimidin und der andere Ring ist Imidazol..
Der heterocyclische Ring von Guanin ist flach und weist einige konjugierte Doppelbindungen auf. Zusätzlich hat es zwei tautomere Formen, die Keto- und die Enolform, zwischen den C-1- und N-6-Gruppen..
Eigenschaften
Die Eigenschaften von Guanin sind wie folgt:
- Guanin ist eine unpolare Substanz. Es ist in Wasser unlöslich, aber in konzentrierten Lösungen starker Säuren oder Basen löslich.
- Es kann als weißer Feststoff mit der Summenformel C isoliert werden5H.5N.5O und Molekulargewicht 151,3 g / mol.
- Die Eigenschaft der DNA, Licht bei 260 nm zu absorbieren, beruht teilweise auf der chemischen Struktur von Guanin.
- In der DNA bildet Guanin drei Wasserstoffbrücken. Die C-6-Carbonylgruppe ist ein Wasserstoffbrückenbindungsakzeptor, die N-1-Gruppe und die C-2-Aminogruppe sind Wasserstoffbrückenbindungsdonoren.
Aus diesem Grund wird mehr Energie benötigt, um eine Bindung zwischen einem Guanin und einem Cytosin aufzubrechen, als die eines Adenins mit einem Thymin, da das letztere Paar nur durch zwei Wasserstoffbrücken verbunden ist..
- In der Zelle wird es immer als Teil von Nukleinsäuren oder als GMP, GDP und GTP gefunden, niemals in seiner freien Form.
Biosynthese
Das Guaninmolekül wird wie andere Purine synthetisiert de novo von 5-Phosphoribosyl-1-pyrophosphat (PRPP) durch durch Enzyme katalysierte Reaktionen.
Der erste Schritt besteht in der Addition einer Aminogruppe von Glutamin an PRPP und der Bildung von 5-Phosphoribosylamin (PRA).
Anschließend erfolgt in einer geordneten Reihenfolge die Zugabe von Glycin, Aspartat, Glutamin, Formiat und Kohlendioxid zum PRA. Auf diese Weise wird ein Zwischenmetabolit namens Inosin-5'-monophosphat (IMP) gebildet..
Während dieses Prozesses wird freie Energie aus der Hydrolyse von ATP (Adenosin-5'-triphosphat) verwendet, wodurch ADP (Adenosin-5'-diphosphat) und Pi (anorganisches Phosphat) entstehen..
Eine Oxidation von IMP ist abhängig von NAD+ (Nicotinamidadenindinukleotid) produziert Xanthin-5'-monophosphat (XMP). Die anschließende Addition einer Aminogruppe an XMP erzeugt das Guanylatmolekül.
Die Regulation der Guanylatbiosynthese erfolgt zu Beginn der PRA-Bildung und am Ende der IMP-Oxidation. Die Regulation erfolgt durch negative Rückkopplung: Ein GMP-Nukleotid hemmt Enzyme in beiden Stadien.
Während des metabolischen Abbaus von Nukleotiden werden stickstoffhaltige Basen recycelt. GMP wird durch das Enzym Hypoxanthin-Guanin-Phosphoribosyltransferase gebildet, das eine Phosribosylgruppe von PRPP auf Guanin überträgt.
Funktion
Da Guanin nicht in seiner freien Form vorkommt, sind seine Funktionen mit GMP, GDP und GTP verbunden. Einige von ihnen sind unten aufgeführt:
- Guanosin-5'-triphosphat (GTP) wirkt als Reservoir für freie Energie. Die Gammaphosphatgruppe von GTP kann auf Adenosin-5'-triphosphat (ADP) übertragen werden, um ATP zu bilden. Diese Reaktion ist reversibel und wird durch die Nucleosiddiphosphatkinase katalysiert..
- GMP ist die stabilste Form des Nukleotids, das Guanin enthält. Durch Hydrolyse bildet GMP in den Translationswegen cyclisches GMP (cGMP), das während der intrazellulären Signalübertragung ein zweiter Botenstoff ist. Zum Beispiel in den Photorezeptor- und Chemorezeptor-Geruchszellen.
- CGMP ist an der Entspannung der Blutgefäße der glatten Muskulatur während der Stickoxidbiosynthese in Endothelzellen beteiligt.
- Die GTP-Gammaphosphat-Hydrolyse dient als freie Energiequelle für die Proteinbiosynthese in Ribosomen.
- Hellicase-Enzyme benötigen freie Energie aus der GTP-Hydrolyse, um die DNA-Doppelhelix während der DNA-Replikation und -Transkription zu trennen.
- In Hippocampus-Neuronen wird die Wirkung von spannungsgesteuerten Natriumkanälen durch die Hydrolyse von GTP zu GDP reguliert..
Verwandte Krankheiten
Hohe Harnsäurespiegel im Blut und Urin wurden mit drei verschiedenen Stoffwechselstörungen in Verbindung gebracht, die wir weiter unten sehen werden..
Lesch-Nyhan-Syndrom
Es ist gekennzeichnet durch einen Mangel an HPRT (Hypoxanthin-Guanin-Phosphoribosyl-Transferase), einem Enzym, das für das Recycling von Hypoxanthin und Guanin wichtig ist. In diesem Fall steigen die PRPP-Spiegel und IMP und GMP, zwei wichtige Regulatoren des Anfangsstadiums der Purinsynthese, werden nicht gebildet. All dies begünstigt die Biosynthese de novo von Purinen.
Erhöhte PRPP-Synthase-Aktivität
Dies führt zu einem Anstieg der PRPP-Spiegel. Dieser Metabolit wirkt als Aktivator der Glutamin-PRPP-Amidotransferase, die für die Synthese von 5-Phosphoribosylamin verantwortlich ist und die Biosynthese erhöht de novo Purine.
Von-Gierke-Syndrom
Es ist eine Krankheit, die mit der Speicherung von Glykogen vom Typ I zusammenhängt. Patienten mit diesem Syndrom haben eine defekte Glucose-6-Phosphatase. Dies führt zu einem Anstieg der Glucose-6-phosphat-Spiegel, der zur Synthese von Ribose-5-phosphat über Pentosephosphat dient..
Ribose-5-phosphat ist der Ausgangsmetabolit für die PRPP-Biosynthese. Ähnlich wie in den beiden vorhergehenden Fällen führt dies zu einer Erhöhung der Biosynthese de novo von Purinen.
Erhöhte Harnsäure im Blut und Urin verursacht Symptome, die allgemein als Gicht bekannt sind. Im Fall des Lesch-Nyhan-Syndroms fehlt den Patienten die Aktivität des HPRP-Enzyms vollständig, was zur Manifestation anderer Symptome wie Lähmungen und geistiger Behinderung führt..
Das HPRP-Gen befindet sich auf dem X-Chromosom. Daher betreffen Mutationen in diesem Gen Männer. Es gibt keine Behandlung zur Behandlung neurologischer Probleme. Symptome, die mit einem Anstieg der Harnsäure verbunden sind, werden mit Allopurinol behandelt.
Verweise
- Dawson, R. et al. 1986. Daten für die biochemische Forschung. Clarendon Press, Oxford.
- Horton, R; Moran, L; Scrimgeour, G; Perry, M. und Rawn, D. 2008. Prinzipien der Biochemie. 4. Auflage. Pearson Ausbildung.
- Mathews, Van Holde, Ahern. 2001. Biochemistry. 3. Auflage.
- Murray, R; Granner, D; Mayes, P. und Rodwell, V. 2003. Harper's Illustrated Biochemistry. 26. Ausgabe. McGraw-Hill-Unternehmen.
- Nelson, DL und Cox, M. 1994. Lehninger. Prinzipien der Biochemie. 4. Auflage. Ed Omega.
- Sigma-Aldrich. 2019. Guanine Chemical Sheet. Word Wide Web-Adresse: sigmaaldrich.com.


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.