
Entamoeba histolytica Morphologie, Lebenszyklus, Symptome

Entamoeba histolytica Es ist ein parasitärer Mikroorganismus des Darms beim Menschen. Es kann Caniden und andere Wirbeltiere parasitieren. Es ist der Erreger von Amöbenruhr oder Amöbiasis.
Es ist ein anaerober Organismus, der als Kommensal im Dickdarm leben oder in die Schleimhaut eindringen und signifikante Läsionen verursachen kann. Vom Darm aus kann er extrainstestinale Leber-, Lungen- und sogar Hirngewebe infizieren. Es können pathogene und nicht pathogene Stämme existieren.
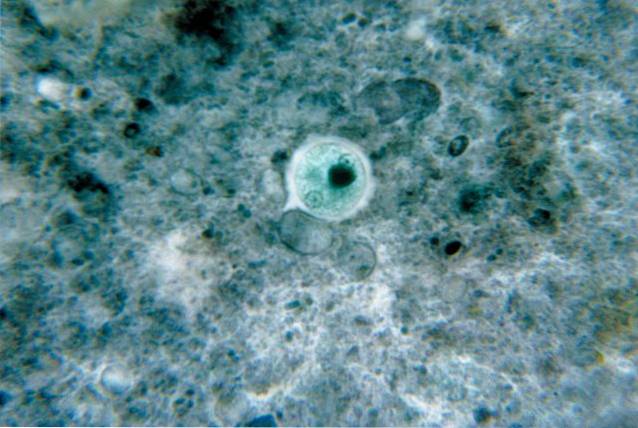
Amöbenruhr ist eine der parasitären Erkrankungen mit der höchsten Morbidität und Mortalität beim Menschen in tropischen Ländern. Es gilt als dritthäufigste Todesursache nach Malaria und Bilharziose.
Faktoren wie unzureichende Abfallentsorgungssysteme für Fäkalien, Trinkwasserversorgung und unzureichender Umgang mit Lebensmitteln tragen zur Existenz endemischer Gebiete auf der Welt bei..
Artikelverzeichnis
- 1 Biologische Eigenschaften von Entamoeba histolytica
- 2 Morphologie
- 3 Lebenszyklus
- 3.1 E. histolitica hat einen direkten oder monoxenischen Lebenszyklus, dh es wird ein einzelner Wirt für seine Entwicklung benötigt. Es präsentiert keine biologischen Vektoren in seinem Lebenszyklus.
- 3.2 Es können jedoch mechanische Vektoren wie Mausfliegen bereitgestellt werden, die nicht aktiv an ihrem Zyklus teilnehmen, sondern nur infektiöse Formen zu Nahrung und Wasser transportieren..
- 3.3 Die Infektion erfolgt nach Einnahme von Tetra-Keimzysten in kontaminierten Lebensmitteln und Wasser. Weil die Wirkung von Magensäften die Zystenwand verdaut.
- 3.4 Die Zysten platzen und bilden Trophozoiten. Diese vermehren sich durch binäre Spaltung und dringen in die Schleimhaut des Dickdarms ein, insbesondere in den Dickdarm, der der Hauptlebensraum für ihre aktive Entwicklung ist..
- 3.5 Einige Trophozoiten können in die Darmwand eindringen und Epithelzellen zerstören. Sie produzieren Lektine, die es ihnen ermöglichen, an Darmzellen zu haften und durch Proteinasen zu lysieren. Vom Darm aus können sie in extraintestinale Gewebe eindringen und in Leber-, Lungen- und Gehirngewebe eindringen.
- 4 Symptome
- 5 Diagnose
- 6 Behandlung
- 7 Kontrolle und Prävention
- 8 Referenzen
Biologische Eigenschaften von Entamoeba histolytica
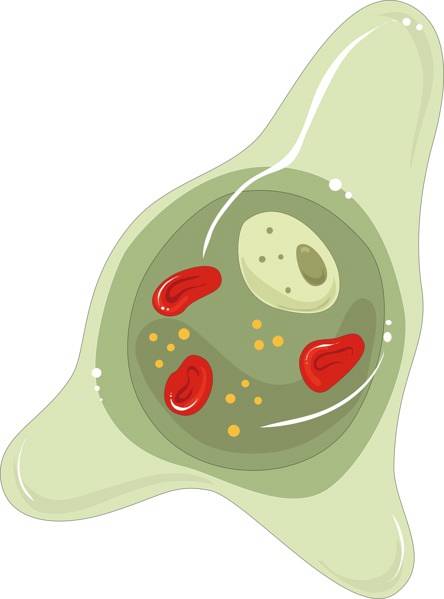
E. histolytica Es zeigt zwei parasitäre Formen: die Zyste und die Trophozoiten. Die Zyste ist die infektiöse Form, sie hat keine Fortbewegung und ist in der äußeren Umgebung resistent; Trophozoiten stellen die vegetative Form dar, sie sind mobil und aktiv.
E. histolytica ernährt sich durch Phagozytose, dh es emittiert Pseudopoden, mit denen es die kleinen Partikel, aus denen seine Nahrung besteht, in seinen Zellinhalt einführt, wo es verdaut wird.
Die Trophozoiten- und Zystenphasen sind in seiner Entwicklung vorhanden. Trophozoiten sind die mobile, amöboidale Form. Die Zyste ist die nicht aktive Form, die gegen widrige Bedingungen resistent ist.
Morphologie
E. histolytica ist morphologisch nicht von Kommensalamöben zu unterscheiden E. dispar Y. E. moshkovskii. Es kann unterschieden werden von E coli, eine andere Art, die beim Menschen vorkommt, weil diese keine Pseudopoden emittiert.
Der Trophozoit hat eine zentrale Masse, die als Endoplasma bezeichnet wird, und eine äußere Schicht, die als Ektoplasma bekannt ist. Sie haben einen Kern mit einem zentralen Karyosom und peripherem Chromatin, die regelmäßig verteilt sind.
Es hat ein vorderes Ende, das Pseudopodien bilden kann, und ein hinteres Ende, das eine Zwiebel oder ein Uroid mit einem Büschel Filopodien zur Ansammlung von Trümmern darstellt. Präsentiert ein System, das aus einem Netzwerk von Verdauungsvakuolen und Ribosomen besteht.
Die Trophozoiten können in zwei Formen vorliegen: Magna und Minuta. Die Magna-Form misst 20 bis 30 Mikrometer und kann dicke Pseudopodien emittieren; Die winzige Form misst 19 bis 20 Mikrometer und kann kürzere Pseudopoden emittieren.
Zysten sind rund oder kugelförmig. Unter dem Mikroskop zeigen sie Brechung, es ist ersichtlich, dass die Membran je nach Reife ein bis vier Kerne enthält.
Metazysten haben eine dünnere Membran. Die Kerne sind stabförmig mit abgerundeten Enden und Glykogenvakuolen. Im Zytoplasma sehen Sie die chromatidalen Körper, bei denen es sich um Glykogeneinschlüsse im Zytoplasma handelt.
Lebenszyklus
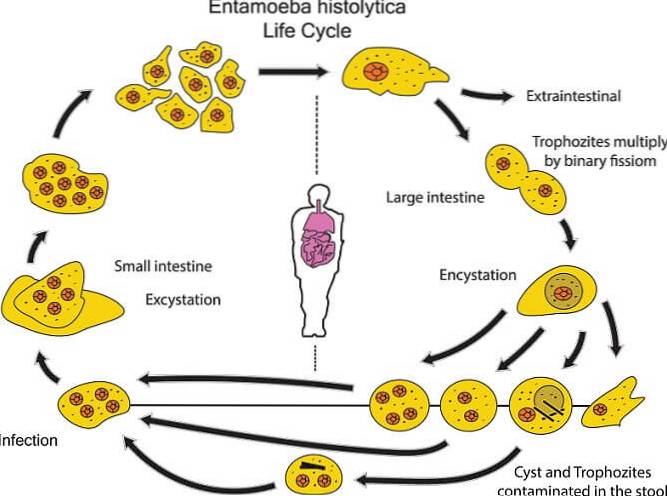
E. histolitica Es hat einen direkten oder monoxenischen Lebenszyklus, dh es benötigt einen einzelnen Wirt für seine Entwicklung. Es präsentiert keine biologischen Vektoren in seinem Lebenszyklus.
Es kann jedoch mechanische Vektoren wie Mausfliegen bereitstellen, die nicht aktiv an ihrem Zyklus teilnehmen, sondern nur infektiöse Formen zu Nahrung und Wasser transportieren..
Die Infektion erfolgt nach Einnahme von Tetra-Keimzysten in kontaminierten Nahrungsmitteln und Wasser. Weil die Wirkung von Magensäften die Zystenwand verdaut.
Die Zysten platzen und bilden Trophozoiten. Diese vermehren sich durch binäre Spaltung und dringen in die Schleimhaut des Dickdarms ein, insbesondere in den Dickdarm, der der Hauptlebensraum für ihre aktive Entwicklung ist..
Einige Trophozoiten können in die Darmwand eindringen und Epithelzellen zerstören. Sie produzieren Lektine, die es ihnen ermöglichen, an Darmzellen zu haften und durch Proteinasen zu lysieren. Vom Darm aus können sie in extraintestinale Gewebe eindringen und in Leber-, Lungen- und Gehirngewebe eindringen.
Im Dickdarm entstehen nichtkernige Prezysten, die sich zunehmend in reife oder vierkernige Zysten verwandeln, die die infizierenden Formen des Parasiten darstellen..
Die kontaminierte Person scheidet sowohl Zysten als auch Trophozoiten über ihren Kot aus, der Wasser und Nahrung kontaminiert. Mit der Aufnahme kontaminierter Lebensmittel beginnt ein neuer Wirt.
Symptome
Die parasitierte Person kann asymptomatisch bleiben oder leichte oder schwere Symptome aufweisen. Am häufigsten sind leichte Fälle, die 90% von ihnen ausmachen.
Leichte symptomatische Fälle zeigen Übelkeit, Durchfall, Gewichtsverlust, Fieber und Bauchschmerzen. In chronischen Fällen können Koliken auftreten, einschließlich Geschwüren und dem Vorhandensein von Blut im Stuhl..
Wenn eine extraintestinale Invasion auftritt, ist die häufigste Erkrankung der Leberabszess, der Fieber und Schmerzen im Oberbauch verursacht..
Diagnose
Die Diagnose wird durch Untersuchung des Stuhls unter einem Lichtmikroskop gestellt. In den Proben werden Formen des Parasiten identifiziert, in Fällen, die positiv für Amöbiasis sind. Serienuntersuchungen mit mindestens drei an aufeinanderfolgenden Tagen analysierten Proben werden empfohlen.
Die Verwendung von PCR oder Serologie mit spezifischen Antikörpern sind ebenfalls nützliche Diagnosetechniken..
In extraintestinalen Fällen kann die Diagnose durch CT-Bilder gestellt werden..
Schleim und Blut können je nach Schwere der Infektion im Stuhl auftreten.
Behandlung
Die Abgabe von Metronidazol, Paromomycin und Tinidazol wurde verwendet. In Fällen einer extraintestinalen Invasion, wie z. B. Leberabszessen, wurde eine Operation angewendet.
Es wird empfohlen, die Diagnose gut zu überprüfen, um falsche Identifikationen aufgrund des Vorhandenseins von Arten wie z E. dispar Y. E. moshkovskii. Die unsachgemäße Anwendung häufig verwendeter Arzneimittel führt zur Bildung resistenter Stämme.
Kontrolle und Prävention
In der Welt konzentrieren sich Gesundheitsstrategien auf die Anwendung von Maßnahmen, die den biologischen Kreislauf des Parasiten unter Beteiligung der verschiedenen beteiligten sozialen Akteure unterbrechen sollen..
Dabei ist die bewusste Beteiligung der Gemeinschaften vor allem in Bereichen mit epidemiologischem Risiko von großer Bedeutung. Unter anderem können wir erwähnen:
- Aufklärung der Bevölkerung über Amöbiasis, ihren Lebenszyklus und die Ansteckungsrisiken
- Aufrechterhaltung angemessener Sanitärsysteme zur Ablagerung und Behandlung von Kot.
- Aufrechterhaltung angemessener Versorgungssysteme und Zugang zu Trinkwasser.
- Verfügbarkeit der Infrastruktur und Zugang der Bevölkerung zu Diagnosediensten und zur Versorgung der Betroffenen.
Verweise
- Chacín-Bonilla, L. (2013). Amöbiasis: klinische, therapeutische und diagnostische Aspekte der Infektion. Medical Journal of Chile, 141 (5): 609 & ndash; 615.
- Diamond, L.S. & Clark, C.G. (1993). Eine Neubeschreibung von Entamoeba histolytica Schaudinn, 1903 (emended Walker, 1911) trennt es von Entamoeba dispar Brumpt, 1925. Journal of Eukaryotic Microbiology, 40: 340 & ndash; 344.
- Elsheikha, H. M., Regan, C.S. & Clark, C.G. (2018). Neuartige Entamoeba-Funde bei nichtmenschlichen Primaten. Trends in Parasitology, 34 (4): 283 & ndash; 294.
- Gómez, J.C., Cortés J.A., Cuervo, S.I. &, López, M.C. (2007). Intestinale Amöbiasis. Infectio, 11 (1): 36 & ndash; 45.
- Showler, A. & Boggild, A. (2013). Entamoeba histolytica. Canadian Medical Association Journal, 185 (12): 1064.



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.