
Chemische Gleichungsteile und Beispiele

Das chemische Gleichung Es ist eine schematische Darstellung einiger Eigenschaften einer chemischen Reaktion. Man kann auch sagen, dass die chemische Gleichung die Veränderungen beschreibt, die die verschiedenen an einer Reaktion beteiligten Substanzen erfahren.
Die Formeln und Symbole der verschiedenen beteiligten Substanzen werden in die chemische Gleichung eingefügt, wobei die Anzahl der Atome jedes in den Verbindungen vorhandenen Elements deutlich angegeben wird. Dies erscheint als Index und kann nicht durch Abwägen der Gleichung geändert werden.
Die chemische Gleichung muss ausgewogen erscheinen, dh die Anzahl der Atome sowohl der Reaktanten als auch der Produkte muss gleich sein. Auf diese Weise wird das Gesetz der Erhaltung der Materie eingehalten. Es ist wünschenswert, dass die zum Ausgleich der Gleichungen verwendeten Zahlen ganze Zahlen sind.
Diese Gleichungen zeigen weder die aufeinanderfolgenden Schritte noch durch welche Mechanismen die Reaktanten in Produkte umgewandelt werden..
Das ist der Grund, warum sie, obwohl sie sehr nützlich sind, um zu verstehen, wohin eine chemische Reaktion verläuft, nicht die molekularen Aspekte verstehen oder wie sie von bestimmten Variablen beeinflusst werden. wie pH, Viskosität, Reaktionszeit, Rührgeschwindigkeit, unter anderem.
Artikelverzeichnis
- 1 Teile einer chemischen Gleichung
- 1.1 Ort der Reagenzien und Produkte
- 1.2 Chemische Gleichungen ausgleichen
- 1.3 Physikalische Zustände der Komponenten der chemischen Gleichung
- 1.4 Änderungen des physischen Zustands
- 2 Beispiel für chemische Gleichungen
- 2.1 - Photosynthese
- 2.2 - Zellatmung
- 2.3 - Reaktionen gemeinsamer Elemente
- 3 Referenzen
Teile einer chemischen Gleichung
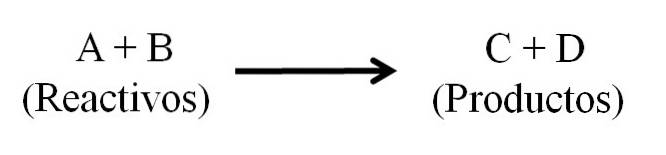
Grundsätzlich besteht eine chemische Gleichung aus drei Hauptteilen: den Reaktanten, den Produkten und dem Pfeil, der die Richtung der chemischen Reaktion angibt..
Ort der Reagenzien und Produkte
Alle Substanzen, die als Reaktanten fungieren, und alle Substanzen, die Produkte sind, erscheinen in der chemischen Gleichung. Diese Stoffgruppen sind durch einen Pfeil getrennt, der die Reaktionsrichtung angibt. Die Reagenzien befinden sich links vom Pfeil und die Produkte rechts.
Der Pfeil bedeutet, was erzeugt wird und ist von links nach rechts ausgerichtet (→), obwohl es bei reversiblen Reaktionen zwei äquivalente und parallele Pfeile gibt; eine nach rechts und eine nach links gerichtet. Das Symbol (Δ) befindet sich normalerweise über dem Pfeil und zeigt an, dass bei der Reaktion Wärme verwendet wurde..
Zusätzlich wird die Kennzeichnung des Katalysators üblicherweise auf dem Pfeil platziert, wenn möglich mit seiner Formel oder seinem Symbol. Die verschiedenen Substanzen, die als Reaktanten erscheinen, sind durch das Zeichen (+) getrennt, was darauf hinweist, dass die Substanzen miteinander reagieren oder sich miteinander verbinden.
Bei Stoffen, die als Produkte erscheinen, hat das Zeichen (+) nicht die vorherige Konnotation. es sei denn, die Reaktion ist reversibel. Es ist zweckmäßig, dass das Zeichen (+) in gleichem Abstand von den Substanzen steht, die es trennt.
Chemische Gleichungen ausgleichen
Es ist eine wesentliche Voraussetzung, dass die chemischen Gleichungen richtig ausgeglichen sind. Hierzu wird eine Zahl mit dem Namen stöchiometrischer Koeffizient gesetzt. Bei Bedarf muss dieser Koeffizient vor den Substanzen stehen, die als Reaktanten oder Produkte auftreten..
Damit soll erreicht werden, dass die Anzahl aller Atome der Elemente, die als Reaktanten erscheinen, genau der Anzahl der Atome entspricht, die im Produkt erscheinen. Die einfachste Methode zum Ausgleich chemischer Gleichungen ist Versuch und Irrtum..
Physikalische Zustände der Komponenten der chemischen Gleichung
In einigen chemischen Gleichungen ist der physikalische Zustand von Substanzen mit einem Index gekennzeichnet. Hierzu werden im Spanischen folgende Abkürzungen verwendet: (s) für den Festkörper; (l) für den flüssigen Zustand; (g) gasförmiger Zustand; und (ac) wässrige Lösung.
Beispiel: Reaktion von Calciumcarbonat mit Salzsäure.
Dieb3 (s) + 2 HCl(ac) → CaCl2 (s) + H.zweiODER(l) + CO2 g)
Änderungen im physischen Zustand
In einigen Fällen wird in der chemischen Gleichung angegeben, ob bei der chemischen Reaktion ein Gas entsteht oder ob eine der erzeugten Substanzen ausfällt.
Das Vorhandensein eines Gases wird durch einen vertikalen Pfeil angezeigt, dessen Ende nach oben zeigt (↑) und der sich auf der rechten Seite der gasförmigen Substanz befindet.
Beispiel: Reaktion von Zink mit Salzsäure.
Zn + 2 HCl → ZnClzwei + H.zwei↑
Wenn bei der chemischen Reaktion eine der Substanzen einen Niederschlag bildet, wird dies durch Platzieren eines vertikalen Pfeils mit dem Ende nach unten (↓) auf der rechten Seite der ausgefällten Substanz symbolisiert..
Beispiel: Reaktion von Salzsäure mit Silbernitrat.
HCl + AgNO3 → HNO3 + AgCl ↓
Beispiel für chemische Gleichungen
- Photosynthese

Die Photosynthese ist ein Prozess, bei dem Pflanzen Lichtenergie aus dem Sonnenlicht einfangen und umwandeln, um die für ihren Lebensunterhalt notwendige Energie zu erzeugen. Die Photosynthese wird von einigen Organellen pflanzlicher Zellen durchgeführt, die als Chloroplasten bezeichnet werden.
Thylakoide finden sich in der Chloroplastenmembran, Stellen, an denen Chlorophylle gefunden werden. zu Y. b, Welches sind die Hauptpigmente, die Lichtenergie einfangen.
Obwohl die Photosynthese ein komplexer Prozess ist, kann sie in der folgenden chemischen Gleichung beschrieben werden:
6 COzwei + 6 hzweiO → C.6H.12ODER6 + 6 O.zwei↑ ΔGº = 2.870 kJ / mol
C.6H.12ODER6 Es ist die Formel für Glukose, ein Kohlenhydrat, das zur Herstellung von ATP metabolisiert wird. Verbindung, die das Hauptreservoir der Energie in den meisten Lebewesen ist. Zusätzlich wird NADPH aus Glucose erzeugt, einem Coenzym, das für viele Reaktionen notwendig ist..
- Zellatmung
Zellen verwenden Sauerstoff für den Stoffwechsel zahlreicher Substanzen, die in aufgenommenen Lebensmitteln enthalten sind. In der Zwischenzeit wird ATP als Energiequelle für die Aktivitäten von Lebewesen verwendet, die bei diesen Prozessen Kohlendioxid und Wasser produzieren..
Wenn Glukose als Modell für eine metabolisierte Substanz verwendet wird, kann die Atmung unter Verwendung der folgenden chemischen Gleichung schematisiert werden:
C.6H.12ODER6 + 6 O.zwei → 6 COzwei + 6 hzweiODER
- Gemeinsame Elementreaktionen
Zersetzungsreaktion
Eine Verbindung oder Verbindungen dissoziieren und bilden mit ihren Atomen andere unterschiedliche Verbindungen:
2 KClO3 (s) → 2 KCl(s) + 3 O.2 g)
Verdrängungsreaktion
Ein Metall reagiert mit einer Verbindung und ersetzt ein darin vorhandenes Metall:
Mg(s) + KURS4 (ac) → Cu(s) + MgSO4 (ac)
Eliminierungsreaktion
Bei dieser Art von Reaktion nimmt die Anzahl der an ein Kohlenstoffatom gebundenen Atome oder Gruppen ab:
CH3-CHzweiBr + NaOH → H.zweiC = CHzwei + H.zweiO + NaBr
Hydratationsreaktion
Es ist eine Reaktion, bei der eine Verbindung ein Wassermolekül hinzufügt. Diese Reaktion ist wichtig bei der Herstellung von Alkoholen:
H.zweiC = CHzwei + H.zweiO → H.zweiC-CHzweiOh
Neutralisierungsreaktion
Eine Base oder ein Alkali reagiert mit einer Säure unter Bildung von Salz und Wasser:
HCl(ac) + NaOH(ac) → NaCl(ac) + H.zweiODER(l)
Synthesereaktion
Bei dieser Art von Reaktion werden zwei oder mehr Substanzen kombiniert, um eine neue Verbindung zu bilden:
2 Li(s) + Cl2 g) → 2 LiCl(s)
Doppelverdrängungsreaktion (Metathese)
Bei dieser Art der Reaktion werden positive und negative Ionen ausgetauscht, um neue Verbindungen zu bilden:
AgNO3 (ac) + NaCl(ac) → AgCl(s) + Älterer Bruder3 (ac)
Verweise
- Flores, J. (2002). Chemie. Ausgabe 1es war. Editorial Santillana
- C. K. Mathews, K. E. Van Holde und K. G. Ahern (2002). Biochemie. 3es war Auflage. Herausgeber Pearson Addison Wesley
- Whitten, Davis, Peck & Stanley. (2008). Chemie. (8. Aufl.). CENGAGE Lernen.
- Wikipedia. (2019). Chemische Gleichung. Wiederhergestellt von: en.wikipedia.org
- Helmenstine, Anne Marie, Ph.D. (20. September 2019). Was ist eine chemische Gleichung? Wiederhergestellt von :oughtco.com


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.