
Kohlenstoff in der Natur Lage, Eigenschaften und Verwendungen

Das Kohlenstoff in der Natur Es kann unter anderem in Diamanten, Öl und Graphiten gefunden werden. Dieses chemische Element nimmt im Periodensystem den sechsten Platz ein und befindet sich in der horizontalen Zeile oder Periode 2 und Spalte 14. Es ist nichtmetallisch und vierwertig; Das heißt, Sie können 4 gemeinsame elektronenchemische Bindungen oder kovalente Bindungen herstellen.
Kohlenstoff ist das am häufigsten vorkommende Element in der Erdkruste. Diese Fülle, seine einzigartige Vielfalt bei der Bildung organischer Verbindungen und seine außergewöhnliche Fähigkeit, Makromoleküle oder Polymere bei auf der Erde üblichen Temperaturen zu bilden, machen es zu einem gemeinsamen Element aller bekannten Lebensformen..

Kohlenstoff existiert in der Natur als chemisches Element, ohne sich in Form von Graphit und Diamant zu verbinden. Zum größten Teil wird es jedoch zu chemischen Kohlenstoffverbindungen wie Calciumcarbonat (CaCO) kombiniert3) und andere Verbindungen in Öl und Erdgas.
Es bildet auch verschiedene Mineralien wie Anthrazit, Kohle, Braunkohle und Torf. Die größte Bedeutung von Kohlenstoff besteht darin, dass er den sogenannten „Baustein des Lebens“ darstellt und in allen lebenden Organismen vorhanden ist..
Artikelverzeichnis
- 1 Wo und in welcher Form befindet sich Kohlenstoff??
- 1.1 Kristalline Formen
- 1.2 Amorphe Formen
- 1.3 Öl, Erdgas und Bitumen
- 2 Physikalische und chemische Eigenschaften
- 2.1 Chemisches Symbol
- 2.2 Ordnungszahl
- 2.3 Physikalischer Zustand
- 2.4 Farbe
- 2,5 Atommasse
- 2.6 Schmelzpunkt
- 2.7 Siedepunkt
- 2.8 Dichte
- 2.9 Löslichkeit
- 2.10 Elektronische Konfiguration
- 2.11 Anzahl der Elektronen in der äußeren oder Valenzschale
- 2.12 Verbindungskapazität
- 2.13 Verkettung
- 3 Biogeochemischer Kreislauf
- 3.1 Photosynthese
- 3.2 Atmung und Zersetzung
- 3.3 Geologische Prozesse
- 3.4 Eingriffe durch menschliche Aktivitäten
- 4 Verwendungen
- 4.1 Öl und Erdgas
- 4.2 Graphit
- 4.3 Diamant
- 4.4 Anthrazit
- 4.5 Kohle
- 4.6 Braunkohle
- 4.7 Torf
- 5 Referenzen
Wo und in welcher Form befindet sich Kohlenstoff??
Kohlenstoff ist nicht nur die gemeinsame chemische Komponente in allen Lebensformen, sondern liegt auch in drei kristallinen Formen vor: Diamant, Graphit und Fulleren..
Es gibt auch verschiedene amorphe Mineralformen von Kohle (Anthrazit, Braunkohle, Kohle, Torf), flüssigen Formen (Ölsorten) und gasförmigen (Erdgas).
Kristalline Formen
In kristallinen Formen verbinden sich Kohlenstoffatome zu geordneten Mustern mit geometrischer räumlicher Anordnung.
Graphit
Es ist ein weicher schwarzer Feststoff mit einem metallischen Glanz oder Glanz und hitzebeständig (feuerfest). Seine kristalline Struktur weist Kohlenstoffatome auf, die in hexagonalen Ringen verbunden sind, die sich wiederum zu Folien verbinden.
Graphitvorkommen sind selten und wurden in China, Indien, Brasilien, Nordkorea und Kanada gefunden..
Diamant
Es ist ein sehr harter Feststoff, transparent für den Lichtdurchgang und viel dichter als Graphit: Der Wert der Diamantdichte ist fast doppelt so hoch wie der von Graphit.
Die Kohlenstoffatome im Diamanten sind in tetraedrischer Geometrie verbunden. Ebenso wird Diamant aus Graphit gebildet, der Bedingungen sehr hoher Temperaturen und Drücke (3000) ausgesetzt ist °C und 100.000 atm).
Die meisten Diamanten befinden sich zwischen 140 und 190 km tief im Mantel. Durch tiefe Vulkanausbrüche kann Magma sie in oberflächennahe Entfernungen transportieren.
Es gibt Diamantenvorkommen in Afrika (Namibia, Ghana, Demokratische Republik Kongo, Sierra Leone und Südafrika), Amerika (Brasilien, Kolumbien, Venezuela, Guyana, Peru), Ozeanien (Australien) und Asien (Indien)..

Fullerene
Es handelt sich um molekulare Formen von Kohlenstoff, die in fast kugelförmigen Molekülen Cluster von 60 und 70 Kohlenstoffatomen bilden, ähnlich wie Fußbälle..
Es gibt auch kleinere Fullerene mit 20 Kohlenstoffatomen. Einige Formen von Fullerenen umfassen Kohlenstoffnanoröhren und Kohlenstofffasern..

Amorphe Formen
In amorphen Formen vereinigen sich die Kohlenstoffatome nicht und bilden eine geordnete und regelmäßige Kristallstruktur. Stattdessen enthalten sie sogar Verunreinigungen aus anderen Elementen.
Anthrazit
Es ist die älteste metamorphe Mineralkohle (die aus der Modifizierung von Gesteinen durch Temperatur-, Druck- oder chemische Einflüsse von Flüssigkeiten stammt), da ihre Entstehung aus der Primär- oder Paläozoikum-Zeit stammt, der Karbonperiode.
Anthrazit ist die amorphe Form von Kohlenstoff mit dem höchsten Gehalt an diesem Element: zwischen 86 und 95%. Es hat eine grau-schwarze Farbe mit metallischem Glanz und ist schwer und kompakt..
Anthrazit kommt im Allgemeinen in geologischen Verformungszonen vor und macht etwa 1% der weltweiten Kohlenreserven aus..
Geografisch ist es in Kanada, USA, Südafrika, Frankreich, Großbritannien, Deutschland, Russland, China, Australien und Kolumbien zu finden.

Kohle
Es ist eine Mineralkohle, ein Sedimentgestein organischen Ursprungs, dessen Entstehung aus dem Paläozoikum und dem Mesozoikum stammt. Es hat einen Kohlenstoffgehalt zwischen 75 und 85%.
Es hat eine schwarze Farbe, zeichnet sich durch Undurchsichtigkeit und ein mattes und fettiges Aussehen aus, da es einen hohen Gehalt an bituminösen Substanzen aufweist. Es wird durch Verdichtung von Braunkohle im Paläozoikum, in der Karbon- und Perm-Zeit gebildet.
Es ist die am häufigsten vorkommende Form von Kohlenstoff auf dem Planeten. In den USA, Großbritannien, Deutschland, Russland und China gibt es große Kohlevorkommen.
Braunkohle
Es ist eine mineralische fossile Kohle, die im Tertiär aus Torf durch Kompression (hoher Druck) gebildet wurde. Es hat einen niedrigeren Kohlenstoffgehalt als Kohle, zwischen 70 und 80%.
Es ist ein Material, das nicht sehr kompakt, bröckelig (eine Eigenschaft, die es von anderen Kohlenstoffmineralien unterscheidet), braun oder schwarz ist. Seine Textur ähnelt der von Holz und sein Kohlenstoffgehalt liegt zwischen 60 und 75%.
Es ist ein leicht zu entzündender Brennstoff mit niedrigem Heizwert und geringerem Wassergehalt als Torf..
Es gibt wichtige Braunkohlebergwerke in Deutschland, Russland, der Tschechischen Republik, Italien (Venetien, Toskana, Umbrien) und Sardinien. In Spanien befinden sich die Braunkohlevorkommen in Asturien, Andorra, Saragossa und La Coruña.
Torf
Es ist ein Material organischen Ursprungs, dessen Entstehung aus der Quartärzeit stammt, viel jünger als frühere Kohlen.
Es hat eine bräunlich-gelbe Farbe und erscheint in Form einer schwammigen Masse mit geringer Dichte, in der Sie Pflanzenreste von dem Ort sehen können, an dem sie entstanden sind..
Im Gegensatz zu den oben genannten Kohlen stammt Torf nicht aus Karbonisierungsprozessen von Holz oder Holz, sondern wurde durch die Ansammlung von Pflanzen - hauptsächlich Gräser und Moose - in sumpfigen Gebieten durch einen Karbonisierungsprozess gebildet, der noch nicht abgeschlossen wurde..
Torf hat einen hohen Wassergehalt; Aus diesem Grund muss es vor Gebrauch getrocknet und verdichtet werden.
Es hat einen niedrigen Kohlenstoffgehalt (nur 55%); Daher hat es einen niedrigen Energiewert. Bei Verbrennung sind die Ascherückstände reichlich vorhanden und geben viel Rauch ab.
Es gibt wichtige Torfvorkommen in Chile, Argentinien (Feuerland), Spanien (Espinosa de Cerrato, Palencia), Deutschland, Dänemark, Holland, Russland, Frankreich.

Öl, Erdgas und Bitumen
Öl (aus dem Lateinischen petrae, was "Stein" bedeutet; Y. Oleum, was "Öl" bedeutet: "Steinöl") ist eine Mischung aus vielen organischen Verbindungen - den meisten Kohlenwasserstoffen -, die durch anaerobe bakterielle Zersetzung (in Abwesenheit von Sauerstoff) von organischer Substanz erzeugt werden.
Es wurde im Untergrund in großen Tiefen und unter besonderen Bedingungen sowohl physikalisch (hohe Drücke und Temperaturen) als auch chemisch (Vorhandensein spezifischer Katalysatorverbindungen) in einem Millionen Jahre dauernden Prozess gebildet.
Während dieses Prozesses wurden C und H aus den organischen Geweben freigesetzt und wieder zusammengefügt, um eine immense Anzahl von Kohlenwasserstoffen zu bilden, die sich entsprechend ihren Eigenschaften mischen und Erdgas, Öl und Bitumen bilden..
Die Ölfelder des Planeten befinden sich hauptsächlich in Venezuela, Saudi-Arabien, Irak, Iran, Kuwait, den Vereinigten Arabischen Emiraten, Russland, Libyen, Nigeria und Kanada.
Unter anderem in Russland, Iran, Venezuela, Katar, den USA, Saudi-Arabien und den Vereinigten Arabischen Emiraten gibt es Erdgasreserven.
Physikalische und chemische Eigenschaften
Unter den Eigenschaften von Kohlenstoff können wir Folgendes erwähnen:
Chemisches Symbol
C..
Ordnungszahl
6.
Körperlicher Status
Fest, unter normalen Druck- und Temperaturbedingungen (1 Atmosphäre und 25 °C).
Farbe
Grau (Graphit) und transparent (Diamant).
Atommasse
12,011 g / mol.
Schmelzpunkt
500 °C..
Siedepunkt
827 °C..
Dichte
2,62 g / cm3.
Löslichkeit
Unlöslich in Wasser, löslich in CCl-Tetrachlorkohlenstoff4.
Elektronische Konfiguration
1szwei 2szwei 2 P.zwei.
Anzahl der Elektronen in der äußeren oder Valenzschale
4.
Verbindungskapazität
4.
Verkettung
Hat die Fähigkeit, chemische Verbindungen in langen Ketten zu bilden.
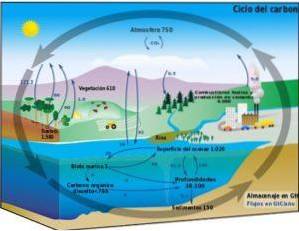
Biogeochemischer Kreislauf
Der Kohlenstoffkreislauf ist ein biogeochemischer Kreislaufprozess, durch den Kohlenstoff zwischen der terrestrischen Biosphäre, der Atmosphäre, der Hydrosphäre und der Lithosphäre ausgetauscht werden kann..
Die Kenntnis dieses zyklischen Kohlenstoffprozesses auf der Erde ermöglicht es uns, menschliches Handeln in diesem Kreislauf und seine Folgen für den globalen Klimawandel zu demonstrieren.
Kohlenstoff kann zwischen den Ozeanen und anderen Gewässern sowie zwischen der Lithosphäre, im Boden und im Untergrund, in der Atmosphäre und in der Biosphäre zirkulieren. In der Atmosphäre und in der Hydrosphäre liegt Kohlenstoff in gasförmiger Form als CO vorzwei (Kohlendioxid).
Photosynthese
Kohlenstoff aus der Atmosphäre wird von terrestrisch und aquatisch produzierenden Organismen von Ökosystemen (photosynthetischen Organismen) eingefangen..
Die Photosynthese ermöglicht eine chemische Reaktion zwischen COzwei und Wasser, vermittelt durch Sonnenenergie und Chlorophyll aus Pflanzen, um Kohlenhydrate oder Zucker zu produzieren. Dieser Prozess transformiert einfache Moleküle mit einem niedrigen CO-Energiegehaltzwei, H.zweiO und Sauerstoff O.zwei, in komplexen hochenergetischen molekularen Formen, die Zucker sind.
Heterotrophe Organismen - die nicht photosynthetisieren können und Verbraucher in Ökosystemen sind - erhalten Kohlenstoff und Energie, indem sie sich von Produzenten und anderen Verbrauchern ernähren.
Atmung und Zersetzung
Atmung und Zersetzung sind biologische Prozesse, die Kohlenstoff in Form von CO an die Umwelt abgebenzwei oder CH4 (Methan, das bei anaerober Zersetzung erzeugt wird, dh in Abwesenheit von Sauerstoff).
Geologische Prozesse
Durch geologische Prozesse und als Folge des Zeitablaufs kann der Kohlenstoff aus der anaeroben Zersetzung in fossile Brennstoffe wie Öl, Erdgas und Kohle umgewandelt werden. Ebenso ist Kohlenstoff auch Teil anderer Mineralien und Gesteine.
Eingriffe durch menschliche Aktivitäten
Wenn der Mensch die Verbrennung fossiler Brennstoffe zur Energiegewinnung nutzt, kehrt Kohlenstoff in Form großer Mengen an CO in die Atmosphäre zurück.zwei das kann nicht durch den natürlichen biogeochemischen Kohlenstoffkreislauf aufgenommen werden.
Dieser Überschuss an COzwei Die durch menschliche Aktivitäten hervorgerufene Wirkung wirkt sich negativ auf das Gleichgewicht des Kohlenstoffkreislaufs aus und ist die Hauptursache für die globale Erwärmung.
Anwendungen
Die Verwendung von Kohlenstoff und seinen Verbindungen ist äußerst vielfältig. Die bekanntesten mit folgenden:
Öl und Erdgas
Die hauptsächliche wirtschaftliche Verwendung von Kohlenstoff wird durch seine Verwendung als Kohlenwasserstoff mit fossilen Brennstoffen wie Methangas und Öl dargestellt.
Öl wird in Raffinerien destilliert, um mehrere Derivate wie Benzin, Diesel, Kerosin, Asphalt, Schmiermittel, Lösungsmittel und andere zu erhalten, die wiederum in der petrochemischen Industrie verwendet werden, die Rohstoffe für die Kunststoff-, Düngemittel-, Arzneimittel- und Farbenindustrie herstellt. unter anderem.
Graphit
Graphit wird in folgenden Aktionen verwendet:
- Es wird zur Herstellung von Stiften verwendet, die mit Tonen gemischt werden.
- Es ist Teil der Herstellung von feuerfesten feuerfesten Ziegeln und Tiegeln.
- In verschiedenen mechanischen Geräten wie Unterlegscheiben, Lagern, Kolben und Dichtungen.
- Es ist ein ausgezeichnetes Festschmiermittel.
- Aufgrund seiner elektrischen Leitfähigkeit und seiner chemischen Inertheit wird es zur Herstellung von Elektroden und Kohlenstoffen für Elektromotoren verwendet..
- Es wird als Moderator in Kernkraftwerken eingesetzt.
Diamant
Diamant hat besonders außergewöhnliche physikalische Eigenschaften, wie den höchsten bisher bekannten Grad an Härte und Wärmeleitfähigkeit.
Diese Eigenschaften ermöglichen aufgrund seiner hohen Abrasivität industrielle Anwendungen in Werkzeugen, die zur Herstellung von Schnitten und Instrumenten zum Polieren verwendet werden..
Seine optischen Eigenschaften - wie Transparenz und die Fähigkeit, weißes Licht aufzubrechen und Licht zu brechen - geben ihm viele Anwendungen in optischen Instrumenten, wie beispielsweise bei der Herstellung von Linsen und Prismen..
Der charakteristische Glanz, der sich aus seinen optischen Eigenschaften ergibt, wird auch in der Schmuckindustrie hoch geschätzt..
Anthrazit
Anthrazit ist schwer zu entzünden, brennt langsam und benötigt viel Sauerstoff. Seine Verbrennung erzeugt eine kleine hellblaue Flamme und gibt viel Wärme ab.
Anthrazit wurde vor einigen Jahren in thermoelektrischen Anlagen und zur Heizung im Haushalt eingesetzt. Seine Verwendung hat Vorteile wie die Erzeugung von wenig Asche oder Staub, wenig Rauch und einen langsamen Verbrennungsprozess..
Aufgrund seiner hohen wirtschaftlichen Kosten und seiner Knappheit wurde Anthrazit in thermoelektrischen Anlagen durch Erdgas und in Haushalten durch Elektrizität ersetzt.
Kohle
Kohle wird als Rohstoff verwendet, um Folgendes zu erhalten:
- Koks, Brennstoff für Hochöfen in Stahlwerken.
- Kreosot, das durch Mischen der Teerdestillate aus Kohle gewonnen und als Schutzversiegelung für Holz verwendet wird, das den Elementen ausgesetzt ist.
- Kresol (chemisch Methylphenol), aus Kohle gewonnen und als Desinfektionsmittel und Antiseptikum verwendet,
- Andere Derivate wie Gas, Teer oder Pech sowie Verbindungen, die unter anderem zur Herstellung von Parfums, Insektiziden, Kunststoffen, Farben, Reifen und Straßenbelägen verwendet werden.
Braunkohle
Braunkohle ist ein Kraftstoff mittlerer Qualität. Jet, eine Braunkohlensorte, zeichnet sich durch einen sehr kompakten Karbonisierungsprozess und hohe Drücke aus und wird in Schmuck und Ornamenten verwendet.
Torf
Torf wird in den folgenden Aktivitäten verwendet;
- Für das Wachstum, die Unterstützung und den Transport von Pflanzenarten.
- Als Bio-Kompost.
- Wie Tierstreu in Ställen.
- Als minderwertiger Kraftstoff.
Verweise
- A. Burrows, J. Holman, A. Parsons, G. Pilling und G. Price (2017). Chemie3: Einführung in die anorganische, organische und physikalische Chemie. Oxford University Press.
- Deming, A. (2010). König der Elemente? Nanotechnologie. 21 (30): 300201. doi: 10.1088
- M. Dienwiebel, G. Verhoeven, N. Pradeep, J. Frenken, J. Heimberg und H. Zandbergen (2004). Überschmierfähigkeit von Graphit. Briefe zur körperlichen Überprüfung. 92 (12): 126101. doi: 10.1103
- T. Irifune, A. Kurio, S. Sakamoto, T. Inoue und H. Sumiya (2003). Materialien: Ultraharter polykristalliner Diamant aus Graphit. Natur. 421 (6923): 599 & ndash; 600. doi: 10.1038
- Savvatimskiy, A. (2005). Messungen des Schmelzpunktes von Graphit und der Eigenschaften von flüssigem Kohlenstoff (eine Übersicht für 1963-2003). Kohle. 43 (6): 1115. doi: 10.1016


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.