
Atomvolumen Wie es im Periodensystem und in den Beispielen variiert
Das Atomvolumen ist ein relativer Wert, der die Beziehung zwischen der Molmasse eines Elements und seiner Dichte angibt. Dieses Volumen hängt also von der Dichte des Elements ab, und die Dichte hängt wiederum von der Phase und der Anordnung der Atome darin ab..
Das Atomvolumen für ein Element Z ist also in einer anderen Phase als der bei Raumtemperatur (flüssig, fest oder gasförmig) oder wenn es Teil bestimmter Verbindungen ist, nicht dasselbe. Somit unterscheidet sich das Atomvolumen von Z in Verbindung ZA von dem von Z in Verbindung ZB.

Warum? Um es zu verstehen, ist es notwendig, Atome beispielsweise mit Murmeln zu vergleichen. Die Murmeln haben wie die bläulichen im Bild oben einen sehr gut definierten Materialrand, der dank ihrer glänzenden Oberfläche sichtbar ist. Im Gegensatz dazu ist die Grenze der Atome diffus, obwohl sie als entfernt kugelförmig betrachtet werden können.
Was also einen Punkt jenseits der Atomgrenze bestimmt, ist die Nullwahrscheinlichkeit, ein Elektron zu finden, und dieser Punkt kann weiter oder näher am Kern liegen, abhängig davon, wie viele benachbarte Atome um das betrachtete Atom herum interagieren..
Artikelverzeichnis
- 1 Atomvolumen und Radius
- 2 Zusätzliche Formel
- 3 Wie variiert das Atomvolumen im Periodensystem??
- 3.1 Atomvolumen von Übergangsmetallen
- 4 Beispiele
- 4.1 Beispiel 1
- 4.2 Beispiel 2
- 5 Referenzen
Atomvolumen und Radius
Durch Wechselwirkung zweier H-Atome im H-Molekülzwei, Die Positionen ihrer Kerne werden ebenso definiert wie die Abstände zwischen ihnen (internukleare Abstände). Wenn beide Atome kugelförmig sind, ist der Radius der Abstand zwischen dem Kern und der Fuzzy-Grenze:
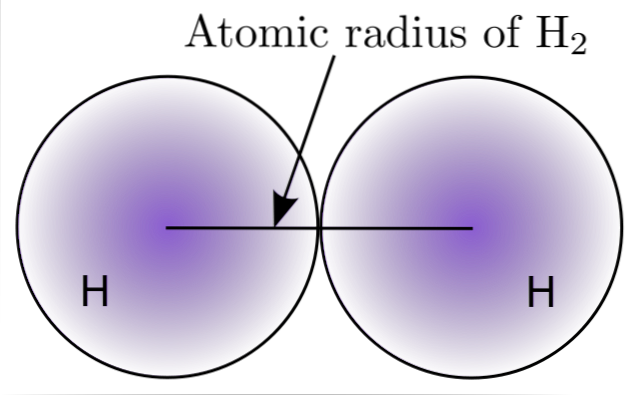
Im Bild oben sehen Sie, wie die Wahrscheinlichkeit, ein Elektron zu finden, abnimmt, wenn es sich vom Kern entfernt. Wenn man dann den Abstand zwischen den Kernen durch zwei teilt, erhält man den Atomradius. Als nächstes wird unter der Annahme einer sphärischen Geometrie für die Atome die Formel verwendet, um das Volumen einer Kugel zu berechnen:
V = (4/3) (Pi) r3
In diesem Ausdruck ist r der für das H-Molekül bestimmte Atomradiuszwei. Der nach dieser ungenauen Methode berechnete Wert von V kann sich ändern, wenn beispielsweise H berücksichtigt wirdzwei in flüssigem oder metallischem Zustand. Diese Methode ist jedoch sehr ungenau, da die Formen der Atome in ihren Wechselwirkungen sehr weit von der idealen Sphäre entfernt sind..
Zur Bestimmung der Atomvolumina in Festkörpern werden viele Variablen bezüglich der Anordnung berücksichtigt, die durch Röntgenbeugungsstudien erhalten werden..
Zusätzliche Formel
Die Molmasse drückt die Menge an Materie aus, die ein Mol Atome eines chemischen Elements enthält.
Seine Einheiten sind g / mol. Andererseits ist die Dichte das Volumen, das ein Gramm des Elements einnimmt: g / ml. Da die Einheiten des Atomvolumens ml / mol sind, müssen Sie mit den Variablen spielen, um zu den gewünschten Einheiten zu gelangen:
(g / mol) (ml / g) = ml / mol
Oder was ist das gleiche:
(Molmasse) (1 / D) = V.
(Molmasse / D) = V.
Somit kann das Volumen eines Mols Atome eines Elements leicht berechnet werden; wohingegen mit der Formel des Kugelvolumens das Volumen eines einzelnen Atoms berechnet wird. Um diesen Wert von Anfang an zu erhalten, ist eine Konvertierung über die Avogadro-Nummer (6.02 · 10) erforderlich-2. 3).
Wie variiert das Atomvolumen im Periodensystem??
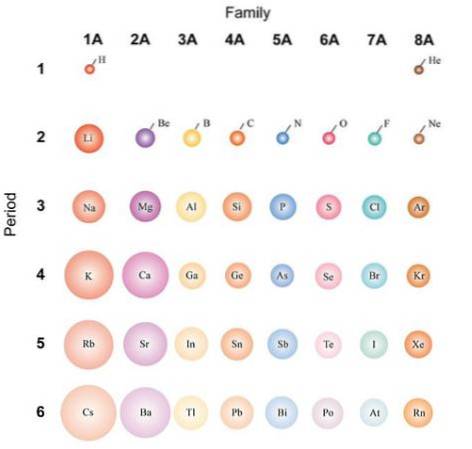
Wenn die Atome als sphärisch betrachtet werden, ist ihre Variation dieselbe wie die in Atomradien beobachtete. In dem obigen Bild, das repräsentative Elemente zeigt, ist dargestellt, dass die Atome von rechts nach links kleiner werden; stattdessen werden sie von oben nach unten voluminöser.
Dies liegt daran, dass der Kern im gleichen Zeitraum Protonen enthält, wenn er sich nach rechts bewegt. Diese Protonen üben eine Anziehungskraft auf die externen Elektronen aus, die eine effektive Kernladung Z fühlenef, weniger als die tatsächliche Kernladung Z..
Die Elektronen der inneren Schalen stoßen die der äußeren Schale ab und verringern die Wirkung des Kerns auf sie; Dies wird als Bildschirmeffekt bezeichnet. Im gleichen Zeitraum kann der Bildschirmeffekt der Zunahme der Anzahl der Protonen nicht entgegenwirken, sodass die Elektronen in der inneren Hülle die Kontraktion der Atome nicht verhindern..
Der Abstieg in eine Gruppe ermöglicht jedoch neue Energieniveaus, die es den Elektronen ermöglichen, weiter vom Kern entfernt zu kreisen. Ebenso nimmt die Anzahl der Elektronen in der inneren Hülle zu, deren Abschirmeffekte sich zu verringern beginnen, wenn der Kern erneut Protonen hinzufügt..
Aus diesen Gründen wird anerkannt, dass die Gruppe 1A im Gegensatz zu den kleinen Atomen der Gruppe 8A (oder 18) die voluminösesten Atome aufweist, die der Edelgase..
Atomvolumina von Übergangsmetallen
Übergangsmetallatome bauen Elektronen in innere d-Orbitale ein. Diese Zunahme des Bildschirmeffekts und der realen Kernladung Z hebt sich nahezu gleich auf, so dass ihre Atome im gleichen Zeitraum eine ähnliche Größe behalten..
Mit anderen Worten: In einer Periode weisen Übergangsmetalle ähnliche Atomvolumina auf. Diese kleinen Unterschiede sind jedoch bei der Definition von Metallkristallen von enormer Bedeutung (als wären sie metallische Murmeln)..
Beispiele
Zur Berechnung des Atomvolumens eines Elements stehen jeweils zwei mathematische Formeln mit den entsprechenden Beispielen zur Verfügung.
Beispiel 1
Angesichts des Atomradius von Wasserstoff -37 pm (1 Pikometer = 10-12m) - und Cäsium -265 pm- berechnen ihre Atomvolumina.
Mit der Kugelvolumenformel haben wir dann:
V.H.= (4/3) (3,14) (37 Uhr)3= 212,07 Uhr3
V.Cs= (4/3) (3,14) (265 Uhr)3= 77912297.67 Uhr3
Diese in Pikometern ausgedrückten Volumina sind jedoch exorbitant, so dass sie in Einheiten von Angström umgewandelt werden und mit dem Umrechnungsfaktor (1 Å / 100 pm) multipliziert werden.3::
(212.07 Uhr3) (1 Å / 100 pm)3= 2,1207 × 10-4 ZU3
(77912297.67 Uhr3) (1 Å / 100 pm)3= 77,912 Å3
Somit sind die Größenunterschiede zwischen dem kleinen H-Atom und dem sperrigen Cs-Atom numerisch belegt. Es muss bedacht werden, dass diese Berechnungen nur Annäherungen unter der Aussage sind, dass ein Atom vollständig kugelförmig ist und vor der Realität wandert.
Beispiel 2

Die Dichte von reinem Gold beträgt 19,32 g / ml und seine Molmasse beträgt 196,97 g / mol. Unter Anwendung der M / D-Formel zur Berechnung des Volumens eines Mols Goldatome wird Folgendes erhalten:
V.Au= (196,97 g / mol) / (19,32 g / ml) = 10,19 ml / mol
Das heißt, 1 Mol Goldatome nimmt 10,19 ml ein, aber welches Volumen nimmt ein Goldatom speziell ein? Und wie man es in Einheiten von pm ausdrückt3? Wenden Sie dazu einfach die folgenden Umrechnungsfaktoren an:
(10,19 ml / mol) · (mol / 6,02 · 10-2. 3 Atome) · (1 m / 100 cm)3(13 Uhr / 10 Uhr-12m)3= 16,92 · 106 p.m3
Andererseits beträgt der Atomradius von Gold 166 pm. Wenn beide Volumina verglichen werden - das nach der vorherigen Methode erhaltene und das mit der Kugelvolumenformel berechnete -, wird festgestellt, dass sie nicht den gleichen Wert haben:
V.Au= (4/3) (3,14) (166 Uhr)3= 19,15 · 106 p.m3
Welcher der beiden Werte kommt dem akzeptierten Wert am nächsten? Diejenige, die den experimentellen Ergebnissen am nächsten kommt, die durch Röntgenbeugung der Kristallstruktur von Gold erhalten wurden.
Verweise
- Helmenstine, Anne Marie, Ph.D. (9. Dezember 2017). Atomvolumendefinition. Abgerufen am 6. Juni 2018 von :oughtco.com
- Mayfair, Andrew. (13. März 2018). So berechnen Sie das Volumen eines Atoms. Wissenschaft. Abgerufen am 6. Juni 2018 von: sciencing.com
- Wiki Kids Ltd. (2018). Lothar Meyer Atomvolumenkurven. Abgerufen am 6. Juni 2018 von: wunderwhizkids.com
- Lumen. Periodische Trends: Atomradius. Abgerufen am 6. Juni 2018 von: course.lumenlearning.com
- Camilo J. Derpich. Atomvolumen und -dichte. Abgerufen am 6. Juni 2018 von: es-puraquimica.weebly.com
- Whitten, Davis, Peck & Stanley. Chemie. (8. Aufl.). CENGAGE Learning, S. 222-224.
- CK-12-Stiftung. (22. Februar 2010). Vergleichende Atomgrößen. [Zahl]. Abgerufen am 6. Juni 2018 von: commons.wikimedia.org
- CK-12-Stiftung. Ausgabe (22. Februar 2010). Atomradius von H.zwei. [Zahl]. Abgerufen am 6. Juni 2018 von: commons.wikimedia.org


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.