
Was ist Verflüchtigung?

Das Verflüchtigung ist der Prozess der Umwandlung einer chemischen Substanz von einem flüssigen oder festen Zustand in einen gasförmigen oder dampfförmigen Zustand. Andere Begriffe, die zur Beschreibung des gleichen Prozesses verwendet werden, sind Verdampfung, Destillation und Sublimation..
Eine Substanz kann oft durch Verflüchtigung von einer anderen getrennt und dann durch Dampfkondensation zurückgewonnen werden..

Die Substanz kann schneller verflüchtigt werden, indem sie entweder erhitzt wird, um ihren Dampfdruck zu erhöhen, oder indem der Dampf unter Verwendung eines Inertgasstroms oder einer Vakuumpumpe entfernt wird..
Zu den Erhitzungsverfahren gehört die Verflüchtigung von Wasser, Quecksilber oder Arsentrichlorid, um diese Substanzen von störenden Elementen zu trennen..
Chemische Reaktionen werden manchmal verwendet, um flüchtige Produkte wie bei der Freisetzung von Kohlendioxid aus Carbonaten, Ammoniak bei der Kjeldahl-Methode zur Bestimmung von Stickstoff und Schwefeldioxid bei der Bestimmung von Schwefel in Stahl herzustellen.
Die Verflüchtigungsverfahren zeichnen sich im Allgemeinen durch große Einfachheit und einfache Bedienung aus, außer wenn hohe Temperaturen oder Materialien mit hoher Korrosionsbeständigkeit erforderlich sind (Louis Gordon, 2014)..
Dampfdruckverflüchtigung
Haben Sie sich jemals gefragt, warum Regenwasser verdunstet, wenn Sie wissen, dass die Siedetemperatur von Wasser 100 ° C beträgt??
Ist es 100 ° C? Wenn ja, warum werde ich nicht warm? Haben Sie sich jemals gefragt, was Alkohol, Essig, Holz oder Kunststoff das charakteristische Aroma verleiht? (Dampfdruck, S.F.)
Verantwortlich für all dies ist eine Eigenschaft, die als Dampfdruck bekannt ist. Dies ist der Druck, den ein Dampf im Gleichgewicht mit der festen oder flüssigen Phase derselben Substanz ausübt..
Auch der Partialdruck der Substanz in der Atmosphäre auf den Feststoff oder die Flüssigkeit (Anne Marie Helmenstine, 2014).
Der Dampfdruck ist ein Maß für die Tendenz eines Materials, in den gasförmigen oder Dampfzustand überzugehen, dh ein Maß für die Flüchtigkeit von Substanzen.
Je höher der Dampfdruck ist, desto größer ist die Fähigkeit der Flüssigkeit oder des Feststoffs, zu verdampfen, wodurch die Flüchtigkeit erhöht wird..
Der Dampfdruck steigt mit der Temperatur. Die Temperatur, bei der der Dampfdruck auf die Oberfläche einer Flüssigkeit dem von der Umgebung ausgeübten Druck entspricht, wird als Siedepunkt der Flüssigkeit bezeichnet (Encyclopædia Britannica, 2017)..
Der Dampfdruck hängt von dem in Lösung gelösten gelösten Stoff ab (es handelt sich um eine kolligative Eigenschaft). Auf der Oberfläche der Lösung (Luft-Gas-Grenzfläche) neigen die oberflächlichsten Moleküle dazu, zu verdampfen, sich zwischen den Phasen auszutauschen und einen Dampfdruck zu erzeugen..
Das Vorhandensein eines gelösten Stoffes verringert die Anzahl der Lösungsmittelmoleküle an der Grenzfläche, wodurch der Dampfdruck verringert wird..
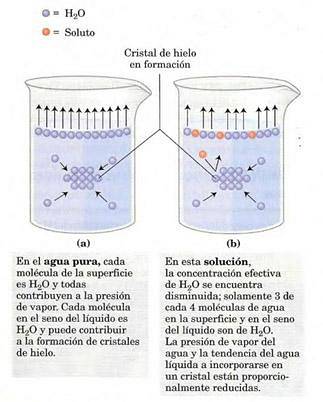
Die Änderung des Dampfdrucks kann mit dem Raoultschen Gesetz für nichtflüchtige gelöste Stoffe berechnet werden, das gegeben ist durch:
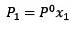
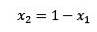
Wobei X2 der Molenbruch des Lösungsmittels ist. Wenn wir beide Seiten der Gleichung mit P ° multiplizieren, bleibt es:
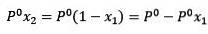
Das Einsetzen von (1) in (3) ist:
(4)
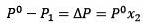
Dies ist die Änderung des Dampfdrucks, wenn sich ein gelöster Stoff auflöst (Jim Clark, 2017)..
Gravimetrische Analyse
Die gravimetrische Analyse ist eine Klasse von Labortechniken, mit denen die Masse oder Konzentration eines Stoffes durch Messung einer Massenänderung bestimmt wird..
Die Chemikalie, die wir zu quantifizieren versuchen, wird manchmal als Analyt bezeichnet. Wir könnten die gravimetrische Analyse verwenden, um Fragen zu beantworten wie:
- Wie hoch ist die Konzentration des Analyten in einer Lösung??
- Wie rein ist unsere Probe? Die Probe könnte hier fest oder in Lösung sein.
Es gibt zwei gebräuchliche Arten der gravimetrischen Analyse. Bei beiden wird die Phase des Analyten geändert, um ihn vom Rest eines Gemisches zu trennen, was zu einer Änderung der Masse führt..
Eine dieser Methoden ist die Niederschlagsgravimetrie, aber die, an der wir wirklich interessiert sind, ist die Verflüchtigungsgravimetrie.
Die Verflüchtigungsgravimetrie basiert auf der thermischen oder chemischen Zersetzung der Probe und der Messung der resultierenden Änderung ihrer Masse..
Alternativ können wir ein flüchtiges Zersetzungsprodukt fangen und wiegen. Da die Freisetzung einer flüchtigen Spezies ein wesentlicher Bestandteil dieser Methoden ist, klassifizieren wir sie gemeinsam als gravimetrische Verflüchtigungsanalysemethoden (Harvey, 2016)..
Gravimetrische Analyseprobleme sind einfach stöchiometrische Probleme mit wenigen zusätzlichen Schritten.
Um eine stöchiometrische Berechnung durchzuführen, benötigen wir die Koeffizienten der ausgeglichenen chemischen Gleichung.
Zum Beispiel, wenn eine Probe Bariumchloriddihydrat (BaCl) enthältzwei● H.zweiO) kann die Menge an Verunreinigungen erhalten werden, indem die Probe erhitzt wird, um das Wasser zu verdampfen.
Der Massendifferenz zwischen der Originalprobe und der erhitzten Probe ergibt in Gramm die im Bariumchlorid enthaltene Wassermenge.
Mit einer einfachen stöchiometrischen Berechnung wird die Menge an Verunreinigungen in der Probe erhalten (Khan, 2009)..
Fraktionierte Destillation
Die fraktionierte Destillation ist ein Prozess, bei dem die Komponenten eines flüssigen Gemisches gemäß ihren unterschiedlichen Siedepunkten in verschiedene Teile (sogenannte Fraktionen) getrennt werden.
Der Unterschied in der Flüchtigkeit der Verbindungen in der Mischung spielt eine grundlegende Rolle bei ihrer Trennung..
Die fraktionierte Destillation wird verwendet, um Chemikalien zu reinigen und auch Gemische zu trennen, um ihre Komponenten zu erhalten. Es wird als Labortechnik und in der Industrie eingesetzt, wo das Verfahren von großer wirtschaftlicher Bedeutung ist.
Dämpfe aus einer kochenden Lösung werden durch eine hohe Säule geleitet, die als Fraktionierungssäule bezeichnet wird..
Die Säule ist mit Kunststoff- oder Glasperlen gefüllt, um die Trennung zu verbessern, indem mehr Oberfläche für Kondensation und Verdampfung bereitgestellt wird.
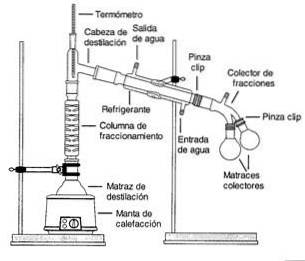
Die Temperatur der Säule nimmt entlang ihrer Länge allmählich ab. Komponenten mit höherem Siedepunkt kondensieren in der Säule und kehren zur Lösung zurück.
Komponenten mit niedrigeren Siedepunkten (flüchtiger) passieren die Säule und werden oben gesammelt.
Theoretisch verbessert das Vorhandensein von mehr Perlen oder Platten die Trennung, aber das Hinzufügen von Platten erhöht auch die Zeit und Energie, die erforderlich sind, um eine Destillation abzuschließen (Helmenstine, 2016)..
Verweise
- Anne Marie Helmenstine. (2014, 16. Mai). Dampfdruckdefinition. Von gedankenco.com wiederhergestellt.
- Encyclopædia Britannica. (2017, 10. Februar). Dampfdruck. Von britannica.com wiederhergestellt.
- Harvey, D. (2016, 25. März). Verflüchtigungsgravimetrie. Aus chem.libretexts wiederhergestellt.
- Helmenstine, A. M. (2016, 8. November). Definition und Beispiele der fraktionierten Destillation. Von gedankenco.com wiederhergestellt.
- Jim Clark, I. L. (2017, 3. März). Raoults Gesetz. Aus chem.libretexts wiederhergestellt.
- Khan, S. (2009, 27. August). Einführung in die gravimetrische Analyse: Verflüchtigungsgravimetrie. Von der Khanacademy erholt.
- Louis Gordon, R. W. (2014). Von accessscience.com wiederhergestellt.
- Dampfdruck. (S.F.). Von chem.purdue.edu wiederhergestellt.



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.