
Struktur und Funktion der Trockenzellen
EIN Trockenbatterie Es ist eine Batterie, deren Elektrolytmedium aus einer Paste und nicht aus einer Lösung besteht. Diese Paste hat jedoch eine bestimmte Luftfeuchtigkeit und ist aus diesen Gründen nicht streng trocken..
Die geringe Wassermenge reicht aus, damit sich die Ionen bewegen und folglich die Elektronen in der Zelle fließen..

Sein enormer Vorteil gegenüber den ersten nassen Batterien besteht darin, dass ihr Inhalt nicht verschüttet werden kann, da es sich um eine Elektrolytpaste handelt. Dies war der Fall bei nassen Batterien, die gefährlicher und empfindlicher waren als ihre trockenen Gegenstücke. Angesichts der Unmöglichkeit von Verschüttungen findet die Trockenzelle Verwendung in vielen tragbaren und mobilen Geräten.
Im Bild oben befindet sich eine trockene Zink-Kohlenstoff-Batterie. Genauer gesagt handelt es sich um eine moderne Version des Georges Leclanché-Stapels. Von allen ist es das häufigste und vielleicht das einfachste.
Diese Geräte stellen eine energetische Annehmlichkeit dar, da sie chemische Energie in der Tasche haben, die in Elektrizität umgewandelt werden kann. und auf diese Weise nicht abhängig von Steckdosen oder der Energie, die von großen Kraftwerken und ihrem riesigen Netzwerk von Türmen und Kabeln geliefert wird.
Artikelverzeichnis
- 1 Struktur der Trockenzelle
- 1.1 Elektroden
- 1.2 Terminals
- 1.3 Sand und Wachs
- 2 Bedienung
- 2.1 Oxidation der Zinkelektrode
- 2.2 Reduktion von Ammoniumchlorid
- 2.3 Herunterladen
- 3 Referenzen
Trockenzellstruktur
Wie ist eine Trockenzelle aufgebaut? Auf dem Bild sehen Sie die Abdeckung, die nichts weiter als eine Polymerfolie, Stahl und die beiden Anschlüsse ist, deren Isolierscheiben von vorne herausragen.
Dies ist jedoch nur seine äußere Erscheinung; Die wichtigsten Teile liegen im Inneren, was das ordnungsgemäße Funktionieren garantiert.
Jede Trockenzelle hat ihre eigenen Eigenschaften, es wird jedoch nur die Zink-Kohlenstoff-Zelle berücksichtigt, von der eine allgemeine Struktur für alle anderen Batterien skizziert werden kann..
Unter Batterie wird die Vereinigung von zwei oder mehr Batterien verstanden, und letztere sind Voltaikzellen, wie in einem zukünftigen Abschnitt erläutert wird..
Elektroden
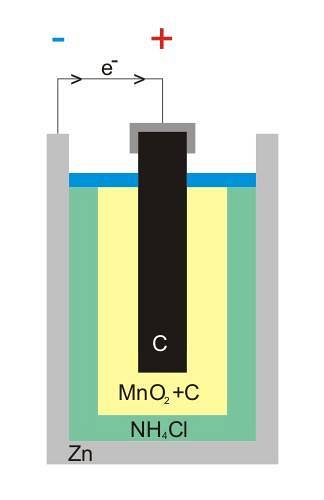
Das obere Bild zeigt die innere Struktur einer Zink-Kohlenstoff-Batterie. Egal was die Voltaikzelle ist, es sollten (normalerweise) immer zwei Elektroden vorhanden sein: eine, von der Elektronen abgegeben werden, und eine andere, die sie empfängt..
Elektroden sind elektrisch leitende Materialien, und damit Strom vorhanden ist, müssen beide unterschiedliche Elektronegativitäten aufweisen.
Zum Beispiel ist Zink, ein weißes Zinn, das die Batterie umschließt, der Ort, an dem die Elektronen zum Stromkreis (Gerät) gelangen, an dem sie angeschlossen sind.
Andererseits ist im gesamten Medium die graphitische Kohlenstoffelektrode; auch in eine Paste aus NH eingetaucht4Cl, ZnClzwei und MnOzwei.
Diese Elektrode empfängt die Elektronen und hat das Symbol '+', was bedeutet, dass es sich um den Pluspol der Batterie handelt.
Terminals
Wie über dem Graphitstab im Bild zu sehen ist, befindet sich der positive elektrische Anschluss; und darunter die innere Zinkdose, aus der Elektronen fließen, der negative Anschluss.
Aus diesem Grund haben die Batterien die Markierungen '+' oder '-', um anzuzeigen, wie sie richtig an das Gerät angeschlossen und somit eingeschaltet werden können..
Sand und Wachs
Obwohl nicht gezeigt, ist die Paste durch einen Puffersand und eine Wachssiegelung geschützt, die verhindert, dass sie unter geringfügigen mechanischen Stößen oder Bewegung verschüttet wird oder mit dem Stahl in Kontakt kommt..
Funktion
Wie funktioniert eine Trockenzelle? Zunächst handelt es sich um eine Voltaikzelle, dh sie erzeugt Elektrizität aus chemischen Reaktionen. Daher treten innerhalb von Zellen Redoxreaktionen auf, bei denen die Spezies Elektronen gewinnen oder verlieren..
Die Elektroden dienen als Oberfläche, die die Entwicklung dieser Reaktionen erleichtert und ermöglicht. Abhängig von ihren Ladungen kann es zu einer Oxidation oder Reduktion der Spezies kommen.
Um dies besser zu verstehen, werden nur die chemischen Aspekte der Zink-Kohlenstoff-Batterie erläutert..
Oxidation der Zinkelektrode
Sobald das elektronische Gerät eingeschaltet ist, setzt die Batterie durch Oxidation der Zinkelektrode Elektronen frei. Dies kann durch die folgende chemische Gleichung dargestellt werden:
Zn => Znzwei+ + 2e--
Wenn es viel Zn gibtzwei+ Um das Metall herum tritt eine positive Ladungspolarisation auf, so dass keine weitere Oxidation stattfindet. Daher ist das Znzwei+ muss durch die Paste in Richtung der Kathode diffundieren, wo die Elektronen zurücktreten.
Sobald die Elektronen das Artefakt aktiviert haben, kehren sie zur anderen Elektrode zurück: der Graphitelektrode, um einige chemische Spezies zu finden, die darauf "warten"..
Ammoniumchloridreduktion
Wie bereits erwähnt, ist NH in Nudeln enthalten4Cl und MnOzwei, Substanzen, die den pH-Wert sauer machen. Sobald die Elektronen eintreten, treten folgende Reaktionen auf:
2NH4+ + 2e- => 2NH3 + H.zwei
Die beiden Produkte Ammoniak und molekularer Wasserstoff, NH3 und H.zwei, Sie sind Gase und können daher die Batterie "anschwellen", wenn sie keine anderen Umwandlungen erfahren. wie die folgenden zwei:
Znzwei+ + 4NH3 => [Zn (NH3)4]]zwei+
H.zwei + 2MnOzwei => 2 MnO (OH)
Es ist zu beachten, dass das Ammonium reduziert wurde (gewonnene Elektronen), um NH zu werden3. Diese Gase wurden dann durch die anderen Komponenten der Paste neutralisiert..
Der Komplex [Zn (NH3)4]]zwei+ erleichtert die Diffusion von Zn-Ionenzwei+ in Richtung der Kathode und verhindern so, dass die Batterie „blockiert“.
Der externe Schaltkreis des Artefakts fungiert als Brücke für die Elektronen; Andernfalls würde es niemals eine direkte Verbindung zwischen der Zinkdose und der Graphitelektrode geben. Im Bild der Struktur würde diese Schaltung das schwarze Kabel darstellen.
Herunterladen
Trockenzellen gibt es in vielen Varianten, Größen und Arbeitsspannungen. Einige von ihnen sind nicht wiederaufladbar (primäre Voltaizellen), während andere (sekundäre Voltaizellen) sind..
Die Zink-Kohle-Batterie hat eine Arbeitsspannung von 1,5V. Ihre Formen ändern sich aufgrund ihrer Elektroden und der Zusammensetzung ihrer Elektrolyte..
Es wird einen Punkt geben, an dem der gesamte Elektrolyt reagiert hat, und egal wie stark das Zink oxidiert wird, es wird keine Spezies geben, die die Elektronen aufnehmen und ihre Freisetzung fördern..
Außerdem kann es vorkommen, dass die gebildeten Gase nicht mehr neutralisiert werden und weiterhin Druck in den Batterien ausüben..
Zink-Kohlenstoff-Batterien und andere Batterien, die nicht wiederaufladbar sind, müssen recycelt werden. da seine Bestandteile, insbesondere Nickel-Cadmium-Bestandteile, durch Verschmutzung von Böden und Gewässern umweltschädlich sind.
Verweise
- Shiver & Atkins. (2008). Anorganische Chemie. (Vierte Edition). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Chemie. (8. Aufl.). CENGAGE Lernen.
- Die "Trockenbatterie". Wiederhergestellt von: makahiki.kcc.hawaii.edu
- Hoffman S. (10. Dezember 2014). Was ist eine Trockenbatterie? Wiederhergestellt von: upsbatterycenter.com
- Gras, Geoffrey. (24. April 2017). Wie funktionieren Trockenbatterien? Wissenschaft. Wiederhergestellt von: sciencing.com
- Woodford, Chris. (2016) Batterien. Wiederhergestellt von: EXPLAINTHATSTAP.com.



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.