
Eigenschaften, Nomenklatur, Reaktionen, Typen aliphatischer Kohlenwasserstoffe
Das Aliphatische Kohlenwasserstoffe sind alle diejenigen, denen es an Aromatizität mangelt, nicht im olfaktorischen Sinne, sondern im Hinblick auf die chemische Stabilität. Die Klassifizierung von Kohlenwasserstoffen auf diese Weise ist heutzutage zu zweideutig und ungenau, da nicht zwischen verschiedenen Arten von Kohlenwasserstoffen unterschieden wird, die nicht aromatisch sind..
Wir haben also aliphatische Kohlenwasserstoffe und aromatische Kohlenwasserstoffe. Letztere sind an ihrer Grundeinheit zu erkennen: dem Benzolring. Die anderen können andererseits jede molekulare Struktur annehmen: linear, verzweigt, cyclisch, ungesättigt, polycyclisch; solange sie keine konjugierten Systeme wie Benzol haben.

Der Begriff "aliphatisch" wurde aus dem griechischen Wort "Aleiphar" geboren, was Fett bedeutet und auch für Öle verwendet wird. Daher wurde diese Klassifizierung im 19. Jahrhundert Kohlenwasserstoffen zugeordnet, die aus öligen Extrakten gewonnen wurden; während aromatische Kohlenwasserstoffe aus Baumharzen extrahiert und duftend wurden.
Als jedoch die Grundlagen der organischen Chemie konsolidiert wurden, wurde festgestellt, dass es eine chemische Eigenschaft gab, die Kohlenwasserstoffe differenzierte, die noch wichtiger als ihre natürlichen Quellen waren: Aromatizität (und nicht Duft).
Auf diese Weise waren aliphatische Kohlenwasserstoffe nicht mehr nur solche, die aus Fetten gewonnen wurden, sondern alle solche, denen es an Aromatizität mangelte. Innerhalb dieser Familie gibt es Alkane, Alkene und Alkine, unabhängig davon, ob sie linear oder cyclisch sind. Deshalb wird "aliphatisch" als ungenau angesehen; obwohl es nützlich ist, einige allgemeine Aspekte anzusprechen.
Wenn Sie beispielsweise aliphatische "Enden" oder "Ketten" sagen, beziehen Sie sich auf molekulare Regionen, in denen keine aromatischen Ringe vorhanden sind. Von allen aliphatischen Kohlenwasserstoffen ist Methan, CH, per Definition der einfachste4;; während Benzol der einfachste der aromatischen Kohlenwasserstoffe ist.
Artikelverzeichnis
- 1 Eigenschaften aliphatischer Kohlenwasserstoffe
- 2 Nomenklatur
- 3 Reaktionen
- 3.1 Verbrennung
- 3.2 Ergänzung
- 3.3 Halogenierung
- 3.4 Knacken
- 4 Typen
- 5 Verwendungen
- 6 Beispiele
- 7 Referenzen
Eigenschaften aliphatischer Kohlenwasserstoffe
Die Eigenschaften aliphatischer Kohlenwasserstoffe variieren in unterschiedlichem Maße, je nachdem, welche berücksichtigt werden. Es gibt solche mit niedriger und hoher Molekularmasse sowie lineare, verzweigte, zyklische oder polyzyklische, selbst solche mit erstaunlichen dreidimensionalen Strukturen; wie beim Kubaner würfelförmig.
Es gibt jedoch einige Allgemeingültigkeiten, die erwähnt werden können. Die meisten aliphatischen Kohlenwasserstoffe sind hydrophobe und unpolare Gase oder Flüssigkeiten, von denen einige unpolarer sind als andere, da auch solche enthalten sind, deren Kohlenstoffketten Halogen-, Sauerstoff-, Stickstoff- oder Schwefelatome enthalten..
Ebenso sind sie brennbare Verbindungen, da sie in der Luft mit minimaler Wärmequelle oxidationsanfällig sind. Diese Eigenschaft wird gefährlicher, wenn wir ihre hohe Flüchtigkeit aufgrund der schwachen dispersiven Wechselwirkungen hinzufügen, die aliphatische Moleküle zusammenhalten..
Wir sehen dies zum Beispiel in Butan, einem Gas, das sich wie Propan relativ leicht verflüssigen kann. Beide sind leicht flüchtig und brennbar, was sie zu aktiven Bestandteilen in Kochgas oder Taschenfeuerzeugen macht..
Natürlich neigt diese Flüchtigkeit dazu, mit zunehmender Molekülmasse abzunehmen und der Kohlenwasserstoff erzeugt zunehmend viskose und ölige Flüssigkeiten..
Nomenklatur
Die Nomenklatur der Kohlenwasserstoffe unterscheidet sich noch mehr als ihre Eigenschaften. Wenn es sich um Alkane, Alkene oder Alkine handelt, gelten dieselben von der IUPAC festgelegten Regeln: Wählen Sie die längste Kette aus und weisen Sie dem am meisten substituierten Ende oder den reaktivsten Heteroatomen oder Gruppen die niedrigsten Indikatorzahlen zu.
Auf diese Weise ist bekannt, auf welchem Kohlenstoff sich jeder Substituent befindet oder sogar die Ungesättigtheit (Doppel- oder Dreifachbindung). Bei cyclischen Kohlenwasserstoffen stehen vor dem Namen die Substituenten in alphabetischer Reihenfolge, gefolgt vom Wort "Zyklus", wobei die Kohlenstoffzahlen gezählt werden, aus denen er besteht..
Betrachten Sie beispielsweise die folgenden zwei Cyclohexane:
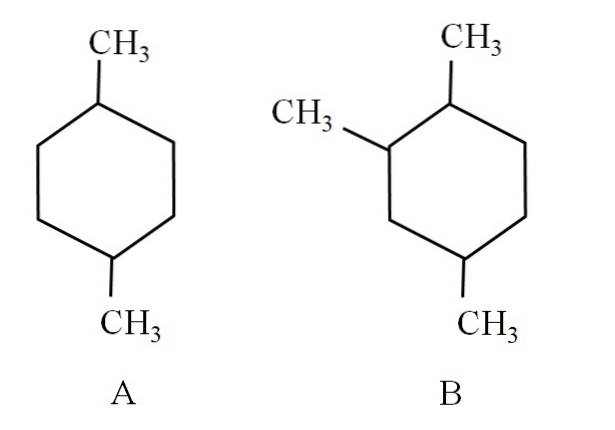
Cyclohexan A wird als 1,4-Dimethylcyclohexan bezeichnet. Wenn der Ring fünf Kohlenstoffe wäre, wäre es 1,4-Dimethylcyclopentan. In der Zwischenzeit wird Cyclohexan B als 1,2,4-Trimethylcyclohexan und nicht als 1,4,6-Cyclohexan bezeichnet, da versucht wird, die niedrigsten Indikatoren zu verwenden.
Jetzt kann die Nomenklatur für Kohlenwasserstoffe mit bizarren Strukturen sehr kompliziert werden. Für sie gibt es spezifischere Regeln, die separat und sorgfältig erklärt werden müssen; wie bei Dienen, Terpenen, Polyenen und polycyclischen Verbindungen.
Reaktionen
Verbrennung
Glücklicherweise sind die Reaktionen für diese Kohlenwasserstoffe weniger unterschiedlich. Eines davon wurde bereits erwähnt: Sie verbrennen leicht und produzieren je nach Vorhandensein von Heteroatomen (Cl, N, P, O usw.) Kohlendioxid und Wasser sowie andere Oxide oder Gase. Der COzwei und H.zweiOder sind sie die Hauptprodukte der Verbrennung.
Zusatz
Wenn sie Ungesättigtheiten aufweisen, können sie Additionsreaktionen eingehen; Das heißt, sie bauen kleine Moleküle als Substituenten nach einem bestimmten Mechanismus in ihr Rückgrat ein. Unter diesen Molekülen befinden sich Wasser, Wasserstoff und Halogene (F.zwei, Clzwei, Brzwei und ichzwei).
Halogenierung
Andererseits aliphatische Kohlenwasserstoffe unter Einfall von ultravioletter Strahlung (hv) und Hitze kann C-H-Bindungen aufbrechen, um sie gegen C-X-Bindungen (C-F, C-Cl usw.) auszutauschen. Dies ist die Halogenierungsreaktion, die in sehr kurzkettigen Alkanen wie Methan oder Pentan beobachtet wird..
Knacken
Eine andere Reaktion, die aliphatische Kohlenwasserstoffe, insbesondere langkettige Alkane, eingehen können, ist das thermische Cracken. Es besteht aus der Zufuhr intensiver Wärme, so dass die Wärmeenergie die C-C-Bindungen aufbricht und so aus großen Molekülen kleine Moleküle gebildet werden, die auf dem Kraftstoffmarkt mehr geschätzt werden.
Die vier oben genannten Reaktionen sind die Hauptreaktionen, die ein aliphatischer Kohlenwasserstoff eingehen kann, wobei die Verbrennung die wichtigste von allen ist, da sie keine Verbindung diskriminiert. Alle werden in Gegenwart von Sauerstoff brennen, aber nicht alle werden Moleküle hinzufügen oder in kleine Moleküle zerfallen.
Typen
Aliphatische Kohlenwasserstoffe gruppieren eine endlose Anzahl von Verbindungen, die wiederum spezifischer klassifiziert werden und den Grad ihrer Ungesättigtheit sowie die Art ihrer Struktur angeben..
Je nachdem, wie ungesättigt sie sind, haben wir Alkane (gesättigt), Alkene und Alkine (ungesättigt).
Alkane zeichnen sich durch einfache C-C-Bindungen aus, während wir in Alkenen und Alkinen C = C- bzw. C≡C-Bindungen beobachten. Eine sehr allgemeine Art, sie zu visualisieren, besteht darin, sich die Kohlenstoffgerüste von Alkanen als zickzackförmige und gebogene Ketten vorzustellen, die für Alkene „Quadrate“ und für Alkine „gerade Linien“ sind.
Dies ist auf die Tatsache zurückzuführen, dass die Doppel- und Dreifachbindungen Energie und sterische Einschränkungen in ihren Rotationen aufweisen und ihre Strukturen "härten"..
Alkane, Alkene und Alkine können verzweigt, cyclisch oder polycyclisch sein. Aus diesem Grund werden Cycloalkane, Cycloalkene, Cycloalkine und Verbindungen wie Decalin (Bicyclostruktur), Adamantan (ähnlich einer Baseballkappe), Heptalen und Gonan unter anderem auch als aliphatische Kohlenwasserstoffe angesehen..
Andere Arten von Kohlenwasserstoffen entstehen aus Alkenen wie Dienen (mit zwei Doppelbindungen), Polyenen (mit vielen alternierenden Doppelbindungen) und Terpenen (Verbindungen, die von Isopren, einem Dien, abgeleitet sind)..
Anwendungen
Auch hier können die Verwendungen dieser Kohlenwasserstoffe variieren, je nachdem, welcher in Betracht gezogen wird. In den Abschnitten Eigenschaften und Reaktionen wurde jedoch klargestellt, dass sie alle brennen, um nicht nur gasförmige Moleküle, sondern auch Licht und Wärme freizusetzen. Sie sind also Energiespeicher, die als Brennstoffe oder Wärmequellen dienen können..
Deshalb werden sie als Teil der Zusammensetzung von Benzin, für Erdgas, in Bunsenbrennern und im Allgemeinen verwendet, um Brände auslösen zu können..
Eines der bemerkenswertesten Beispiele ist das von Acetylen, HC≡CH, dessen Verbrennung es ermöglicht, die Metallionen einer Probe in der Atomabsorptionsspektrometrie anzuregen, die in analytischen Tests durchgeführt wird. Das entstehende Feuer kann auch zum Schweißen verwendet werden.
Flüssige aliphatische Kohlenwasserstoffe wie Paraffin werden häufig als Extraktionslösungsmittel für Fette verwendet. Darüber hinaus kann seine Lösungsmittelwirkung verwendet werden, um Flecken, Emails, Farben zu entfernen oder einfach Lösungen einer bestimmten organischen Verbindung herzustellen.
Diejenigen mit der höchsten Molekülmasse, ob viskos oder fest, werden zur Herstellung von Harzen, Polymeren oder Arzneimitteln verwendet.
Der Begriff "aliphatisch" wird häufig verwendet, um sich auf jene Regionen in einem Makromolekül zu beziehen, denen die Aromatizität fehlt. Beispielsweise werden Asphaltene oberflächlich als aromatischer Kern mit aliphatischen Ketten beschrieben.
Beispiele
Zunächst wurde gesagt, Methan sei der einfachste der aliphatischen Kohlenwasserstoffe. Es folgt Propan, CH3CHzweiCH3, Butan, CH3CHzweiCHzweiCH3, Pentan, CH3CHzweiCHzweiCHzweiCH3, Oktan, Nonan, Dekan usw. mit immer längeren Alkanen.
Gleiches gilt für Ethylen, CHzwei= CHzwei, Propen, CH3CH = CHzwei, Buten, CH3CHzweiCH = CH3, und für den Rest der Alkine. Wenn es zwei Doppelbindungen gibt, sind sie Diene, und wenn es mehr als zwei gibt, Polyene. Ebenso können Doppel- und Dreifachbindungen im selben Gerüst vorhanden sein, was die strukturelle Komplexität erhöht..
Unter den Cycloalkanen können wir Cyclopropan, Cyclobutan, Cyclopentan, Cyclohexan, Cycloheptan, Cyclooctan sowie Cyclohexen und Cyclohexin erwähnen. Aus all diesen Kohlenwasserstoffen werden wiederum verzweigte Derivate erhalten, wobei sich die verfügbaren Beispiele noch mehr vervielfachen (wie 1,4-Dimethylcyclohexan)..
Von den repräsentativsten Terpenen haben wir Limonen, Menthol, Pinen, Vitamin A, Squalen usw. Polyethylen ist ein mit -CH-Einheiten gesättigtes Polymerzwei-CHzwei-, es ist also auch ein Beispiel für diese Kohlenwasserstoffe. Andere Beispiele wurden bereits in den vorhergehenden Abschnitten angeführt.
Verweise
- Morrison, R. T. und Boyd, R., N. (1987). Organische Chemie. 5. Auflage. Editorial Addison-Wesley Interamericana.
- Carey F. (2008). Organische Chemie. (Sechste Ausgabe). Mc Graw Hill.
- Graham Solomons T. W., Craig B. Fryhle. (2011). Organische Chemie. Amine. (10. Auflage). Wiley plus.
- Helmenstine, Anne Marie, Ph.D. (22. August 2019). Definition des aliphatischen Kohlenwasserstoffs. Wiederhergestellt von :oughtco.com
- Wikipedia. (2019). Aliphatische Verbindung. Wiederhergestellt von: en.wikipedia.org
- Chemie LibreTexts. (20. August 2019). Aliphatische Kohlenwasserstoffe. Wiederhergestellt von: chem.libretexts.org
- Elizabeth Wyman. (2019). Aliphatische Kohlenwasserstoffe: Definition & Eigenschaften. Studie. Wiederhergestellt von: study.com



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.