
Anaerobe Glykolyse-Reaktionen und Fermentationswege
Das anaerobe Glykolyse oder anaerob ist ein katabolischer Weg, der von vielen Zelltypen zum Abbau von Glucose in Abwesenheit von Sauerstoff verwendet wird. Das heißt, Glucose wird nicht vollständig zu Kohlendioxid und Wasser oxidiert, wie dies bei der aeroben Glykolyse der Fall ist, sondern es werden fermentative Produkte erzeugt..
Es wird als anaerobe Glykolyse bezeichnet, da es ohne die Anwesenheit von Sauerstoff stattfindet, der in anderen Fällen als endgültiger Elektronenakzeptor in der mitochondrialen Transportkette fungiert, in der große Mengen an Energie aus der Verarbeitung glykolytischer Produkte erzeugt werden.
Je nach Organismus führt ein Zustand der Anaerobiose oder die Abwesenheit von Sauerstoff zur Produktion von Milchsäure (z. B. Muskelzellen) oder Ethanol (Hefe) aus dem Pyruvat, das durch den Abbau von Glukose erzeugt wird.
Infolgedessen sinkt die Energieausbeute drastisch, da nur zwei Mol ATP für jedes Mol verarbeitete Glucose produziert werden, verglichen mit den 8 Mol, die während der aeroben Glykolyse erhalten werden können (nur in der glykolytischen Phase)..
Der Unterschied in der Anzahl der ATP-Moleküle hat mit der Reoxidation von NADH zu tun, das im Gegensatz zur aeroben Glykolyse, bei der für jedes NADH 3 ATP-Moleküle erhalten werden, kein zusätzliches ATP erzeugt.
Artikelverzeichnis
- 1 Reaktionen
- 2 Fermentationswege
- 2.1 Milchsäureproduktion
- 2.2 Ethanolproduktion
- 3 Aerobe Gärung
- 4 Glykolyse und Krebs
- 5 Referenzen
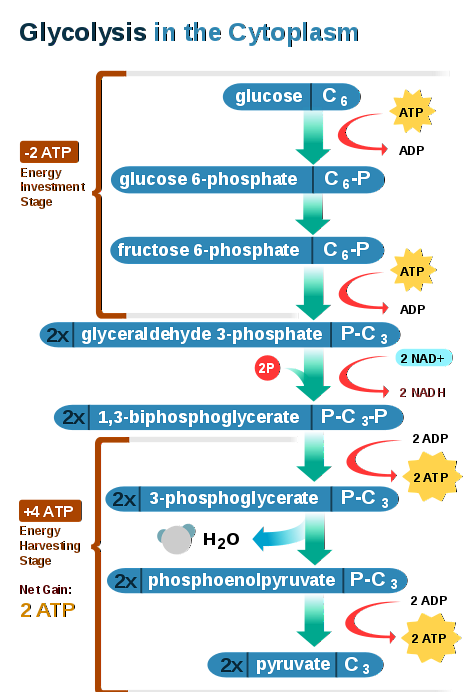
Reaktionen
Die anaerobe Glykolyse unterscheidet sich überhaupt nicht von der aeroben Glykolyse, da sich der Begriff „anaerob“ eher auf das bezieht, was nach dem glykolytischen Weg geschieht, dh auf das Schicksal der Reaktionsprodukte und Zwischenprodukte..
Somit sind zehn verschiedene Enzyme an anaeroben Glykolyse-Reaktionen beteiligt, nämlich:
1-Hexokinase (HK): Verwendet ein ATP-Molekül für jedes Glucosemolekül. Es produziert Glucose-6-phosphat (G6P) und ADP. Die Reaktion ist irreversibel und erfordert Magnesiumionen.
2-Phosphoglucose-Isomerase (PGI): Isomerisiert G6P zu Fructose-6-phosphat (F6P).
3-Phosphofructokinase (PFK): Phosphoryliert F6P zu Fructose-1,6-Bisphosphat (F1,6-BP) unter Verwendung eines ATP-Moleküls für jedes F6P. Diese Reaktion ist ebenfalls irreversibel.
4-Aldolase: spaltet das F1,6-BP-Molekül und produziert Glycerinaldehyd-3-phosphat (GAP) und Dihydroxyacetonphosphat (DHAP).
5-Triose-Phosphat-Isomerase (TIM): ist an der gegenseitigen Umwandlung von DHAP und GAP beteiligt.
6-Glycerinaldehyd-3-phosphat-Dehydrogenase (GAPDH): Verwendet zwei NAD-Moleküle+ und 2 Moleküle anorganisches Phosphat (Pi) zur Phosphorylierung von GAP ergeben 1,3-Bisphosphoglycerat (1,3-BPG) und 2 NADH.
7-Phosphoglyceratkinase (PGK): Produziert zwei ATP-Moleküle durch Phosphorylierung auf Substratebene von zwei ADP-Molekülen. Es verwendet als Phosphatgruppendonor jedes 1,3-BPG-Molekül. Produziert 2 Moleküle 3-Phosphoglycerat (3PG).
8-Phosphoglyceratmutase (PGM): ordnet das 3PG-Molekül neu an, um ein Zwischenprodukt mit höherer Energie, 2PG, zu erzeugen.
9-Enolase: Aus 2PG entsteht durch Dehydratisierung des ersten Phosphoenolpyruvats (PEP).
10-Pyruvatkinase (PYK): Phosphoenolpyruvat wird von diesem Enzym zur Bildung von Pyruvat verwendet. Die Reaktion beinhaltet die Übertragung der Phosphatgruppe an Position 2 von Phosphoenolpyruvat auf ein ADP-Molekül. Für jede Glucose werden 2 Pyruvate und 2 ATP produziert.
Fermentationswege
Fermentation ist der Begriff, der verwendet wird, um anzuzeigen, dass Glucose oder andere Nährstoffe in Abwesenheit von Sauerstoff abgebaut werden, um Energie zu erhalten.
In Abwesenheit von Sauerstoff hat die Elektronentransportkette keinen Endakzeptor und daher tritt keine oxidative Phosphorylierung auf, die große Energiemengen in Form von ATP ergibt. NADH wird nicht über den Mitochondrienweg reoxidiert, sondern über alternative Wege, die kein ATP produzieren.
Nicht genug NAD+ Der glykolytische Weg wird gestoppt, da die Übertragung von Phosphat auf GAP eine gleichzeitige Reduktion dieses Cofaktors erfordert.
Einige Zellen haben alternative Mechanismen, um mit Perioden der Anaerobiose fertig zu werden, und im Allgemeinen beinhalten diese Mechanismen eine Art von Fermentation. Andere Zellen hingegen sind für ihren Lebensunterhalt fast ausschließlich auf fermentative Prozesse angewiesen..
Die Produkte der Fermentationswege vieler Organismen sind für den Menschen wirtschaftlich relevant; Beispiele sind die Produktion von Ethanol durch einige anaerobe Hefen und die Bildung von Milchsäure durch die zur Herstellung von Joghurt verwendeten Lactobakterien..
Milchsäureproduktion
Viele Arten von Zellen produzieren in Abwesenheit von Sauerstoff Milchsäure dank der Reaktion, die durch den Lactatdehydrogenasekomplex katalysiert wird, der die Kohlenstoffe von Pyruvat und das in der GAPDH-Reaktion erzeugte NADH verwendet..
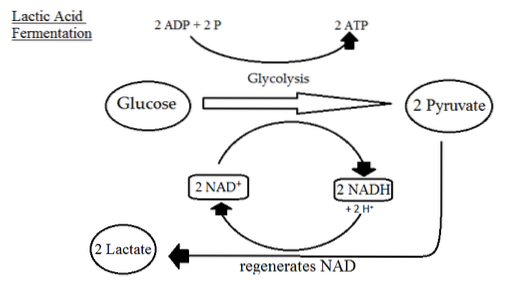
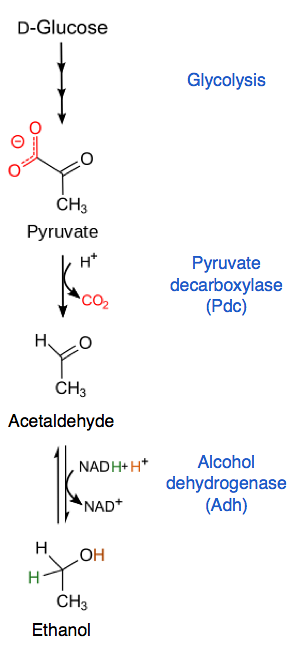
Ethanolproduktion
Pyruvat wird durch Pyruvatdecarboxylase in Acetaldehyd und CO2 umgewandelt. Acetaldehyd wird dann von Alkoholdehydrogenase verwendet, die es reduziert, Ethanol produziert und ein NAD-Molekül regeneriert.+ für jedes Pyruvatmolekül, das auf diese Weise eintritt.
Aerobe Gärung
Die anaerobe Glykolyse hat als Hauptmerkmal die Tatsache, dass die Endprodukte nicht CO entsprechenzwei und Wasser, wie im Fall der aeroben Glykolyse. Stattdessen werden typische Produkte von Fermentationsreaktionen erzeugt.
Einige Autoren haben einen Prozess der "aeroben Fermentation" oder aeroben Glykolyse von Glucose für bestimmte Organismen beschrieben, unter denen einige Parasiten der Trypanosomatidae-Familie und viele Krebstumorzellen hervorstechen..
In diesen Organismen wurde gezeigt, dass selbst in Gegenwart von Sauerstoff die Produkte des glykolytischen Weges Produkten von Fermentationswegen entsprechen, weshalb angenommen wird, dass eine „teilweise“ Oxidation von Glucose auftritt, da nicht die gesamte Energie vorhanden ist möglich von seinen Kohlenstoffen extrahiert.
Obwohl die "aerobe Fermentation" von Glucose nicht das völlige Fehlen von Atmungsaktivität impliziert, da es sich nicht um einen Alles-oder-Nichts-Prozess handelt. Die Literatur gibt jedoch die Ausscheidung von Produkten wie Pyruvat, Lactat, Succinat, Malat und anderen organischen Säuren an..
Glykolyse und Krebs
Viele Krebszellen zeigen eine Zunahme der Glukoseaufnahme und des glykolytischen Flusses.
Tumore bei Krebspatienten wachsen schnell, so dass die Blutgefäße hypoxisch sind. Daher hängt die Energieergänzung dieser Zellen hauptsächlich von der anaeroben Glykolyse ab..
Dieses Phänomen wird jedoch durch einen durch Hypoxie induzierbaren Transkriptionsfaktor (HIF) unterstützt, der die Expression von glykolytischen Enzymen und Glucosetransportern in der Membran durch komplexe Mechanismen erhöht..
Verweise
- Akram, M. (2013). Mini-Review zu Glykolyse und Krebs. J. Canc. Educ., 28, 454-457.
- Bustamante, E. & Pedersen, P. (1977). Hohe aerobe Glykolyse von Rattenhepatomzellen in Kultur: Rolle der mitochondrialen Hexokinase. Proc. Natl. Acad. Sci., 74(9), 3735 & ndash; 3739.
- Cazzulo, J. J. (1992). Aerobe Fermentation von Glucose durch Trypanosomatiden. Das FASEB-Journal, 6, 3153-3161.
- Jones, W. & Bianchi, K. (2015). Aerobe Glykolyse: jenseits der Proliferation. Grenzen in der Immunologie, 6, 1-5.
- Li, X., Gu, J. & Zhou, Q. (2015). Überprüfung der aeroben Glykolyse und ihrer Schlüsselenzyme - neue Ziele für die Lungenkrebstherapie. Brustkrebs, 6, 17-24.
- Maris, A.J.A. Van, Abbott, Æ. D. A., Bellissimi, Æ. E., Brink, J. Van Den, Kuyper, Æ. M., Luttik, Æ. M.A.H., Pronk, J.T. (2006). Alkoholische Fermentation von Kohlenstoffquellen in Biomassehydrolysaten durch Saccharomyces cerevisiae: aktueller Stand. Antonie van Leeuwenhoek, 90, 391-418.
- Nelson, D. L. & Cox, M. M. (2009). Lehninger Prinzipien der Biochemie. Omega-Ausgaben (5. Aufl.).


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.