
Phosphodiester binden, wie es gebildet wird, Funktion und Beispiele
Das Phosphodiesterbindungen sind die kovalenten Bindungen, die zwischen zwei der Sauerstoffatome einer Phosphatgruppe und den Hydroxylgruppen zweier anderer verschiedener Moleküle auftreten. Bei dieser Art der Bindung wirkt die Phosphatgruppe als stabile Bindungsbrücke zwischen den beiden Molekülen über ihre Sauerstoffatome..
Die grundlegende Rolle von Phosphodiesterbindungen in der Natur ist die Bildung von Nukleinsäureketten, sowohl DNA als auch RNA. Zusammen mit den Pentosezuckern (Desoxyribose bzw. Ribose) sind die Phosphatgruppen Teil der Stützstruktur dieser wichtigen Biomoleküle..
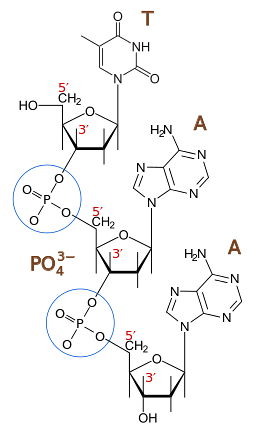
Die Nukleotidketten von DNA oder RNA können wie Proteine unterschiedliche dreidimensionale Konformationen annehmen, die durch nichtkovalente Bindungen wie Wasserstoffbrücken zwischen komplementären Basen stabilisiert werden..
Die Primärstruktur ist jedoch durch die lineare Sequenz von Nukleotiden gegeben, die über Phosphodiesterbindungen kovalent verbunden sind..
Artikelverzeichnis
- 1 Wie entsteht eine Phosphodiesterbindung??
- 1.1 Beteiligte Enzyme
- 2 Funktion und Beispiele
- 3 Referenzen
Wie entsteht eine Phosphodiesterbindung??
Wie Peptidbindungen in Proteinen und glykosidische Bindungen zwischen Monosacchariden resultieren Phosphodiesterbindungen aus Dehydratisierungsreaktionen, bei denen ein Wassermolekül verloren geht. Hier ist das allgemeine Schema einer dieser Dehydratisierungsreaktionen:
H-X1-OH + H-Xzwei-OH → H-X1-X.zwei-OH + H.zweiODER
Phosphationen entsprechen der vollständig deprotonierten konjugierten Base der Phosphorsäure und werden als anorganische Phosphate bezeichnet, die als Pi abgekürzt werden. Wenn zwei Phosphatgruppen miteinander verbunden sind, wird eine wasserfreie Phosphatbindung gebildet und ein Molekül erhalten, das als anorganisches Pyrophosphat oder PPi bekannt ist..
Wenn ein Phosphation an ein Kohlenstoffatom in einem organischen Molekül gebunden ist, wird die chemische Bindung als Phosphatester bezeichnet, und die resultierende Spezies ist ein organisches Monophosphat. Wenn das organische Molekül an mehr als eine Phosphatgruppe bindet, werden organische Diphosphate oder Triphosphate gebildet.
Wenn ein einzelnes anorganisches Phosphatmolekül an zwei organische Gruppen gebunden ist, wird eine Phosphodiester- oder "Phosphatdiester" -Bindung verwendet. Es ist wichtig, die Phosphodiesterbindungen nicht mit den hochenergetischen Phosphoanhydro-Bindungen zwischen den Phosphatgruppen von Molekülen wie beispielsweise ATP zu verwechseln..
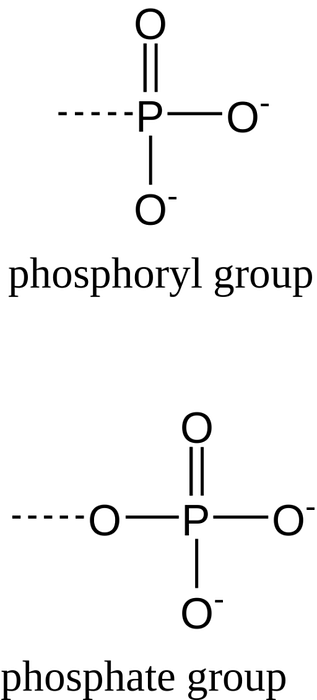
Phosphodiesterbindungen zwischen benachbarten Nukleotiden bestehen aus zwei Phosphoesterbindungen, die zwischen der Hydroxylgruppe an der 5'-Position eines Nukleotids und der Hydroxylgruppe an der 3'-Position des nächsten Nukleotids in einem DNA- oder RNA-Strang auftreten.
Abhängig von den Umgebungsbedingungen können diese Bindungen sowohl enzymatisch als auch nicht enzymatisch hydrolysiert werden..
Beteiligte Enzyme
Die Bildung und das Aufbrechen chemischer Bindungen ist für alle uns bekannten lebenswichtigen Prozesse von entscheidender Bedeutung, und der Fall von Phosphodiesterbindungen ist keine Ausnahme..
Zu den wichtigsten Enzymen, die diese Bindungen bilden können, gehören DNA- oder RNA-Polymerasen und Ribozyme. Phosphodiesteraseenzyme können sie enzymatisch hydrolysieren.
Während der Replikation, einem entscheidenden Prozess für die Zellproliferation, wird in jedem Reaktionszyklus ein zur Matrizenbase komplementäres dNTP (Desoxynukleotidtriphosphat) durch eine Nukleotidtransferreaktion in die DNA eingebaut..
Die Polymerase ist verantwortlich für die Bildung einer neuen Bindung zwischen dem 3'-OH des Matrizenstrangs und dem α-Phosphat des dNTP, dank der Energie, die durch das Aufbrechen der Bindungen zwischen den α- und β-Phosphaten des dNTP freigesetzt wird sind durch Phosphoanhydro-Bindungen verbunden.
Das Ergebnis ist die Verlängerung der Kette um ein Nukleotid und die Freisetzung eines Pyrophosphatmoleküls (PPi). Es wurde festgestellt, dass diese Reaktionen zwei zweiwertige Magnesiumionen (Mg) verdienenzwei+), deren Anwesenheit die elektrostatische Stabilisierung des nukleophilen OH ermöglicht- um die Annäherung an das aktive Zentrum des Enzyms zu erhalten.
Das pKzu einer Phosphodiesterbindung liegt nahe bei 0, so dass diese Bindungen in einer wässrigen Lösung vollständig ionisiert und negativ geladen sind.
Dies gibt Nukleinsäuremolekülen eine negative Ladung, die durch ionische Wechselwirkungen mit den positiven Ladungen von Proteinaminosäureresten, elektrostatische Bindung mit Metallionen oder Assoziation mit Polyaminen neutralisiert wird..
In einer wässrigen Lösung sind die Phosphodiesterbindungen in DNA-Molekülen viel stabiler als in RNA-Molekülen. In alkalischer Lösung werden diese Bindungen in RNA-Molekülen durch intramolekulare Verschiebung des Nukleosids am 5'-Ende durch ein 2'-Oxyanion gespalten.
Funktion und Beispiele
Wie bereits erwähnt, ist die wichtigste Rolle dieser Bindungen ihre Beteiligung an der Bildung des Rückgrats von Nukleinsäuremolekülen, die eines der wichtigsten Moleküle in der Zellwelt sind..
Die Aktivität von Topoisomeraseenzymen, die aktiv an der DNA-Replikation und Proteinsynthese beteiligt sind, hängt von der Wechselwirkung der Phosphodiesterbindungen am 5'-Ende der DNA mit der Seitenkette der Tyrosinreste im aktiven Zentrum dieser Enzyme ab.
Moleküle, die als Second Messenger beteiligt sind, wie cyclisches Adenosinmonophosphat (cAMP) oder cyclisches Guanosintriphosphat (cGTP), besitzen Phosphodiesterbindungen, die durch spezifische Enzyme hydrolysiert werden, die als Phosphodiesterasen bekannt sind und deren Beteiligung für viele mobile Signalprozesse von größter Bedeutung ist.
Glycerophospholipide, grundlegende Bestandteile in biologischen Membranen, bestehen aus einem Glycerinmolekül, das über Phosphodiesterbindungen an die polaren "Kopf" -Gruppen bindet, die die hydrophile Region des Moleküls bilden..
Verweise
- M. Fothergill, M. F. Goodman, J. Petruska & A. Warshel (1995). Struktur-Energie-Analyse der Rolle von Metallionen bei der Hydrolyse von Phosphodiesterbindungen durch DNA-Polymerase I.. Zeitschrift der American Chemical Society, 117(47), 11619 & ndash; 11677.
- H. Lodish, A. Berk, C. A. Kaiser, M. Krieger, A. Bretscher, H. Ploegh, K. Martin (2003). Molekulare Zellbiologie (5. Aufl.). Freeman, W. H. & Company.
- T. Nakamura, Y. Zhao, Y. Yamagata, Y. J. Hua & W. Yang (2012). Beobachten, wie die DNA-Polymerase η eine Phosphodiesterbindung eingeht. Natur, 487(7406), 196-201.
- Nelson, D. L. & Cox, M. M. (2009). Lehninger Prinzipien der Biochemie. Omega-Ausgaben (5. Aufl.)
- M. Oivanen, S. Kuusela & H. Lönnberg (1998). Kinetik und Mechanismen zur Spaltung und Isomerisierung der Phosphodiesterbindungen von RNA durch Brönsted-Säuren und -Basen. Chemische Bewertungen, 98(3), 961 & ndash; 990.
- Pradeepkumar, P. I., Höbartner, C., Baum, D. & Silverman, S. (2008). DNA-katalysierte Bildung von Nucleopeptidbindungen. Angewandte Chemie International Edition, 47(9), 1753 & ndash; 1757.
- Soderberg, T. (2010). Organische Chemie mit biologischem Schwerpunkt Band II (Band II). Minnesota: Universität von Minnesota Morris Digital Well. Abgerufen von www.digitalcommons.morris.umn.edu


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.