
Konzepte und Beispiele für die chemische Teilbarkeit

Wir können das definieren Teilbarkeit in der Chemie als eine Eigenschaft der Materie, die es ermöglicht, sie in kleinere Teile zu trennen. Um das Konzept zu verstehen, können wir ein Beispiel geben.
Wenn wir einen Laib Brot nehmen und ihn immer wieder halbieren, werden wir jemals zu einem grundlegenden Materieblock gelangen, der nicht weiter geteilt werden kann? Diese Frage beschäftigt Wissenschaftler und Philosophen seit Tausenden von Jahren.
Ursprung und Konzept der chemischen Teilbarkeit
Lange Zeit wurde diskutiert, ob Materie aus Teilchen besteht (was wir heute als Atome kennen). Die allgemeine Idee war jedoch, dass Materie ein Kontinuum ist, das geteilt werden kann.
Dieses weit verbreitete Konzept machte brillante Wissenschaftler wie James Clerk Maxwell (nach Maxwells Gleichungen) und Ludwing Boltzman (nach Boltzman-Verteilung) zum Opfer von Spott, der erstere zum Wahnsinn und letztere zum Selbstmord trieb..
Im 5. Jahrhundert v. Chr. Verwendeten der griechische Philosoph Leucippus und sein Schüler Demokrit das Wort Atome, um das kleinste einzelne Stück Materie zu bezeichnen, und schlugen vor, dass die Welt nur aus Atomen in Bewegung besteht..
Diese frühe Atomtheorie unterschied sich von späteren Versionen darin, dass sie die Idee einer menschlichen Seele enthielt, die aus einem verfeinerten Atomtyp besteht, der im ganzen Körper verteilt ist..
Die Atomtheorie verfiel im Mittelalter, wurde aber zu Beginn der wissenschaftlichen Revolution im 17. Jahrhundert wiederbelebt..
Isaac Newton glaubte beispielsweise, dass Materie aus "festen, massiven, harten, undurchdringlichen und beweglichen Teilchen" bestehe..
Die Teilbarkeit kann durch verschiedene Methoden erfolgen, am häufigsten ist die Teilbarkeit durch physikalische Methoden, beispielsweise das Hacken eines Apfels mit einem Messer.
Die Teilbarkeit kann jedoch auch durch chemische Verfahren erfolgen, bei denen Materie in Moleküle oder Atome getrennt wird.
10 Beispiele für chemische Teilbarkeit
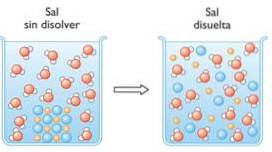
1- Salz in Wasser auflösen
Wenn ein Salz, beispielsweise Natriumchlorid, in Wasser gelöst wird, tritt ein Solvatationsphänomen auf, bei dem die Ionenbindungen des Salzes aufgebrochen werden:
NaCl → Na+ + Cl-
Durch das Auflösen nur eines Salzkorns in Wasser wird es in Milliarden von Natrium- und Chloridionen in Lösung getrennt..
2- Oxidation von Metallen in einem sauren Medium
Alle Metalle, beispielsweise Magnesium oder Zink, reagieren mit Säuren, beispielsweise verdünnter Salzsäure, zu Wasserstoffblasen und einer farblosen Lösung des Metallchlorids.
Mg + HCl → Mgzwei+ +Cl- + H.zwei
Die Säure oxidiert das Metall und trennt die Metallbindungen, um Ionen in Lösung zu erhalten (BBC, 2014)..
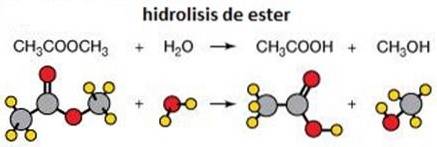
3- Hydrolyse von Estern
Hydrolyse ist das Aufbrechen einer chemischen Bindung durch Wasser. Ein Beispiel für die Hydrolyse ist die Hydrolyse von Estern, bei denen diese in zwei Moleküle unterteilt sind, einen Alkohol und eine Carbonsäure..
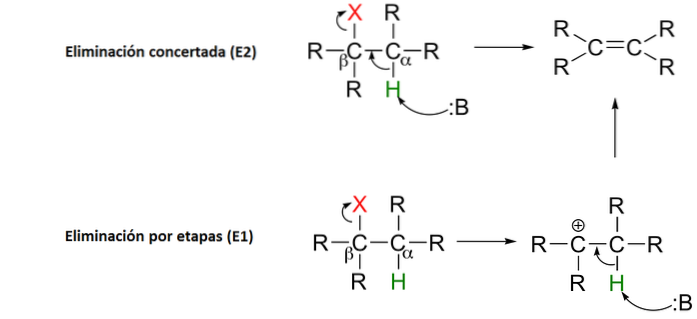
4- Eliminierungsreaktionen
Eine Eliminierungsreaktion macht genau das, was sie sagt: Sie entfernt Atome aus einem Molekül. Dies geschieht, um eine Kohlenstoff-Kohlenstoff-Doppelbindung zu erzeugen. Dies kann unter Verwendung einer Base oder einer Säure erfolgen.
Es kann in einem einzigen konzertierten Schritt (die Abstraktion des Protons an Cα erfolgt gleichzeitig mit der Spaltung der Cβ-X-Bindung) oder in zwei Schritten (die Spaltung der Cβ-X-Bindung erfolgt zuerst unter Bildung eines Zwischenprodukts) erfolgen Carbokation, die sich dann durch die Abstraktion des Protons im Alpha-Kohlenstoff "ausschaltet").
5- Enzymatische Reaktion von Aldolase
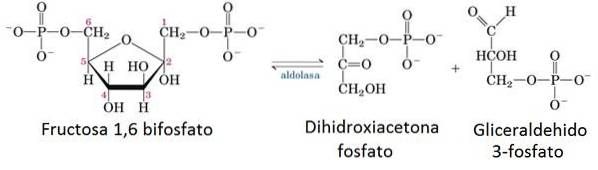
In der präparativen Phase der Glykolyse wird ein Glucosemolekül unter Verwendung von 2 ATP in zwei Moleküle Glycerinaldehyd-3-phosphat (G3P) aufgeteilt.
Das für diesen Einschnitt verantwortliche Enzym ist Aldolase, die durch umgekehrte Kondensation das Fructose-1,6-Bisphosphat-Molekül in einem G3P-Molekül und ein Dihydroxyacetonphosphat-Molekül, das später zu einem anderen G3P-Molekül isomerisiert wird, in zwei Teile teilt.
6- Abbau von Biomolekülen
Nicht nur die Glykolyse, sondern der gesamte Abbau von Biomolekülen bei Katabolismusreaktionen sind Beispiele für die chemische Teilbarkeit.
Dies liegt daran, dass sie von großen Molekülen wie Kohlenhydraten, Fettsäuren und Proteinen ausgehen, um kleinere Moleküle wie Acetyl-CoA zu produzieren, die in den Krebszyklus eintreten und Energie in Form von ATP produzieren.
7- Verbrennungsreaktionen
Dies ist ein weiteres Beispiel für die chemische Teilbarkeit, da komplexe Moleküle wie Propan oder Butan mit Sauerstoff unter Bildung von CO reagieren.zwei und Wasser:
C.3H.8 + 50zwei → 3COzwei + 4HzweiODER
Der Abbau von Biomolekülen könnte als Verbrennungsreaktion bezeichnet werden, da die Endprodukte CO sindzwei und Wasser, jedoch werden diese in vielen Schritten mit verschiedenen Vermittlern gegeben.
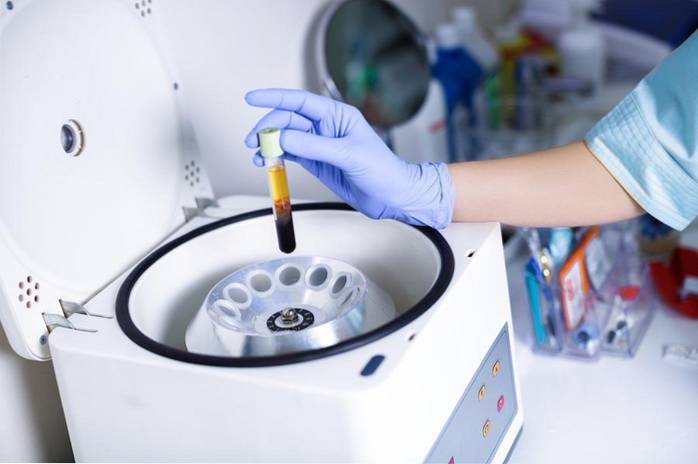
8- Zentrifugation von Blut
Die Trennung der verschiedenen Blutbestandteile ist ein Beispiel für die Teilbarkeit. Obwohl es sich um einen physikalischen Prozess handelt, erscheint mir das Beispiel interessant, da die Komponenten durch Dichteunterschiede durch Zentrifugation getrennt werden.
Die dichtesten Komponenten, das Serum mit den roten Blutkörperchen, verbleiben am Boden des Zentrifugenröhrchens, während die weniger dichten Komponenten, das Plasma, oben bleiben..
9- Bicarbonatpuffer
Natriumbicarbonat, HCO3- Es ist die Haupttransportart von COzwei im Körperprodukt von Stoffwechselabbaureaktionen.
Diese Verbindung reagiert mit einem Proton im Medium unter Bildung von Kohlensäure, die anschließend in CO2 und Wasser aufgeteilt wird:
HCO3- + H.+ D H.zweiCO3 D COzwei + H.zweiODER
Da die Reaktionen reversibel sind, kann der Organismus auf diese Weise durch Atmung den physiologischen pH-Wert steuern, um Alkalose- oder Azidoseprozesse zu vermeiden.
10- Teilung des Atoms oder der Kernspaltung
Falls ein massiver Kern (wie Uran-235) zerfällt (Spaltungen), führt dies zu einer Nettoenergieausbeute. Dies liegt daran, dass die Summe der Massen der Fragmente geringer ist als die Masse des Urankerns..
In dem Fall, dass die Masse der Fragmente am Peak der Bindungsenergiekurve gleich oder größer als die von Eisen ist, werden die Kernteilchen enger gebunden als im Urankern, und diese Abnahme der Masse tritt in Energieform entsprechend auf zu Einsteins Gleichung.
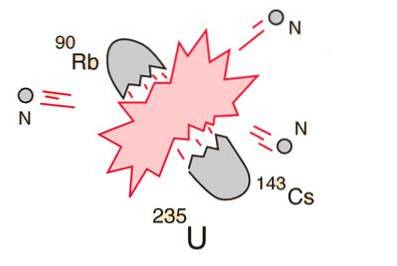
Bei Elementen, die leichter als Eisen sind, erzeugt die Fusion Energie. Dieses Konzept führte zur Schaffung der Atombombe und der Atomkraft..
Verweise
- AJ Software & Multimedia. (2015). Kernspaltung: Grundlagen. Von atomicarchive.com wiederhergestellt.
- (2014). Reaktionen von Säuren. Von bbc.co.uk wiederhergestellt.
- Clark, J. (2016, Januar). HYDROLYSIERENDE ESTER. Von chemguide.co.uk wiederhergestellt.
- Foist, L. (S.F.). Eliminierungsreaktionen in der organischen Chemie. Von study.com wiederhergestellt.
- Miller, W. A. (1867). Elemente der Chemie: Theoretisch und praktisch, Teil 1. New York: John Wiley und Sohn.
- Kernspaltung. (S.F.). Von der Hyperphysik erholt.
- Pratt, D. (1997, November). Die unendliche Teilbarkeit der Materie. Von davidpratt.info wiederhergestellt.
- Soderberg, T. (2016, 31. Mai). Eliminierung durch die E1- und E2-Mechanismen. Aus chem.libretext wiederhergestellt.



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.