
Struktur, Eigenschaften, Verwendungen, Risiken von Dimethylamin ((CH3) 2NH)

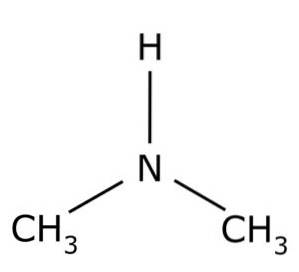
Das Dimethylamin ist eine organische Verbindung, die aus zwei Methylgruppen -CH gebildet wird3 an eine -NH-Gruppe gebunden. Seine chemische Formel lautet (CH3)zweiNH. Es ist ein farbloses Gas. Wenn es in geringen Konzentrationen in der Luft ist, wird ein fischartiger Geruch wahrgenommen. Wenn es jedoch in hoher Konzentration vorliegt, riecht es nach Ammoniak NH3.
Dimethylamin ist in Pflanzen und Tieren vorhanden. Es wird angenommen, dass es beim Menschen durch den Abbau bestimmter Enzyme, aber auch durch die Aufnahme einiger Lebensmittel wie Fisch entsteht. Wenn sich Dimethylamin-Gas in Wasser löst, bildet es stark alkalische und ätzende Lösungen.
Es hat verschiedene industrielle Anwendungen, wie zur Herstellung von Lösungsmitteln, zur Beschleunigung der Vulkanisation von Kautschuk, zur Verhinderung der Korrosion von Rohren, zur Herstellung von Seifen, zur Herstellung von Farbstoffen und zur Absorption von sauren Gasen in bestimmten Prozessen..
Dimethylamin ist ein leicht entzündliches Gas. Behälter dürfen weder Hitze noch Feuer ausgesetzt werden, da sie explodieren können. Darüber hinaus reizen seine Dämpfe die Augen, die Haut und die Atemwege..
Es ist eine Verbindung, die Teil von atmosphärischen Aerosolen sein kann, dh sehr feine Tröpfchen, die in der Atmosphäre gefunden werden.
Artikelverzeichnis
- 1 Struktur
- 2 Nomenklatur
- 3 Eigenschaften
- 3.1 Physikalischer Zustand
- 3.2 Molekulargewicht
- 3.3 Schmelzpunkt
- 3.4 Siedepunkt
- 3.5 Flammpunkt
- 3.6 Selbstentzündungstemperatur
- 3.7 Dichte
- 3.8 Löslichkeit
- 3,9 pH
- 3.10 Dissoziationskonstante
- 3.11 Chemische Eigenschaften
- 3.12 Andere Eigenschaften
- 3.13 Biochemische Reaktionen
- 4 Erhalten
- 5 Präsenz in der Natur
- 5.1 Patienten mit überschüssigem Dimethylamin
- 6 Verwendungen
- 7 Risiken
- 8 Einfluss von DMA auf die Atmosphäre
- 9 Referenzen
Struktur
Dimethylamin ist ein sekundäres aliphatisches Amin. Dies bedeutet, dass die Stickstoffsubstituenten (N) aliphatisch (-CH) sind3), was bedeutet, dass sie nicht aromatisch sind und dass sie zwei sind. Daher sind sie zwei Methyl-CH3 gebunden an Stickstoff, der auch einen Wasserstoff (H) hat.
Im Dimethylaminmolekül hat Stickstoff (N) ein Paar freier Elektronen, dh ein Elektronenpaar, das an kein anderes Atom gebunden ist..
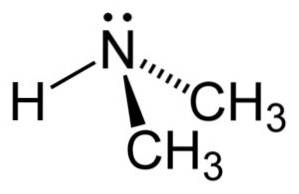
Nomenklatur
- Dimethylamin
- N, N-Dimethylamin
- N-Methylmethanamin
- DMA (Abkürzung für Di-Methyl-Amin).
Eigenschaften
Körperlicher Status
Farbloses Gas.
Molekulargewicht
45,08 g / mol
Schmelzpunkt
-93 ºC
Siedepunkt
7,3 ºC
Flammpunkt
-6,69 ºC (Methode mit geschlossenem Becher).
Selbstentzündungstemperatur
400 ° C.
Dichte
Flüssigkeit = 0,6804 g / cm3 bei 0 ºC.
Dampf = 1,6 (relative Dichte in Bezug auf Luft, Luft = 1).
Löslichkeit
In Wasser sehr gut löslich: 163 g / 100 g Wasser bei 40 ° C. Löslich in Ethanol und Ethylether.
pH
Wässrige Dimethylaminlösungen sind stark alkalisch.
Dissoziationskonstante
K.b = 5,4 × 10-4
pKzu konjugierte Säure = 10,732 bei 25 ° C. Die konjugierte Säure ist das Dimethylammoniumion: (CH3) NHzwei+
Chemische Eigenschaften
Flüssiges Dimethylamin kann einige Kunststoffe, Kautschuke und Beschichtungen angreifen.
In Wasser gelöst nimmt das freie Elektronenpaar (N) von Stickstoff ein Proton (H) an+) aus dem Wasser, so dass ein OH frei bleibt-, so bildet es sehr alkalische und ätzende Lösungen:
Dimethylamin + Wasser → Dimethylammoniumion + Hydroxylion
(CH3)zweiNH + H.zweiO → (CH3)zweiNHzwei+ + Oh-
Mit Salpetersäure erhalten Sie ein Nitratsalz, dh Dimethylammoniumnitrat:
Dimethylamin + Salpetersäure → Dimethylammoniumnitrat
(CH3)zweiNH + HNO3 → (CH3)zweiNHzwei+NICHT3-
Andere Eigenschaften
Wenn es sich in geringer Konzentration in der Luft befindet, hat es einen fischartigen Geruch, während es in hohen Konzentrationen nach Ammoniak (NH) riecht3).
Biochemische Reaktionen
Im Körper kann Dimethylamin unter schwach sauren Bedingungen eine Nitrosierung eingehen, um Dimethylnitrosamin eine krebserzeugende Verbindung (CH) zu geben3)zweiN-NO.
Die Bildung von Dimethylnitrosamin erfolgt aus Dimethylamin und Nitrit (Natriumnitrit) im Magen (bei pH 5-6) durch die Einwirkung von Bakterien im Magen-Darm-Trakt. Natriumnitrit ist in einigen Lebensmitteln enthalten.
Dimethylamin + Natriumnitrit → Dimethylnitrosamin + Natriumhydroxid
(CH3)zweiNH + NaNOzwei → (CH3)zweiN-NO + NaOH
Erhalten
Dimethylamin wird kommerziell durch Umsetzen von Methanol (CH) hergestellt3OH) mit Ammoniak (NH3) bei 350-450ºC in Gegenwart eines Siliciumdioxid-Aluminiumoxid-Katalysators (SiO)zwei/ZumzweiODER3).
2 CH3OH + NH3 → (CH3)zweiNH + 2 H.zweiODER
Da auch Monomethylamin und Trimethylamin hergestellt werden, erfolgt die Reinigung in einer Reihe von vier bis fünf Destillationskolonnen..
Präsenz in der Natur
Dimethylamin kommt in Pflanzen und Tieren vor. Es ist auch natürlich und reichlich im menschlichen Urin vorhanden.
Es wird geschätzt, dass seine Anwesenheit beim Menschen auf die Tatsache zurückzuführen ist, dass es von bestimmten Arten von Darmbakterien aus einigen in Lebensmitteln vorkommenden Verbindungen produziert wird.
Einige dieser Verbindungen sind Cholin (eine Verbindung, die mit der Gruppe der B-Vitamine assoziiert ist) und Trimethylaminoxid. Es wird auch angenommen, dass es von einem Enzym stammt, das Stickoxid (NO) hemmt, das im Körper gebildet wird..
Bestimmte Informationsquellen weisen darauf hin, dass der Anstieg des Dimethylamins im Urin durch die Aufnahme von Fisch und Meeresfrüchten verursacht wird, wobei die höchsten Werte beim Verzehr von Tintenfisch, Seehecht, Sardinen, Schwertfisch, Kabeljau, Wittling und Rochen erzielt werden..

Patienten mit überschüssigem Dimethylamin
Dimethylamin wird als urämisches Toxin angesehen, dh als eine Substanz, die Schaden anrichten kann, wenn ihre Konzentration im Urin zu hoch ist. Tatsächlich wurden bei Patienten mit Nierenerkrankungen im Endstadium sehr hohe Dimethylaminspiegel beobachtet..
Es wird angenommen, dass es bei diesen Patienten zu einer Überbevölkerung von Darmbakterien kommen kann, die diese produzieren könnten.
Anwendungen
Dimethylamin oder DMA wird verwendet, um:
- Herstellung anderer Verbindungen.
- Herstellung der Lösungsmittel Dimethylformamid und Dimethylacetamid.
- Beschleunigen Sie die Vulkanisation bestimmter Kautschuke.
- Entfernen Sie die Haare während des Bräunens aus den Häuten.
- Wirken als Antioxidans für Lösungsmittel.
- Als mineralisches Flotationsmittel dienen.
- Korrosionsschutz und als Antifoulingmittel für Rohre.
- Funktion als Tensid.
- Machen Sie Seifen und Reinigungsmittel.
- Als Textilchemiker tätig sein.
- Funktion als Antiklopfmittel in Kraftstoffen und als Stabilisator für Benzin.
- Bereiten Sie Farbstoffe vor.
- Saure Gase aufnehmen.
- Als Treibmittel für Pestizide und Raketen dienen.
- Seien Sie Teil der Mittel zur Wasseraufbereitung.
- Wirken als Fungizid in agrochemischen Produkten.
- Eingestellte Anwendungen wie das Anziehen und Töten von Rüsselkäfern oder Insekten, die Baumwolle angreifen.


Risiken
Dimethylamin-Dämpfe reizen Haut, Augen und Atemwege..
Wenn es in flüssiger Form mit der Haut in Kontakt kommt, kann es zu Erfrierungen und Verätzungen kommen. Das Einatmen hat gesundheitsschädliche Auswirkungen.
DMA-Gas ist ätzend und kann ätzende wässrige Lösungen bilden. Ihre wässrigen Lösungen können entzündlich werden, wenn sie nicht gut verdünnt werden..
Dimethylamin in Gasform entzündet sich leicht und erzeugt giftige Stickoxiddämpfe (NOx).
Wenn der Behälter, der dieses Gas enthält, Feuer oder starker Hitze ausgesetzt ist, kann er explodieren..
Einfluss von DMA auf die Atmosphäre
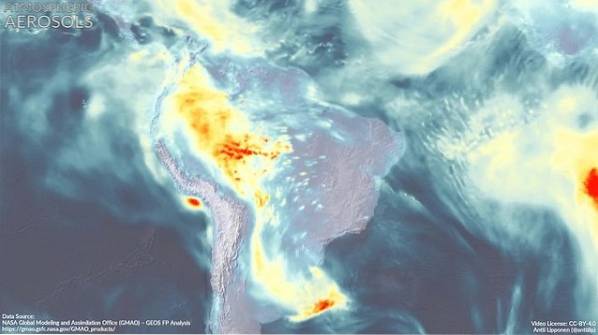
Das atmosphärische Aerosol (sehr kleine Tröpfchen einer Mischung aus natürlichen Verbindungen und / oder Schadstoffen in der Atmosphäre) hat einen tiefgreifenden Einfluss auf das globale Klima und die Luftqualität in den verschiedenen Regionen der Welt..
Die Bildung der neuen Aerosolpartikel ist noch nicht vollständig verstanden.
Es wird geschätzt, dass Dimethylamin zusammen mit anderen Verbindungen an der Bildung dieser Partikel beteiligt ist, was anscheinend von der Tatsache abhängt, dass in der Region starke DMA-Emissionen auftreten..
In Industriegebieten ist beispielsweise die Konzentration höher als in landwirtschaftlichen Gebieten, und dies kann die Art und Weise beeinflussen, in der sich die WRRL beteiligt..
Es ist bemerkenswert, dass nach Ansicht einiger Wissenschaftler das Verbrennen von Pflanzenmaterial, das Glyphosat enthält (eines der weltweit am häufigsten verwendeten Herbizide), zur Bildung von Dimethylamin führen kann.
Verweise
- UNS. Nationalbibliothek für Medizin. (2019). Dimethylamin. Von pubchem.ncbi.nlm.nih.gov wiederhergestellt.
- Kirk-Othmer (1994). Enzyklopädie der chemischen Technologie. Vierte Edition. John Wiley & Sons.
- Morrison, R.T. und Boyd, R.N. (2002). Organische Chemie. 6. Auflage. Prentice-Hall.
- Windholz, M. et al. (Herausgeber) (1983). Der Merck-Index. Eine Enzyklopädie der Chemikalien, Drogen und Biologika. Zehnte Ausgabe. Merck & CO., Inc..
- Abramowitz, M.K. et al. (2010). Die Pathophysiologie der Urämie. Aliphatische Amine. Bei chronischen Nierenerkrankungen, Dialyse und Transplantation (dritte Ausgabe). Von sciencedirect.com wiederhergestellt.
- Li, H. et al. (2019). Einfluss der atmosphärischen Bedingungen auf die Bildung neuer Partikel auf Schwefelsäure-Dimethylamin-Ammoniak-Basis. Chemosphere 2019; 245: 125554. Von ncbi.nlm.nih.gov wiederhergestellt.
- Mackie, J.C. und Kennedy, E.M. (2019). Pyrolyse von Glyphosat und seinen toxischen Produkten. Environ. Sci. Technol. 2019: 53 (23): 13742 & ndash; 13747. Von ncbi.nlm.nih.gov wiederhergestellt.



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.