
Kieselsäureeigenschaften, Reaktionen und Verwendungen

Das Kieselsäure Es ist eine hydratisierte Form von Siliziumoxid. Es ist der allgemeine Name für die Familie der chemischen Verbindungen, die aus einem Silizium und einer bestimmten Menge an Wasserstoff- und Sauerstoffmolekülen bestehen..
Die allgemeine Formel dieser Säuren lautet [SiOx(OH)4-2x]]n, und die häufigste Form, in der es gewöhnlich gefunden wird, ist die von Orthokieselsäure H.4Ja4.
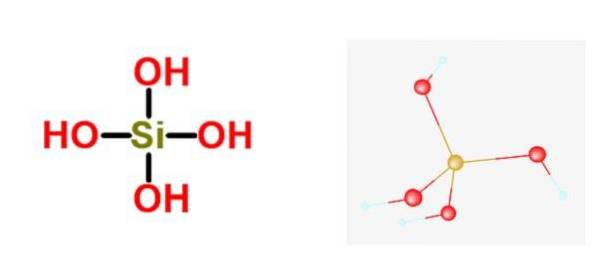
Kieselsäure gehört zur Familie der verschiedenen Silikate. Dies bedeutet, dass das größte metallische Oxoanion das Silikat ist und dass kein nichtmetallisches Atom daran gebunden ist. Es gibt einige Einzelfälle, in denen sie ein nichtmetallisches Atom haben, aber niemals mehr als eines.
Physikalische Eigenschaften der Kieselsäure
Kieselsäure existiert nur in zwei Zuständen, amorph und kristallin. Das erste wird durch einen Fällungsprozess erhalten und das zweite wird als Bergkristall dargestellt.
Kieselsäure in ihrer amorphen Form (SiO3) ist weiß, geschmacklos, wasserunlöslich und bildet mit Molekülen von sich selbst keine zusammenhängende plastische Masse, wie sie bei Aluminium auftritt.
In seinem kristallinen Zustand wird es von keiner Oxacid gelöst. Wenn eine sehr verdünnte Lösung einer Kieselsäurelösung mit Schwefel-, Salpeter- oder Salzsäure behandelt wird, fällt die Kieselsäure nicht aus. Stattdessen scheint es als Hydrat in Wasser gelöst zu sein.
Wenn eine Lösung der Säure oder Säure zu einer Silikatlösung gegeben wird, fällt das Hydrat in gelatineartiger Form aus, so dass es beim Trocknen und anschließenden Erhitzen mit großer Energie zu einer unlöslichen Substanz wird.
Chemische Reaktionen
Kieselsäure ist extrem schwach und verliert ihr erstes Proton erst bei Annäherung an pH 10. Nur 3 bekannte Reaktionen mit dieser Säure treten unter normalen physiologischen Lebensbedingungen auf..
- Reaktion mit sich selbst, wenn die Löslichkeit überschritten wird, um amorphes Siliciumdioxidhydrat zu bilden.
- Seine Reaktion mit Aluminiumhydroxid unter Bildung von Aluminiumsilikathydroxid.
- Reaktion mit überschüssigem Molybdat unter Bildung von Heteropolysäuren wie Silicomolybdat.
Wo ist Kieselsäure gefunden?
Silizium ist nach Sauerstoff das häufigste Element in der Natur, es liegt in Form von Kristallen vor. In wässrigem Medium wird es nicht ionisierend, so dass die Siliziumsalze im Ozean das Silizium ansäuern und Kieselsäure erzeugen können..
Die Nettoeinträge von Kieselsäure in den Weltozean wurden mit 6,1 ± 2,0 Teramol Silizium pro Jahr (1 Teramol = 1012 Mol) gefunden. Fast 80% dieses Beitrags stammen aus Flüssen mit einer globalen Durchschnittskonzentration von 150 Mikromolar (Konzentration in Wasser)..
In modernen marinen Sedimenten beträgt die Nettoausbeute an biogenem Silizium (Umwandlung von gelöstem Silikat in teilchenförmiges Skelettmaterial) 7,1 ± 1,8 Teramol pro Jahr.
Die Bruttoproduktion von biogener Kieselsäure in Oberflächengewässern beträgt 240 ± 40 Teramol Silizium pro Jahr, und das Konservierungsverhältnis (Anreicherung von Opalen in Sedimenten / Bruttoproduktion in Oberflächengewässern) beträgt 3 Prozent..
In der Flora kann es in der Pflanze gefunden werden Borago officinalis (Borraje), das in seiner Zusammensetzung bis zu 2,2% Kieselsäure enthält.
Orthokieselsäure ist die häufigste Form von Kieselsäure, die an vielen verschiedenen Orten vorkommt. Die größten bioverfügbaren Quellen dieser Säure befinden sich im Wasser, entweder im Meerwasser oder in anderen Getränken wie Bier..
Um es im Labor zu erhalten, folgt es dem gleichen Prinzip wie im Ozean. Es kann durch Ansäuern von Natriumsilikat in einer wässrigen Lösung erhalten werden..
Verwendung im Alltag
Zahnpasta
Es ist das Schleifgel, das in Zahnpasta oder im klaren Teil von zerkratzter Zahnpasta verwendet wird, da es in Kombination mit Kalziumkarbonat hilft, Plaque beim Bürsten sicher zu entfernen.
Es ist als sichere Verbindung bei der US-amerikanischen Food & Drug Administration registriert und weist keine bekannte Toxizität oder Karzinogenität auf.
Trockenmittel
Wenn es in einem Ofen getrocknet wird, verliert es Wasser und wird zu einem Trockenmittel (eine Substanz, die Wasser aus der Luft zieht). Daher befinden sich kleine Päckchen Kieselgelkristalle in Behältern, deren Inhalt durch Feuchtigkeit wie Vitaminflaschen, Elektronik, Schuhe oder Lederprodukte beschädigt werden kann..
Andere Verwendungen
Es kann in Geschenkartikelläden wie magischen Steinen, im chemischen Garten oder im Kristallgarten gefunden werden. Seine trockene Form wird mit Salzen verschiedener Metalle gemischt.
Wenn Natrium ins Wasser geworfen wird, wird es durch das Metall ersetzt, und da das Metallsilikat nicht wasserlöslich ist, bildet sich ein Niederschlag mit der charakteristischen Farbe des Metalls. Metallsilikat dehnt sich auch als Gel aus und wächst als bunte Stalagmiten in Wasser..
Medizinische Vorteile von Orthokieselsäure (OSA)
Orthokieselsäure ist das beste bioverfügbare Siliziummedium für den Menschen. Es kann verwendet werden, um verschiedene Gesundheitszustände wie Alzheimer, Arthritis, Atherosklerose, Bluthochdruck, Herzerkrankungen, Osteoporose, Schlaganfall und Haare zu behandeln.
Knochen Gesundheit
In einer Studie von 2008 mit 136 Frauen mit Osteopenie erhielten sie ein Jahr lang täglich Orthokieselsäure zusammen mit Kalzium und Vitamin D oder einem Placebo. Nach einem Jahr verbesserten sich die Knochenbildung der Teilnehmer, die die Säure erhielten.
Wissenschaftler sagen, dass dies auf die Fähigkeit von Orthokieselsäure zurückzuführen ist, die Produktion von Kollagen (einem im Bindegewebe vorkommenden Protein) zu stimulieren und die Entwicklung knochenbildender Zellen zu fördern..
Haargesundheit
Eine kleine Studie aus dem Jahr 2007 legt nahe, dass diese Säure zur Verbesserung der Haarqualität und -gesundheit beitragen kann. In der Studie wurden 48 Frauen mit "feinem Haar" in zwei Gruppen eingeteilt und neun Monate lang mit einem Placebo oder einem Orthosiliciumpräparat behandelt..
Die Forscher fanden heraus, dass Orthosalicylsäure die Haarstärke und -dicke zu erhöhen schien. Im Allgemeinen wurde die Haarqualität auch durch eine Orthosalicylsäure-Supplementierung verbessert.
Verweise
- Nationales Zentrum für Informationen zur Biotechnologie. PubChem Compound Database; CID = 14942. Wiederhergestellt von: pubchem.ncbi.nlm.nih.gov.
- Graham, T. (1863). Zu den Eigenschaften von Kieselsäure und anderen analogen kolloidalen Substanzen. Verfahren der Royal Society of London, 13, 335-341. Wiederhergestellt von: jstor.org.
- Die Herausgeber der Encyclopedia Britannica (1998) Silicic Acid Chemical Compound. Enzyklopädie Britannica. Wiederhergestellt von: britannica.com.
- Tomsofmaine.com. (2017). Hydrated Silica | Tom ist von Maine. [online] Wiederhergestellt von: tomsofmaine.com.
- William Thomas Brande, Alfred Swaine Taylor. Chemie. Blanchard und Lea. [online] Abgerufen am 21. März 2017 von books.google.co.ve.id.
- Field, S. (2017). Kieselsäuregel. [online] Abgerufen am 22. März 2017 von: sci-toys.com.


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.