
Begründung, Herstellung und Verwendung von Phosphatpuffer (PBS)
Das Phosphatpuffer, BPS oder Phosphatpuffer-Kochsalzlösung Es ist eine Puffer- und isotonische Lösung, deren Funktion darin besteht, den pH-Wert und den osmotischen Druck so nah wie möglich an der natürlichen biologischen (physiologischen) Umgebung zu halten. Das Akronym PBS steht für phosphatgepufferte Kochsalzlösung..
Der pH-Wert und die Osmolarität sind zwei sehr wichtige Aspekte, die in bestimmten Laborprotokollen kontrolliert werden müssen. Im Falle eines pH-Werts ist es wichtig, dass er kontrolliert wird, insbesondere bei biochemischen Reaktionen, da diese variieren können oder nicht durchgeführt werden, wenn die Reaktanten einen ungeeigneten pH-Wert haben.

In der Zwischenzeit ist die Kontrolle der Osmolarität insbesondere bei der Arbeit mit lebenden Zellen von wesentlicher Bedeutung, da die Plasmamembranen der Zellen entsprechend der Konzentration der gelösten Stoffe reagieren, in denen sie sich befinden..
Wenn die Zellen auf ein hypertonisches Medium übertragen werden, dehydrieren sie, da der Wassergradient zu der Seite transportiert wird, an der eine höhere Konzentration an gelösten Stoffen vorliegt. Wenn andererseits Zellen in ein hypotonisches Medium gegeben werden, absorbieren die Zellen Flüssigkeit, bis sie lysiert sind..
Aus diesem Grund wird der PBS-Puffer für Laborprotokolle verwendet, bei denen die Zellen gewartet werden müssen. in vitro, Auf diese Weise werden die Zellen nicht beschädigt.
PBS besteht aus einer Kombination von Salzen wie Natriumchlorid, Natriumphosphat, Kaliumchlorid und Kaliumphosphat. Die Zusammensetzung des PBS kann je nach Protokoll variieren..
Artikelverzeichnis
- 1 Begründung
- 2 Vorbereitung
- 2.1 -Stocklösung Phosphatpuffer-Salzlösung (PBS 10X)
- 2,2-Pufferphosphatsalzlösung (1 × PBS)
- 2.3. Lösungen zur pH-Einstellung
- 3 Verwendungen
- 4 Einschränkungen
- 5 Referenzen
Basis
Grundsätzlich besteht die Funktion des Salzphosphatpuffers darin, einen konstanten physiologischen pH-Wert zusammen mit einer Elektrolytkonzentration aufrechtzuerhalten, die derjenigen im Körper ähnlich ist..
In dieser Umgebung können Zellen stabil bleiben, da physiologische Bedingungen so weit wie möglich simuliert werden..
Falls erforderlich, können der ursprünglichen PBS-Formulierung andere Verbindungen zugesetzt werden, beispielsweise ist die Zugabe von EDTA zu dem Puffer zum Waschen roter Blutkörperchen im Kreuzunverträglichkeitstest nützlich..
EDTA verhindert, dass die im Serum vorhandene Fraktion des Komplements C1 gespalten und an die roten Blutkörperchen lysiert wird, dh es vermeidet falsche Inkompatibilitätsergebnisse. Darüber hinaus hilft EDTA, Zellen zu dissoziieren.
Vorbereitung
Die Menge an Salzen, die für die Herstellung der PBS-phosphatgepufferten Salzlösung gewogen werden muss, hängt von der Menge ab, die hergestellt werden muss:
-Stammphosphat-gepufferte Salzlösung (10 × PBS)
Für einen Liter Lösung:
Wiegen:
80,6 g NaCl,
2,2 g KCl,
11,5 g NazweiHPO4,
2,0 g KHzweiHPO4
Vorbereitungstechnik
Die schweren Salze in ein Becherglas geben, ausreichend Wasser (80%) hinzufügen und mit einem Magnetstab auf der Rührplatte mischen, bis sich die Salze aufgelöst haben..

Filtern, um ungelöste Partikel zu entfernen. Verwenden Sie Filter mit 0,45 µm Poren. Autoklavieren und aseptisch in einer Laminar-Flow-Haube in Gläsern mit Deckel verteilen.
Die 10X-Lösung (konzentriert) stellt den pH-Wert nicht ein. Die Einstellung erfolgt nach Verdünnung auf die 1X PBS-Pufferkonzentration (1:10 Verdünnung)..
-Phosphatpuffer-Kochsalzlösung (1 × PBS)
1X PBS kann direkt hergestellt werden, wobei die entsprechenden Mengen jedes Salzes gewogen werden, oder es kann hergestellt werden, indem die Stammlösung (1:10) mit sterilem destilliertem Wasser verdünnt wird..
-Um einen Liter 1X PBS phosphatgepufferte Kochsalzlösung direkt herzustellen, wiegen Sie:
8,06 g NaCl,
0,22 g KCl,
1,15 g NazweiHPO4,
0,20 g KHzweiHPO4
Vorbereitungstechnik
Verfahren Sie wie für die konzentrierte Lösung erläutert. Anschließend muss der pH-Wert eingestellt werden. Messen Sie dazu den pH-Wert und verwenden Sie je nach Ergebnis Säure (HCl) oder Base (NaOH), um den pH-Wert nach Bedarf zu senken bzw. zu erhöhen, bis er 7,4 beträgt.
Die Säure oder Base wird tropfenweise zugegeben, während der pH-Wert der Lösung mit einem pH-Meter überwacht wird. Filtern, autoklavieren und nach Bedarf aseptisch in konische Röhrchen oder Gläser verteilen.
-So stellen Sie 1X PBS aus der 10X-Stammlösung her:
Machen Sie eine 1:10 Verdünnung. Um beispielsweise 1 Liter 1X PBS herzustellen, messen Sie 100 ml der Stammlösung ab und geben Sie 700 ml steriles destilliertes Wasser hinzu. Stellen Sie den pH-Wert ein und füllen Sie die Wassermenge auf 1000 ml.
Der hergestellte PBS-Puffer ist farblos und transparent.
Das tägliche PBS kann bei Raumtemperatur und der Rest im Kühlschrank aufbewahrt werden.
.Lösungen zur pH-Einstellung
HCl
Für 100 ml 1 molare HCl (Salzsäure).
Messen Sie 91 ml destilliertes Wasser und geben Sie es in ein 250 ml Becherglas.
Messen Sie 8,62 ml konzentrierte HCl und geben Sie sie langsam in das Becherglas mit dem Wasser (niemals umgekehrt). Treffen Sie die entsprechenden Biosicherheitsmaßnahmen beim Umgang mit starken Säuren (stark ätzende Substanz)..
5 Minuten lang mischen, vorzugsweise unter Verwendung einer Rührplatte mit einem Magnetstab im Glas. In einen 100 ml Ballon geben und mit H auf 100 ml auffüllenzweiOder destilliert.
NaOH
Für 100 ml NaOH (Natriumhydroxid) 10 molar.
Messen Sie 40 ml destilliertes Wasser und geben Sie es in ein 250 ml Becherglas. Messen Sie 40 g NaOH und geben Sie es ins Wasser. Mischen Sie mit einer Rührplatte mit einem Magnetstab im Glas.
In einen 100-ml-Messkolben überführen und mit destilliertem Wasser bis zur Marke auffüllen. Beachten Sie die Vorschriften zur biologischen Sicherheit, da diese Reaktion exotherm ist (sie setzt Energie in Form von Wärme frei)..
Wenn Sie andere Mengen Phosphat-Kochsalzlösung herstellen möchten, können Sie die folgende Tabelle konsultieren:
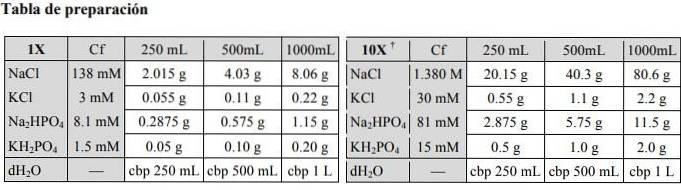
Anwendungen
Hauptsächlich in den Laboratorien für Zellbiologie, Immunologie, Immunhistochemie, Bakteriologie, Virologie und Forschung eingesetzt.
Es ist ideal zum Waschen von Zellen durch Zentrifugation (rote Blutkörperchen), Waschen von Zellmonoschichten, bei spektroskopischen Ellipsometrietechniken, bei der Quantifizierung von bakteriellen Biofilmen, bei der Aufrechterhaltung von Zellkulturen für Viren als Waschlösung bei der indirekten Immunfluoreszenztechnik und in Techniken zur Charakterisierung monoklonaler Antikörper.
Es wird auch verwendet, um Zellen oder Gewebe als Verdünnungsmittel für die Zellzählung, die Herstellung von zellulären Enzymen (Trypsin), als Verdünnungsmittel für das Austrocknungsverfahren für Biomoleküle und zur Herstellung anderer Reagenzien zu transportieren..
Auf der anderen Seite haben Martin et al. 2006 gezeigt, dass PBS in forensischen Laboratorien nützlich ist, insbesondere bei der Gewinnung von Spermien aus Vaginalabstrichen oder bei der Gewinnung von Vaginalzellen aus Penisabstrichen. Auf diese Weise kann festgestellt werden, ob eine sexuelle Beziehung besteht.
Einschränkungen
-Einige PBS-Puffer enthalten eine Substanz namens Natriumazid als Konservierungsmittel. Diese Verbindung kann explosive Substanzen erzeugen, wenn sie mit Blei oder Kupfer in Kontakt kommt. Aus diesem Grund ist bei der Entsorgung dieses Reagenzes im Abfluss besondere Vorsicht geboten. Wenn es auf diese Weise verworfen wird, muss viel Wasser hinzugefügt werden, um es so weit wie möglich zu verdünnen..
-Dem Phosphatpuffer sollte kein Zink zugesetzt werden, da dadurch einige Salze ausfallen.
-Wangen et al. Stellten 2018 fest, dass die Verwendung von PBS nicht zum Waschen von primären Zellen der akuten myeloischen Leukämie (AML) geeignet ist, die aus peripherem Blut extrahiert wurden, da viele Zellen durch Lyse verloren gehen und das Proteinmaterial stark abnimmt.
Daher stellten sie fest, dass primäre AML-Zellen nach Lagerung in flüssigem Stickstoff nicht mit PBS gewaschen werden sollten..
Verweise
- Coll J. (1993). Diagnosetechniken in der Virologie. Ed Díaz de Santos. 360 pg
- Rodríguez M, Ortiz T. Zellkultur. Mediumwechsel. Abteilung für normale und pathologische Zytologie und Histologie Universität Sevilla. Verfügbar bei personal.us.es
- Herstellung von phosphatgepufferter Salzlösung (PBS). (2008). Standard Operating Procedures (SOPs) Labor für Virus- und Humangenomik UASLP School of Medicine. Verfügbar unter: genomica.uaslp.mx
- "Phosphatpuffer-Kochsalzlösung." Wikipedia, die freie Enzyklopädie. 3. April 2019, 19:36 UTC. 13. April 2019, 02:57 en.wikipedia.org.
- Pietrasanta L, Von-Bilderling C. Themen der Molekularbiophysik. Verfügbar unter: users.df.uba.ar
- Rediar. Handbuch. PBS + EDTA. Verfügbar unter: felsan.com.ar
- Martin NC, Pirie AA, Ford LV, Callaghan CL, McTurk K., Lucy D., Scrimger DG. Verwendung von phosphatgepufferter Kochsalzlösung zur Gewinnung von Zellen und Spermien aus Tupfern. Sci Gerechtigkeit. 2006; 46 (3): 179 & ndash; 84. Verfügbar in: ncbi.nlm.nih.gov
- Wangen R, Aasebø E, Trentani A., et al. Konservierungsmethode und Waschen mit phosphatgepufferter Kochsalzlösung beeinflussen das Proteom der akuten myeloischen Leukämie. Int J Mol Sci. 2018; 19 (1): 296. Verfügbar in: ncbi.nlm.nih.gov
- Martínez R, Gragera R. (2008). Theoretische und praktische Grundlagen der Histochemie. Oberster Rat für wissenschaftliche Untersuchungen. Madrid. Verfügbar unter: books.google.co.ve



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.