
Aminoglykoside Klassifizierung, Wirkungen, Indikationen, Kontraindikationen

Das Aminoglycoside Es handelt sich um eine Reihe von Antibiotika, die dieselben chemischen und pharmakologischen Eigenschaften aufweisen. Sie haben eine bakterizide Wirkung gegen aerobe gramnegative Bakterien (Bakterien, die hellrosa und nicht dunkelblau oder lila mit Gramfärbung färben).
Das erste entdeckte Aminoglycosid war 1943 Streptomycin. Später erschienen Tobramycin und Gentamicin als wirksame Anti-Gram-negative Antibiotika. In den 1970er Jahren (1970) wurden halbsynthetische Aminoglycoside wie Amikacin, Netilmycin und Dibekacin entwickelt..

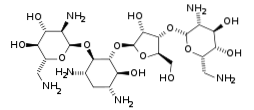
Die meisten Mitglieder dieser Familie haben in ihrer Struktur ein Aminocyclitol (einen cyclischen Alkohol mit einer Aminogruppe R-NH2), das durch eine glycosidische Bindung an einen oder mehrere Aminozucker gebunden ist, so dass sie tatsächlich Aminoglycoside-Aminocyclitole sind.
Diese Antibiotika werden nicht oral resorbiert, daher werden sie parenteral (intravenös, intramuskulär oder subkutan) verabreicht oder topisch angewendet. Sie werden durch glomeruläre Filtration eliminiert, ohne zuvor metabolisiert zu werden.
Alle Mitglieder dieser Familie zeigen einen gewissen Grad an Nephrotoxizität (Nierentoxine) und / oder Ototoxizität (toxisch sowohl für das Ohr als auch für das Vestibularsystem, kann zu Hör- und Gleichgewichtsstörungen führen)..
Sie werden im Allgemeinen in Kombination mit etwas Beta-Lactam (einer anderen Familie von Antibiotika) angewendet, und ihre Verwendung ist normalerweise auf schwere Infektionen beschränkt.
Diese Antibiotika sind bei Patienten kontraindiziert, die allergische Reaktionen auf diese Medikamente entwickelt haben. Obwohl sie in die Muttermilch übergehen, da sie nicht über den intestinalen (oralen) Weg aufgenommen werden, werden sie als geeignet angesehen, der Mutter bei Bedarf während der Stillzeit verabreicht zu werden..
Die Anwendung während der Schwangerschaft ist nur in Fällen zulässig, in denen der klinische Nutzen die Risiken überwiegt (Risikokategorie D)..
Artikelverzeichnis
- 1 Wirkmechanismus
- 2 Klassifizierung
- 2.1 Aminoglycosid mit Aminocyclit
- 2.2 Aminocyclit ohne Aminoglycosid: Spectinomycin
- 3 Nebenwirkungen
- 3.1 - Ototoxizität
- 3.2 - Nephrotoxizität
- 3.3 - Neurotoxizität und andere toxische Wirkungen
- 4 Beständigkeit gegen Aminoglykoside
- 5 Indikationen
- 6 Gegenanzeigen
- 7 Referenzen
Wirkmechanismus
Alle Aminoglycoside hemmen die Proteinsynthese in anfälligen Bakterien. Diese haften an der 30S-Einheit der bakteriellen Ribosomen und hemmen deren Funktion. Im Gegensatz zu den meisten bakteriostatischen antimikrobiellen Wirkstoffen, die die Proteinsynthese hemmen, sind diese bakterizid.
"Bakteriostatisch" leitet sich vom Präfix "Bakterium" ab, was Bakterien bedeutet, und "Stasis", dem griechischen Ende, das statisch bedeutet, ohne Änderung. In der Medizin werden bakteriostatische Mittel eingesetzt, um den Stoffwechsel von Bakterien zu reduzieren und deren Wachstum und Fortpflanzung zu verlangsamen..
Wenn das bakteriostatische Mittel durch Auflösung eliminiert wird, entwickeln sich die zuvor gehemmten Bakterien weiter. Ein bakterizides Mittel ist eines, das Bakterien abtöten kann. Aminoglykoside sind bakterizid.
Die bakterizide Wirkung von Aminoglycosiden ist konzentrationsabhängig. Aminoglycoside dringen durch Wasserkanäle, sogenannte Aquaporine, in den periplasmatischen Raum aerober gramnegativer Bakterien ein..
Der Transport durch die zytoplasmatische Membran hängt vom Elektronentransport ab und kann durch Anaerobiose (Abwesenheit von Sauerstoff), Calcium, Magnesium, sauren pH-Wert oder Hyperosmolarität gehemmt oder blockiert werden..
In der Zelle binden Aminoglycoside an der 30S-Untereinheit an Polysomen (mehrere Ribosomen, die dieselbe mRNA translatieren). Sie stören die Proteinsynthese und führen zu einem Lesefehler und einer vorzeitigen Beendigung des mRNA-Translationsprozesses.
Dies erzeugt defekte Proteine, die beim Einsetzen in die Zellmembran ihre Permeabilität verändern, was später den späteren Eintritt dieser Antibiotika erleichtert. Später werden Ionenlecks beobachtet, gefolgt von größeren Molekülen, bis vor dem Tod der Bakterien die Proteine verloren gehen..
Einstufung
Aminoglycoside werden in zwei große Gruppen eingeteilt, je nachdem, ob sie ein Aminocyclitol mit oder ohne Aminoglycosidkomponente aufweisen: Aminoglycoside mit Aminocyclitol und Aminocyclitol ohne Aminoglycosid.
In der ersten Gruppe, die Aminocyclit mit Aminoglycosidkomponente enthält, gibt es zwei Untergruppen. Diese Untergruppen werden durch die verschiedenen Komponenten von Aminocyclit gebildet: Streptidin und Desoxystreptamin.

Somit gibt es eine Untergruppe mit Aminocyclitol-Streptidin und eine andere mit Aminocyclitol-Desoxystreptamin. Die wichtigsten Aminoglycoside in jeder Gruppe sind unten gezeigt.
Aminoglycosid mit Aminocyclit
Aminocyclitol-Streptidin: Streptomycin
Aminocyclitoldesoxystreptamin: Innerhalb dieser Gruppe befinden sich die Familien Kanamycin, Gentamicin und andere.
Kanamycin Familie:
- Kanamycin
- Amikacin
- Tobramycin
- Dibekacin
Gentamicin Familie:
- Gentamicin
- Sisomycin
- Netilmycin
- Isepamycin
Andere:
- Neomycin
- Paromomycin
Aminocyclit ohne Aminoglycosid: Spectinomycin
Nebenwirkungen
Alle Aminoglykoside sind potenziell toxisch für das Nierensystem, das Hörsystem und das Vestibularsystem. Diese toxischen Wirkungen können reversibel oder irreversibel sein. Diese nachteiligen sekundären Folgen erschweren die Verabreichung und Verwendung dieser Antibiotika..
Wenn es notwendig ist, ein Aminoglykosid über lange Zeiträume und in hohen Dosen zuzuführen, ist es notwendig, die Hör-, Vestibular- und Nierenfunktion zu überwachen, da diese Schäden im Anfangsstadium reversibel sind.
- Ototoxizität
Bei der Verabreichung von Aminoglykosiden kann es zu Funktionsstörungen sowohl des auditorischen Systems als auch des vestibulären Systems kommen. Diese Medikamente reichern sich an und konzentrieren sich in der Perilymphe und Endolymphe des Innenohrs, insbesondere wenn hohe Dosen angewendet werden..
Die Diffusion von diesen Ohrflüssigkeiten zurück in das Plasma ist sehr langsam und die Halbwertszeit von Aminoglykosiden im Ohr ist 5- bis 6-mal höher als im Blutplasma. Ototoxizität tritt häufiger bei Patienten mit anhaltend hohen Plasmakonzentrationen auf.
Bei niedrigen Dosen wird eine Schädigung der Sinneszellen des Vestibularorgans und der Cochlea beobachtet, die die Enden (Stereozilien) der Haarzellen betrifft. Bei höheren Dosen wird in diesen Zellen eine Grundschädigung beobachtet, bis die Zerstörung der Sinneszellen erzeugt wird..
Wenn die Sinneszellen zerstört werden, ist der Effekt irreversibel und folglich treten dauerhafte Hörverluste auf. Da Cochlea-Sinneszellen mit dem Alter verloren gehen, sind ältere Patienten bei Verwendung dieser Antibiotika anfälliger für Ototoxizität..
Drogen wie Furosemid oder der Acid ethacrinic Sie verstärken die ototoxische Wirkung von Aminoglykosiden. Beide Medikamente sind Schleifendiuretika (Erhöhung des Urinausstoßes) zur Behandlung von Bluthochdruck und Ödemen..
Obwohl alle Aminoglykoside sowohl die Cochlea- als auch die Vestibularfunktion beeinflussen können, besteht eine offensichtliche bevorzugte Toxizität.
Daher beeinflussen Streptomycin und Gentamicin bevorzugt das Vestibularsystem, während Amikacin, Kanamycin und Neomycin hauptsächlich die Hörfunktion beeinflussen und Tobramycin beide Funktionen gleichermaßen beeinflusst..
Symptome der Cochlea-Ototoxizität
Als erstes Symptom der Ototoxizität tritt normalerweise ein hochfrequenter Tinnitus (Zischen oder Summen, das nicht mit Geräuschen von außen verbunden ist) auf. Wenn die Behandlung nicht unterbrochen wird, ist der Schaden in wenigen Tagen dauerhaft.
Tinnitus kann bis zu zwei Wochen andauern, und da die Wahrnehmung hochfrequenter Geräusche zuerst verloren geht, ist sich der Patient seines Hörverlusts zunächst nicht bewusst. Wenn die Behandlung unter diesen Bedingungen fortgesetzt wird, schreitet der Hörverlust fort und entwickelt Sprachprobleme.
Symptome der vestibulären Ototoxizität
Zunächst treten mäßig intensive Kopfschmerzen auf. Darauf folgen Erbrechen, Übelkeit und Probleme mit dem Haltungsgleichgewicht, die ein bis zwei Wochen anhalten können. Die auffälligsten Symptome sind Schwindel in aufrechter Position, mit Schwierigkeiten beim Sitzen oder Stehen ohne visuelle Hinweise.
Die akuten Symptome klingen abrupt ab und werden über einen Zeitraum von ungefähr zwei Monaten durch Manifestationen einer chronischen Labyrinthitis ersetzt. Nach und nach tritt eine Kompensation auf, und beim Schließen der Augen treten nur Symptome auf. Die Erholung von dieser Phase dauert 12 bis 18 Monate.
Die meisten dieser Patienten haben einen gewissen bleibenden Restschaden. Da es keine spezifische Behandlung für vestibuläre Schäden gibt, ist die Suspendierung des Aminoglykosids bei den ersten klinischen Manifestationen die einzig wirksame Maßnahme zur Vermeidung dauerhafter Verletzungen.
- Nephrotoxizität
Ungefähr 8 bis 25% der Patienten, die mehrere Tage lang mit einem Aminoglykosid behandelt werden, entwickeln eine reversible Nierenfunktionsstörung. Diese Toxizität ist das Ergebnis der Akkumulation, Konzentration und Retention von Aminoglycosiden in den Zellen des proximalen Tubulus der Niere..
Folglich wird die Struktur und Funktion des proximalen Tubulus verändert. Im Urin treten zunächst mäßige Proteinurie und hyaline Abdrücke auf. Nach einigen Tagen tritt eine Verringerung des glomerulären Filtrationsvolumens mit einem leichten Anstieg der Plasmakreatininwerte auf..
Nierenveränderungen sind häufig reversibel, da der proximale Tubulus die Fähigkeit zur Regeneration besitzt. Die Nierentoxizität hängt von der abgegebenen Gesamtmenge und vom verwendeten Aminoglycosid ab..
Neomycin ist eines der Aminoglycoside, das eine größere Nierentoxizität aufweist, da es in viel größeren Mengen in der Nierenrinde konzentriert ist als die anderen Aminoglycoside.
- Neurotoxizität und andere toxische Wirkungen
Andere weniger häufige toxische Wirkungen wurden beschrieben, darunter die neuromuskuläre Blockade, die in einigen Muskeln Atemprobleme und / oder Lähmungen verursachen kann. Veränderungen der Sehnervenfunktion mit dem Auftreten von Skotomen, die vorübergehende Bereiche der Blindheit sind, und peripherer Neuritis.
Resistenz gegen Aminoglycoside
Die Resistenz von Mikroorganismen gegen Aminoglykoside kann auf eine der folgenden Ursachen zurückzuführen sein: 1) Die Membranen der Bakterien sind gegen diese Antibiotika undurchlässig. 2) Die Ribosomen dieser Bakterien haben eine geringe Affinität für das Antibiotikum. 3) Die Bakterien synthetisieren inaktivierende Enzyme das Aminoglycosid.
Die ersten beiden Ursachen erklären die natürliche Resistenz gegen Aminoglykoside. Im Gegensatz dazu erklärt die Enzyminaktivierung die erworbene Resistenz, die klinisch unter Verwendung von Aminoglycosiden beschrieben wurde..
Die Gene für die Synthese dieser Enzyme werden durch Plasmide übertragen. Plasmide sind kreisförmige Strukturen extrachromosomaler DNA. Diese Plasmide sind in der Natur weit verbreitet, insbesondere aber in Bakterien in der Umgebung von Krankenhäusern..
Plasmide kodieren für viele Enzyme und diese inaktivieren Aminoglycoside. Da die Enzyme, die jedes Aminoglycosid inaktivieren, unterschiedlich sind, führt die Resistenz für eines nicht unbedingt zur Resistenz für ein anderes..
Während dies für Streptomycin und Gentamicin gilt, zeigt die Resistenz gegen Gentamicin (als das Enzym, das es bifunktionell verursacht) gleichzeitig eine Resistenz gegen Tobramycin, Amikacin, Kanamycin und Netilmicin..
Indikationen
Obwohl weniger toxische Antibiotika entwickelt wurden, bleibt die Verwendung von Aminoglykosiden ein wichtiges Instrument zur Bekämpfung schwerer Infektionen durch Enterokokken oder Streptokokken..
Gentamicin, Amikacin, Tobramycin und Netilmicin haben ein breites Spektrum gegen aerobe gramnegative Bakterien. Kanamycin und Streptomycin haben ein engeres Spektrum und sollten nicht für verwendet werden Pseudomonas aeruginosa oder Serratia spp.
Gentamicin wird zusammen mit Penicillin oder Vancomycin bei Streptokokken und Enterokokken angewendet. Tobramycin ist es gewohnt Pseudomonas aeruginosa und einige Arten von Proteus. Bei nosokomialen Infektionen (Krankenhausinfektionen) werden Amikacin und Netilmicin verwendet.
Obwohl das Vorstehende die häufigsten Indikationen für Aminoglykoside darstellt, sollte die rationelle Verwendung dieser Antibiotika auf der Kultur und dem Antibiogramm des betreffenden Mittels beruhen..
Kontraindikationen
Aminoglykoside sind bei Patienten mit allergischen Reaktionen auf diese Antibiotika kontraindiziert. Sie sollten nicht bei Krankheiten angewendet werden, die durch resistente Keime verursacht werden. Sie sollten während der Schwangerschaft nicht angewendet werden, wenn es weniger toxische Alternativen gibt..
Es gibt relative Kontraindikationen bei Patienten mit Nierenerkrankungen und / oder Hörproblemen.
Verweise
- N. Boussekey & S. Alfandari (2007). Aminoglycoside. EMV-Vertrag der Medizin, elf(1), 1-4.
- Während Mangoni, E., Grammatikos, A., Utili, R. & Falagas, M. E. (2009). Brauchen wir noch die Aminoglykoside?? Internationale Zeitschrift für antimikrobielle Wirkstoffe, 33(3), 201-205.
- Goodman und Gilman, A. (2001). Die pharmakologische Basis von Therapeutika. Zehnte Ausgabe. McGraw-Hill
- Kotra, L. P., Haddad, J. & Mobashery, S. (2000). Aminoglykoside: Perspektiven auf Wirk- und Resistenzmechanismen und Strategien zur Resistenzbekämpfung. Antimikrobielle Mittel und Chemotherapie, 44(12), 3249 & ndash; 3256.
- Meyers, F.H., Jawetz, E., Goldfien, A. & Schaubert, L.V. (1978). Überprüfung der medizinischen Pharmakologie. Lange Medical Publications.
- Palomino, J. und Pachon, J. (2003) Aminoglycosides, Infectious Diseases and Clinical Microbiology 21 (2), 105-115.
- Rodríguez-Julbe, M.C., Ramírez-Ronda, C.H., Arroyo, E., Maldonado, G., Saavedra, S., Meléndez, B., ... & Figueroa, J. (2004). Antibiotika bei älteren Erwachsenen. Zeitschrift für Gesundheitswissenschaften in Puerto Rico, 2. 3(1).


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.