
Struktur, Eigenschaften, Synthese und Verwendung von Isopropylalkohol
Das Isopropylalkohol oder Isopropanol ist eine organische Verbindung mit der chemischen Formel CH3CHOHCH3 oder (CH3)zweiCHOH. Es gehört zu einer der wichtigsten Familien in der organischen Chemie: Alkohole, wie der Name schon sagt..
Es ist eine flüssige, farblose, stark riechende, flüchtige und brennbare chemische Verbindung. Es ist eine schwache Säure und Base gleichzeitig, ähnlich wie Wasser, abhängig vom pH-Wert der Lösung und / oder der Anwesenheit einer Säure oder einer Base, die stärker als diese ist. Dämpfe von Isopropylalkohol verursachen eine sehr leichte Reizung der Schleimhaut von Nase, Rachen und Augen..
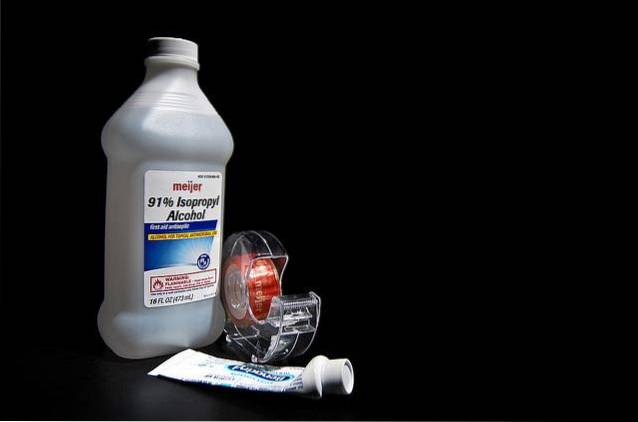
Isopropylalkohol wird als Hauptbestandteil in verschiedenen Produkten der Pharma-, Chemie-, Handels- und Haushaltsindustrie verwendet. Aufgrund seiner antimikrobiellen Eigenschaften wird es häufig als Antiseptikum auf Haut und Schleimhaut sowie als Desinfektionsmittel in inerten Materialien eingesetzt..
Es ist sehr nützlich als Lösungsmittel, da es eine geringe Toxizität aufweist, und es wird auch als Benzinadditiv verwendet..
Ebenso ist es der Rohstoff für die Synthese anderer organischer Verbindungen durch Substitution der funktionellen Hydroxylgruppe (OH). Auf diese Weise ist dieser Alkohol sehr nützlich und vielseitig, um andere organische Verbindungen zu erhalten; wie Alkoxide, Alkylhalogenide, unter anderen chemischen Verbindungen.
Artikelverzeichnis
- 1 Struktur von Isopropylalkohol oder Isopropanol
- 2 Physikalische und chemische Eigenschaften
- 2.1 Molekulargewicht
- 2.2 Aussehen
- 2.3 Geruch
- 2.4 Schmelzpunkt
- 2,5 Siedepunkt
- 2.6 Dichte
- 2.7 Löslichkeit
- 2,8 pKa
- 2.9 Basis konjugieren
- 2.10 Absorption
- 3 Nomenklatur
- 4 Synthese
- 5 Verwendungen
- 5.1 Zusammenfassend
- 5.2 Zur Reinigung
- 5.3 Antimikrobiell
- 5.4 Medizin
- 5.5 Lösungsmittel
- 6 Referenzen
Struktur von Isopropylalkohol oder Isopropanol
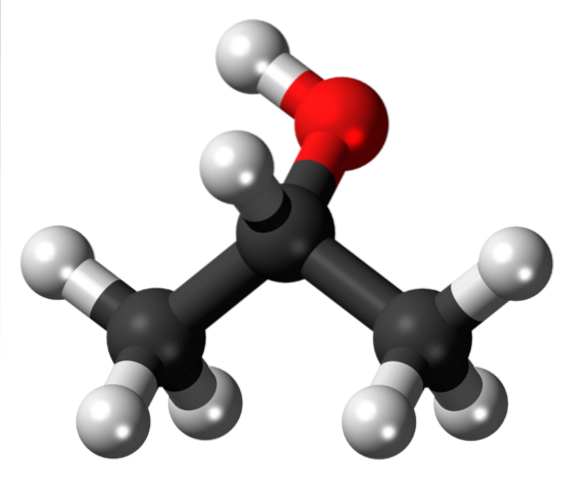
Das obere Bild zeigt die Struktur von Isopropylalkohol oder Isopropanol mit einem Modell von Kugeln und Balken. Die drei grauen Kugeln stellen die Kohlenstoffatome dar, aus denen die Isopropylgruppe besteht, die an eine Hydroxylgruppe gebunden ist (rote und weiße Kugeln)..
Wie alle Alkohole bestehen sie strukturell aus einem Alkan; in diesem Fall Propan. Dies verleiht Alkohol die Eigenschaft eines Lipophilen (Fähigkeit, Fette aufgrund seiner Affinität zu ihnen aufzulösen). Es ist an eine Hydroxylgruppe (-OH) gebunden, die der Struktur andererseits die hydrophile Eigenschaft verleiht.
Daher kann Isopropylalkohol Fett oder Flecken lösen. Es ist zu beachten, dass die -OH-Gruppe an den mittleren Kohlenstoff gebunden ist (2., dh an zwei andere Kohlenstoffatome), was zeigt, dass diese Verbindung ein sekundärer Alkohol ist.
Sein Siedepunkt ist niedriger als der von Wasser (82,6 ° C), was sich aus dem Propanskelett erklären lässt, das durch Londoner Dispersionskräfte kaum miteinander interagieren kann; niedriger als Wasserstoffbrücken (CH3)zweiCHO-H-H-O-CH (CH3)zwei.
Physikalische und chemische Eigenschaften
Molekulargewicht
60,10 g / mol.
Aussehen
Flüssig und farblos und brennbar.
Geruch
Starker Geruch
Schmelzpunkt
-89 ° C..
Siedepunkt
82,6 ° C..
Dichte
0,786 g / ml bei 20 ° C..
Löslichkeit
Es ist wasserlöslich und in organischen Verbindungen wie Chloroform, Benzol, Ethanol, Glycerin, Ether und Aceton löslich. Es ist in Salzlösungen unlöslich.
pKa
17
Basis konjugieren
(CH3)zweiCHO-
Absorption
Isopropylalkohol im sichtbaren ultravioletten Spektrum hat eine maximale Absorption bei 205 nm.
Nomenklatur
In der Nomenklatur der organischen Verbindungen gibt es zwei Systeme: das der gebräuchlichen Namen und das international standardisierte IUPAC-System..
Isopropylalkohol entspricht dem gebräuchlichen Namen, der mit dem Suffix -ico endet, dem das Wort Alkohol und der Name der Alkylgruppe vorangestellt sind. Die Alkylgruppe besteht aus 3 Kohlenstoffatomen, zwei Methylenden und dem im Zentrum, das an die -OH-Gruppe gebunden ist; Isopropylgruppe.
Isopropylalkohol oder Isopropanol hat andere Namen, wie unter anderem 2-Propanol, sec-Propylalkohol; Nach der IUPAC-Nomenklatur heißt es jedoch Propan-2-ol.
Nach dieser Nomenklatur handelt es sich zunächst um Propan, da die Kohlenstoffkette drei Kohlenstoffatome enthält oder aus diesen besteht.
Zweitens wird die Position der OH-Gruppe an der Kohlenstoffkette unter Verwendung einer Zahl angegeben; in diesem Fall ist es 2.
Der Name endet mit 'ol', charakteristisch für organische Verbindungen der Alkoholfamilie, da sie die Hydroxylgruppe (-OH) enthalten..
Der Name Isopropanol wird von der IUPAC aufgrund des Fehlens des Kohlenwasserstoff-Isopropans als falsch angesehen.
Synthese
Die chemische Synthesereaktion von Isopropylalkohol auf industrieller Ebene ist im Grunde eine Wasseradditionsreaktion; das heißt, Flüssigkeitszufuhr.
Das Ausgangsprodukt für die Synthese oder Gewinnung ist Propen, dem Wasser zugesetzt wird. Propen CH3-CH = CHzwei Es ist ein Alken, ein aus Erdöl gewonnener Kohlenwasserstoff. Durch Hydratation wird ein Wasserstoff (H) durch eine Hydroxylgruppe (OH) ersetzt..
Dem Alkenpropen wird in Gegenwart von Säuren Wasser zugesetzt, um Isopropanolalkohol herzustellen..
Es gibt zwei Möglichkeiten, es zu hydratisieren: die direkte und die indirekte, die unter polaren Bedingungen durchgeführt werden und Isopropanol erzeugen..
CH3-CH = CHzwei (Propen) => CH3CHOHCH3 (Isopropanol)
Bei der direkten Hydratation in der Gas- oder Flüssigphase wird Propen durch Säurekatalyse bei hohem Druck hydratisiert.
Bei der indirekten Hydratisierung reagiert Propen mit Schwefelsäure unter Bildung von Sulfatestern, die durch Hydrolyse Isopropylalkohol produzieren.
Isopropylalkohol wird auch durch Hydrieren von Aceton in der flüssigen Phase erhalten. Diesen Prozessen folgt eine Destillation, um den Alkohol vom Wasser zu trennen, wobei wasserfreier Isopropylalkohol mit einer Ausbeute von ungefähr 88% erzeugt wird..
Anwendungen
Isopropylalkohol hat auf chemischer Ebene ein breites Anwendungsspektrum. Es ist nützlich zur Herstellung anderer chemischer Verbindungen. Es hat zahlreiche Anwendungen auf industrieller Ebene, für Reinigungsgeräte, auf medizinischer Ebene, in Haushaltsprodukten und für kosmetische Zwecke..
Dieser Alkohol wird unter anderem in Parfums, Haarfärbemitteln, Lacken und Seifen verwendet, wie Sie weiter unten sehen werden. Seine Verwendung erfolgt hauptsächlich und grundsätzlich äußerlich, da sein Einatmen oder Verschlucken für Lebewesen sehr giftig ist.
Zusammenfassend
Daraus können Alkylhalogenide durch allgemeines Ersetzen von Brom (Br) oder Chlor (Cl), der funktionellen Gruppe Alkohol (OH), erhalten werden..
Durch einen Oxidationsprozess von Isopropylalkohol mit Chromsäure kann Aceton entstehen. Durch die Reaktion von Isopropylalkohol mit einigen Metallen wie Kalium kann es zu Alkoxiden kommen.
Zur Reinigung
Isopropylalkohol ist ideal für die Reinigung und Wartung von optischen Gläsern wie Linsen und elektronischen Geräten. Dieser Alkohol verdunstet schnell, hinterlässt keine Rückstände oder Spuren und zeigt bei seiner Anwendung oder äußerlichen Anwendung keine Toxizität.
Antimikrobiell
Isopropanol hat antimikrobielle Eigenschaften, bewirkt eine Denaturierung von Bakterienproteinen, löst unter anderem Lipoproteine der Zellmembran auf.
Als Antiseptikum wird Isopropylalkohol auf die Haut und die Schleimhäute aufgetragen und verdunstet schnell, wodurch ein kühlender Effekt entsteht. Es wird unter anderem für kleinere Operationen, das Einführen von Nadeln und Kathetern verwendet. Darüber hinaus wird es als Desinfektionsmittel für medizinische Instrumente verwendet.
Medizin
Abgesehen von seiner Verwendung als antimikrobielles Mittel wird es in Labors zur Reinigung, Konservierung von Proben und DNA-Extraktion benötigt..
Dieser Alkohol ist auch sehr nützlich bei der Herstellung von pharmakologischen Produkten. Isopropylalkohol wird mit Duftstoffen und ätherischen Ölen gemischt und in therapeutischen Verbindungen verwendet, um den Körper zu reiben.
Lösungsmittel
Isopropylalkohol hat die Eigenschaft, einige Öle, Naturharze, Gummis, Alkaloide, Ethylcellulose und andere chemische Verbindungen aufzulösen.
Verweise
- Carey, F. A. (2006). Organische Chemie Sechste Ausgabe. Mc Graw Hill Verlag
- Morrison, R. und Boyd, R. (1990). Organische Chemie. Fünfte Ausgabe. Editorial Addison-Wesley Iberoamericana.
- PubChem. (2019). Isopropylalkohol. Wiederhergestellt von: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Isopropylalkohol. Wiederhergestellt von: en.wikipedia.org
- Wade, L. (5. April 2018). Isopropylalkohol. Encyclopaedia Britannica. Wiederhergestellt von: britannica.com



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.