
Struktur, Eigenschaften, Nomenklatur der linearen Alkane, Beispiele
Das lineare Alkane sind gesättigte Kohlenwasserstoffe, deren allgemeine chemische Formel lautet n-C.nH.2n + 2. Da es sich um gesättigte Kohlenwasserstoffe handelt, sind alle ihre Bindungen einfach (C-H) und bestehen nur aus Kohlenstoff- und Wasserstoffatomen. Sie werden auch Paraffine genannt und unterscheiden sie von verzweigten Alkanen, die Isoparaffine genannt werden..
Diesen Kohlenwasserstoffen fehlen Äste und Ringe. Diese Familie organischer Verbindungen ähnelt mehr als Linien eher Ketten (geradkettiges Alkan); oder aus kulinarischer Sicht zu Spaghetti (roh und gekocht).

Rohe Spaghetti stellen den idealen und isolierten Zustand linearer Alkane dar, wenn auch mit einer ausgeprägten Tendenz zum Brechen; während diejenigen, die gekocht werden, unabhängig davon, ob sie al dente sind oder nicht, sich ihrem natürlichen und synergistischen Zustand nähern: einige interagieren mit anderen in einem Ganzen (zum Beispiel das Nudelgericht).
Diese Arten von Kohlenwasserstoffen kommen natürlicherweise in Erdgas und in Ölfeldern vor. Die leichtesten weisen Schmiereigenschaften auf, während sich die schweren wie unerwünschter Asphalt verhalten. löslich jedoch in Paraffinen. Sie dienen sehr gut als Lösungsmittel, Schmiermittel, Kraftstoffe und Asphalt.
Artikelverzeichnis
- 1 Struktur linearer Alkane
- 1.1 Gruppen
- 1.2 Längen Ihrer Ketten
- 1.3 Konformationen
- 2 Eigenschaften
- 2.1 Physisch
- 2.2 Wechselwirkungen
- 2.3 Stabilität
- 3 Nomenklatur
- 4 Beispiele
- 5 Referenzen
Struktur linearer Alkane
Gruppen
Es wurde erwähnt, dass die allgemeine Formel dieser Alkane C istnH.2n + 2. Diese Formel ist in der Tat für alle Alkane gleich, ob linear oder verzweigt. Der Unterschied dann in der n- das der Formel für Alkan vorausgeht, dessen Bezeichnung "normal" bedeutet.
Es wird später zu sehen sein, dass dies n- es ist nicht erforderlich für Alkane mit einer Kohlenstoffzahl von vier oder weniger (n ≤ 4).
Eine Linie oder Kette kann nicht aus einem einzigen Kohlenstoffatom bestehen, also Methan (CH4, n = 1). Wenn n = 2 ist, haben wir Ethan, CH3-CH3. Es ist zu beachten, dass dieses Alkan aus zwei Methylgruppen besteht, CH3, miteinander verbunden.
Durch Erhöhen der Anzahl der Kohlenstoffe, n = 3, erhält man das Alkanpropan CH3-CHzwei-CH3. Nun erscheint eine neue Gruppe, CHzwei, Methylen genannt. Egal wie groß das lineare Alkan ist, es wird immer nur zwei Gruppen haben: CH3 und CHzwei.
Länge ihrer Ketten
Wenn n oder die Anzahl der Kohlenstoffe im linearen Alkan zunimmt, gibt es in allen resultierenden Strukturen eine Konstante: Die Anzahl der Methylengruppen nimmt zu. Angenommen, lineare Alkane mit n = 4, 5 und 6:
CH3-CHzwei-CHzwei-CH3 ((n-Butan)
CH3-CHzwei-CHzwei-CHzwei-CH3 ((n-Pentan)
CH3-CHzwei-CHzwei-CHzwei-CHzwei-CH3 ((n-Hexan)
Die Ketten werden länger, weil sie ihren Strukturen CH-Gruppen hinzufügenzwei. Somit unterscheidet sich ein langes oder kurzes lineares Alkan um wie viele CHzwei trennt die beiden Endgruppen CH3. Alle diese Alkane haben nur zwei dieser CH3: am Anfang des Strings und am Ende. Wenn ich mehr hätte, würde dies das Vorhandensein von Zweigen bedeuten.
Ebenso kann das völlige Fehlen von CH-Gruppen gesehen werden, die nur in den Zweigen vorhanden sind oder wenn Substituentengruppen vorhanden sind, die an einen der Kohlenstoffe der Kette gebunden sind.
Die Strukturformel kann wie folgt zusammengefasst werden: CH3(CHzwei)n-2CH3. Versuchen Sie es anzuwenden und zu veranschaulichen.
Konformationen
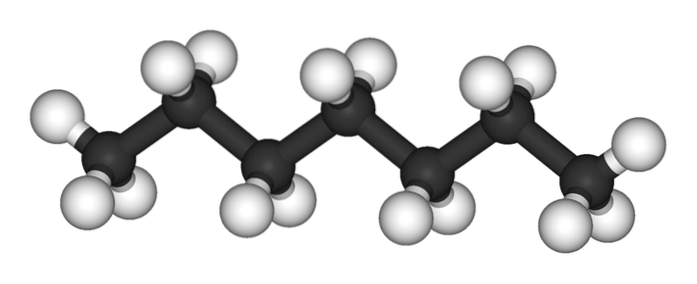
Einige lineare Alkane können länger oder kürzer sein als andere. In diesem Fall kann n einen Wert von 2 a ∞ haben; das heißt, eine Kette, die aus unendlichen CH-Gruppen bestehtzwei und zwei CH-Gruppen3 Terminals (theoretisch möglich). Es werden jedoch nicht alle Zeichenfolgen im Raum auf die gleiche Weise "untergebracht"..
Hier entstehen die strukturellen Konformationen von Alkanen. Was schulden sie? Zur Rotierbarkeit der CH-Bindungen und ihrer Flexibilität. Wenn sich diese Glieder um eine Kernachse drehen oder drehen, beginnen sich die Ketten zu biegen, zu falten oder zu wickeln, wobei sie sich von ihrer ursprünglichen linearen Charakteristik entfernen..
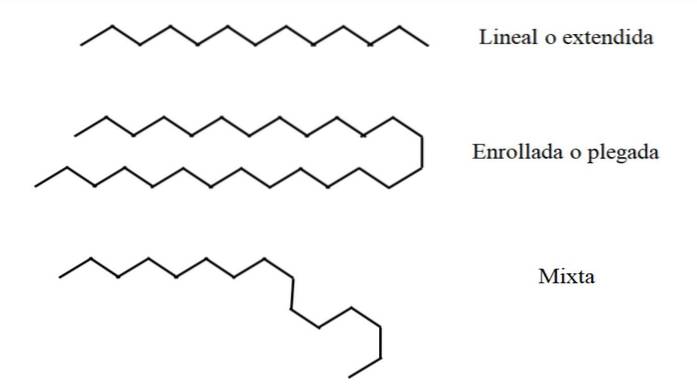
Linear
Im oberen Bild ist beispielsweise oben eine Kette mit dreizehn Kohlenstoffatomen dargestellt, die linear oder verlängert bleibt. Diese Konformation ist ideal, da angenommen wird, dass die molekulare Umgebung die räumliche Anordnung der Atome in der Kette minimal beeinflusst. Nichts stört sie und sie muss sich nicht beugen.
Aufgerollt oder gefaltet
In der Bildmitte erfährt die 27-Kohlenstoff-Kette eine äußere Störung. Um "bequemer" zu sein, dreht die Struktur ihre Glieder so, dass sie sich auf sich selbst faltet. genau wie eine lange Spaghetti.
Computerstudien zeigten, dass die maximale Anzahl von Kohlenstoffen, die eine lineare Kette haben kann, n = 17 ist. Ab n = 18 ist es unmöglich, dass sie sich nicht zu biegen oder zu wickeln beginnt.
Gemischt
Wenn die Kette sehr lang ist, können Bereiche der Kette linear bleiben, während andere gebogen oder gewickelt wurden. Von allen ist dies vielleicht die der Realität am nächsten kommende Konformation.
Eigenschaften
Körperlich
Als Kohlenwasserstoffe sind sie im Wesentlichen unpolar und daher hydrophob. Dies bedeutet, dass sie sich nicht mit Wasser mischen können. Sie sind nicht sehr dicht, weil ihre Ketten zu viele leere Räume zwischen ihnen lassen.
Ebenso reichen ihre physikalischen Zustände von gasförmig (für n < 5), líquidos (para n < 13) o sólidos (para n ≥ 14), y dependen de la longitud de la cadena.
Interaktionen
Die Moleküle linearer Alkane sind unpolar und daher sind ihre intermolekularen Kräfte vom Londoner Streutyp. Die Ketten (die wahrscheinlich eine gemischte Konformation annehmen) werden dann durch die Wirkung ihrer Molekularmassen und der augenblicklich induzierten Dipole ihrer Wasserstoff- und Kohlenstoffatome angezogen..
Aus diesem Grund steigen die Siede- und Schmelzpunkte der Kette in gleicher Weise an, wenn sie länger und damit schwerer wird..
Stabilität
Je länger die Kette ist, desto instabiler ist sie. Sie brechen im Allgemeinen ihre Glieder, um aus einer großen Kette kleinere Ketten zu machen. In der Tat ist dieser Prozess bekannt als knacken, hoch in der Ölraffination verwendet.
Nomenklatur
Um lineare Alkane zu benennen, fügen Sie einfach den n-Indikator vor dem Namen hinzu. Wenn n = 3 ist, wie bei Propan, kann dieses Alkan keine Verzweigung aufweisen:
CH3-CHzwei-CH3
Was nach n = 4, also mit n-Butan und den anderen Alkanen, nicht passiert:
CH3-CHzwei-CHzwei-CH3
ODER
(CH3)zweiCH-CH3
Die zweite Struktur entspricht Isobutan, das aus einem Strukturisomer von Butan besteht. Zur Unterscheidung kommt der n-Indikator ins Spiel. Und so kam es dass der n-Butan bezieht sich nur auf das lineare Isomer ohne Verzweigungen.
Je höher n ist, desto größer ist die Anzahl der Strukturisomere und desto wichtiger ist es, n- zu verwenden, um auf das lineare Isomer Bezug zu nehmen.
Zum Beispiel Oktan, C.8H.18 (C.8H.8 × 2 + 2) hat bis zu dreizehn Strukturisomere, da viele Verzweigungen möglich sind. Das lineare Isomer heißt jedoch: n-Oktan und seine Struktur ist:
CH3-CHzwei-CHzwei-CHzwei-CHzwei-CHzwei-CHzwei-CH3
Beispiele
Sie werden unten erwähnt und um einige lineare Alkane fertigzustellen:
-Ethan (C.zweiH.6): CH3CH3
-Propan (C.3H.8): CH3CHzweiCH3
-n-Heptan (C.7H.16): CH3(CHzwei)5CH3.
- n-Dean (C.10H.22): CH3(CHzwei)8CH3.
-n-Hexadecan (C.16H.3. 4): CH3(CHzwei)14CH3.
-n-Nonadecan (C.19H.40): CH3(CHzwei)17CH3.
-n-Eicosan (C.zwanzigH.42): CH3(CHzwei)18CH3.
- n-Hektan (C.100H.202): CH3(CHzwei)98CH3.
Verweise
- Carey F. (2008). Organische Chemie. (Sechste Ausgabe). Mc Graw Hill.
- Morrison, R. T. und Boyd, R., N. (1987). Organische Chemie. (5. Auflage). Editorial Addison-Wesley Interamericana.
- Graham Solomons T. W., Craig B. Fryhle. (2011). Organische Chemie. Amine. (10. Auflage). Wiley plus.
- Jonathan M. Goodman. (1997). Was ist das längste unverzweigte Alkan mit einer linearen globalen Mindestkonformation? J. Chem. Inf. Comput. Sci. 1997, 37, 5, 876 & ndash; 878.
- Garcia Nissa. (2019). Was sind Alkane? Studie. Wiederhergestellt von: study.com
- Herr Kevin A. Boudreaux. (2019). Alkane. Wiederhergestellt von: angelo.edu
- Liste der geradkettigen Alkene. [PDF]. Wiederhergestellt von: laney.edu
- Helmenstine, Anne Marie, Ph.D. (7. September 2018). Nennen Sie die ersten 10 Alkane. Wiederhergestellt von :oughtco.com
- Skurrile Wissenschaft. (20. März 2013). Geradkettige Alkane: Vorhersage von Eigenschaften. Wiederhergestellt von: quirkyscience.com
- Wikipedia. (2019). Höhere Alkane. Wiederhergestellt von: en.wikipedia.org


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.