
Kaliumiodid (KI) Struktur, Eigenschaften, Gewinnung, Verwendung, Risiken

Das Kaliumiodid ist eine anorganische Verbindung, die durch ein Kaliumion (K) gebildet wird+) und ein Iodidion (I.-). Seine chemische Formel lautet KI. Es ist ein weißer kristalliner Feststoff, ionischer Natur und in Wasser sehr gut löslich..
KI ermöglicht die Durchführung verschiedener chemischer Reaktionen und Analysen und dient zur Messung der Ozonmenge in der Atmosphäre. Wird auch in Infrarot (IR) -Analysegeräten verwendet.

Kaliumjodid wird dem üblichen Speisesalz zugesetzt, um Jodmangel bei Menschen zu verhindern, da dies ein ernstes Gesundheitsproblem sein kann.
Es wird als Expektorans verwendet, da es dem Schleim hilft, leicht von den Atmungskanälen nach außen zu fließen. Es wird auch zur Behandlung einiger Pilzinfektionen und in einigen Kosmetika verwendet.
Es wird von Tierärzten verwendet, um Tiere von ähnlichen Problemen wie Menschen wie Husten und Hautinfektionen zu heilen. Es wird sogar in sehr geringen Mengen dem Tierfutter zugesetzt.
Artikelverzeichnis
- 1 Struktur
- 2 Nomenklatur
- 3 Eigenschaften
- 3.1 Physikalischer Zustand
- 3.2 Molekulargewicht
- 3.3 Schmelzpunkt
- 3.4 Siedepunkt
- 3.5 Dichte
- 3.6 Löslichkeit
- 3,7 pH
- 3.8 Chemische Eigenschaften
- 3.9 Andere Eigenschaften
- 4 Erhalten
- 5 Verwendungen
- 5.1 Bei der Behandlung von Hyperthyreose
- 5.2 In anderen medizinischen Anwendungen
- 5.3 In veterinärmedizinischen Anwendungen
- 5.4 Zum Schutz der Schilddrüse in radioaktiven Notfällen
- 5.5 Bei Messungen von Ozon in der Atmosphäre
- 5.6 In verschiedenen Anwendungen
- 6 Risiken
- 7 Referenzen
Struktur
Kaliumiodid ist eine ionische Verbindung, die durch das Kaliumkation K gebildet wird+ und das Jodidanion I.-, daher ist die Bindung zwischen den beiden ionisch. Die Oxidationsstufe von Kalium beträgt +1 und die Wertigkeit von Jod beträgt -1.
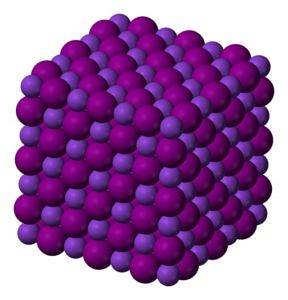
KI-Kaliumiodidkristalle sind kubisch.
Nomenklatur
- Kaliumiodid
- Kaliumiodid
Eigenschaften
Körperlicher Status
Farbloser bis weißer kristalliner Feststoff. Kubische Kristalle.
Molekulargewicht
166,003 g / mol
Schmelzpunkt
681 ºC
Siedepunkt
1323 ºC
Dichte
3,13 g / cm3
Löslichkeit
In Wasser sehr gut löslich: 149 g / 100 g Wasser bei 25 ° C. In Ethanol und Ether schwer löslich.
pH
Seine wässrigen Lösungen sind neutral oder alkalisch mit einem pH-Wert zwischen 7 und 9.
Chemische Eigenschaften
Leicht hygroskopisch in feuchter Luft.
Es ist in trockener Luft stabil. Licht und Feuchtigkeit beschleunigen seine Zersetzung und seine Farbe ändert sich aufgrund der Freisetzung kleiner Mengen Jod (I.zwei) und Jodate (IO3-).
Wässrige KI-Lösungen färben sich mit der Zeit ebenfalls gelb, ein wenig Alkali kann dies jedoch verhindern.
Diese Lösungen lösen Jod (I.zwei) KI geben3::
ich- + ichzwei → I.3-
Andere Eigenschaften
Es hat einen stark bitteren und salzigen Geschmack. Es ist nicht brennbar.
Erhalten
Kaliumiodid kann durch Erhitzen von Jod erhalten werden (I.zwei) in einer konzentrierten Lösung von Kaliumhydroxid (KOH):
3 I.zwei + 6 KOH → 5 KI + KIO3 + H.zweiODER
Die resultierende Iodat- und Iodidlösung wird erhitzt, um Wasser zu entfernen, zur Trockne reduziert, Holzkohle wird zugegeben und auf hohe Temperatur erhitzt. Kohle entnimmt dem Jodat Sauerstoff und oxidiert zu Kohlendioxid, wodurch Jodat zu Jodid reduziert wird:
2 KIO3 + C → 2 KI + 3 COzwei
Das erhaltene Kaliumiodid kann zur Reinigung umkristallisiert werden. Das heißt, es löst sich in Wasser wieder auf und wird dazu gebracht, wieder zu kristallisieren..
Anwendungen
Bei der Behandlung von Hyperthyreose
Kaliumiodid dient als zusätzliche Behandlung zusammen mit anderen Antithyreotika zur Behandlung von Hyperthyreose.
Hyperthyreose ist eine Krankheit, bei der die Schilddrüse unter anderem zu viel Schilddrüsenhormon produziert, darunter eine vergrößerte Schilddrüse, eine Gewichtsabnahme, ein schneller Herzschlag und Reizbarkeit..
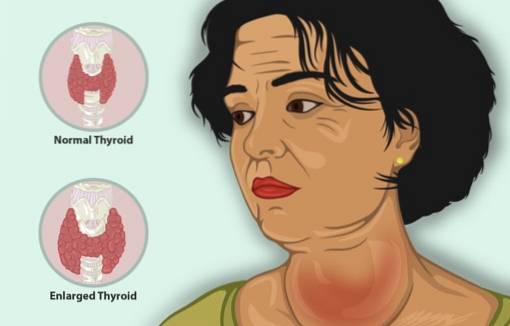
Bei Patienten mit Hyperthyreose reduziert KI die Symptome schnell, da es die Freisetzung von Schilddrüsenhormon hemmt.
Seine Auswirkungen auf die Schilddrüse sind: Verringerung der Anzahl der Blutgefäße in der Drüse, Straffung des Gewebes und Verringerung der Größe der Zellen.
Aus diesem Grund wird es als präoperative Behandlung angewendet, um die Involution oder Verkleinerung der Schilddrüse vor einer Schilddrüsenentfernung (Entfernung der Schilddrüse) zu induzieren, da dies diese Operation erleichtert..
In anderen medizinischen Anwendungen
Kaliumiodid hat schleimlösende Eigenschaften, da es die Sekretion von Atemflüssigkeiten erhöht, was zu einer Abnahme der Schleimviskosität führt..

Es wird zur Behandlung von Erythema nodosum angewendet, einer schmerzhaften Schwellung der Beine, in der sich rote Knötchen bilden, und einer Temperaturerhöhung.
Es ist ein Antimykotikum. Es ermöglicht die Behandlung von Sporotrichose, einer durch einen Pilz verursachten Hautinfektion. Diese Krankheit tritt bei Menschen auf, die mit Pflanzen und Erde arbeiten, wie z. B. Bauern und Gärtner..
Es wird auch zur Behandlung von Jodmangel oder zur Vermeidung von Jodmangel verwendet und daher Tafelsalz oder essbarem Salz (Natriumchlorid NaCl) als Jodquelle und manchmal in Trinkwasser zugesetzt.
In veterinärmedizinischen Anwendungen
Kaliumiodid wird Tieren als Antitussivum verabreicht, um die Flüssigkeiten der Atemwege zu erhöhen und zu verflüssigen, bei chronischem Bronchialhusten sowie bei Rheuma und als entzündungshemmendes Mittel.
Es wird auch zur Mykose (Pilzinfektion) von Tieren, zur Verringerung des Juckreizes und zur chronischen Vergiftung mit Blei oder Quecksilber eingesetzt.
Beim Schutz der Schilddrüse in radioaktiven Notfällen
Kaliumiodid hat Schilddrüsenschutzeigenschaften für den Fall, dass die Person nuklearer Strahlung ausgesetzt war.
KI überflutet die Schilddrüse mit nicht radioaktivem Jod und blockiert so die Aufnahme radioaktiver Moleküle und die Absorption von radioaktivem Jod, wodurch die Schilddrüse vor Krebs geschützt wird, den Strahlung verursachen kann..
Bei Messungen von Ozon in der Atmosphäre
Ozongas (O.3) können in der Atmosphäre mit Elektrolysezellen gemessen werden, die Ozonsonden genannt werden und von Radiosondenballons getragen werden.
Diese Elektrolysezellen enthalten eine KI-Kaliumiodidlösung. Zellen befinden sich zunächst im chemischen und elektrischen Gleichgewicht.
Wenn eine Ozonluftprobe (O.3) dringt in eine der Zellen ein, das Gleichgewicht wird unterbrochen, weil folgende Reaktion auftritt:
2 KI + O.3 + H.zweiO → I.zwei + ODERzwei + 2 KOH
Diese Reaktion erzeugt einen elektrischen Strom, der zwischen den Zellen fließt..
Die Menge des erzeugten elektrischen Stroms wird kontinuierlich durch Funkwellen zu einer Station am Boden übertragen. Auf diese Weise wird das Ozonprofil vom Boden bis zur Höhe des Balls erhalten..

In verschiedenen Anwendungen
Kaliumiodid ermöglicht auch:
- Eliminierung von freien Radikalen wie dem Hydroxylradikal OH.
- Die Herstellung von fotografischen Emulsionen, um Silber auszufällen.
- Verbessern Sie das Tierfutter, indem Sie es in Mikromengen hinzufügen.
- Desodorieren Sie Viehdung.
- Übertragen Sie das Licht des Infrarotspektrums in IR-Analysegeräten.
- Führen Sie bestimmte chemische Reaktionen und Analysen in Chemielabors durch.
- Verwenden Sie es in Körperpflegeprodukten.
- Führen Sie eine Umweltverschmutzungsanalyse durch.
Risiken
Einige Menschen, die empfindlich auf Jodide reagieren, sollten es mit Vorsicht einnehmen, da es Jodismus oder chronische Jodvergiftungen verursachen kann, z. B. Menschen mit einer Autoimmunerkrankung der Schilddrüse.
Menschen mit Tuberkulose oder akuter Bronchitis sollten ebenfalls vorsichtig sein.
KI kann eine Erweichung der Speicheldrüsen verursachen, Mund oder Rachen verbrennen, unter anderem eine ungewöhnliche Zunahme des Speichelflusses, Zahnschmerzen und Zahnfleischentzündungen sowie einen metallischen Geschmack verursachen..
Es kann auch die Augen reizen und Wunden auf der Haut öffnen..
Verweise
- UNS. Nationalbibliothek für Medizin. (2019). Kaliumiodid. Von pubchem.ncbi.nlm.nih.gov wiederhergestellt.
- Kirk-Othmer (1994). Enzyklopädie der chemischen Technologie. Vierte Edition. John Wiley & Sons.
- Dean, J.A. (Editor). (1973). Langes Handbuch der Chemie. Elfte Ausgabe. McGraw-Hill Book Company.
- Valkovic, V. (2019). Dekontamination nach Strahlenexposition. Die empfindlichsten Körperteile. In Radioaktivität in der Umwelt (2. Auflage). Von sciencedirect.com wiederhergestellt.
- Smit, H.G.J. (2015). Chemie der Atmosphärenbeobachtungen für die Chemie (in situ). In der Encyclopedia of Atmospheric Sciences (2. Auflage). Von sciencedirect.com wiederhergestellt.
- Muralikrishna, I.V. und Manickam, V. (2017). Analysemethoden zur Überwachung der Umweltverschmutzung. Im Umweltmanagement. Von sciencedirect.com wiederhergestellt.
- Wallace, J.M. und Hobbs, P.V. (2006). Chemie der Atmosphäre 1. In Atmospheric Science (Second Edition). Von sciencedirect.com wiederhergestellt.



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.