
Svante August Arrhenius Biographie, Theorien, Beiträge, Werke

Svante August Arrhenius (1859-1927) war ein schwedischer Physiker und Chemiker, der weltweit für seine Arbeit auf dem Gebiet der elektrolytischen Dissoziation und anderer Theorien bekannt ist, die ihn zu einem Weltmarktführer in der wissenschaftlichen Forschung machten.
Er war der erste Schwede, der den Nobelpreis für Chemie erhielt, ein Verfasser wissenschaftlicher Texte und als Vater der Physik-Chemie anerkannt; übte Universitätsunterricht aus und veröffentlichte Hypothesen über den Ursprung des Lebens und die Bildung von Sternen und Kometen.
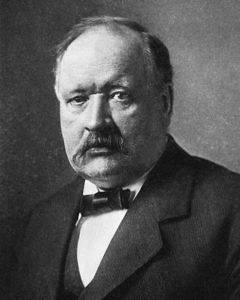
Experten sagen, dass Arrhenius 'Experimente ihrer Zeit voraus waren. Ein Beispiel hierfür war seine Forschung zu den Erregern der globalen Erwärmung des Planeten und seine Empfehlungen zur Vermeidung dieses ernsten Problems, das derzeit das Leben auf der Erde betrifft.
Artikelverzeichnis
- 1 Biografie
- 1.1 Kindheit und Studium
- 1.2 Neue Erfahrungen
- 2 Theorien
- 2.1 Theorie der elektrolytischen Dissoziation
- 2.2 Arrhenius-Gleichung
- 2.3 Arrhenius und Klimawandel
- 2.4 Der Ursprung des Lebens und andere Beiträge
- 3 Werke
- 4 Danksagung
- 5 Persönliches Leben
- 6 Referenzen
Biografie
Kindheit und Studium
Svante August Arrhenius wurde am 19. Februar 1859 auf einem rustikalen Bauernhof in Vik, Schweden, geboren. Sein Vater war Gustav Arrhenius und seine Mutter Carolina Christina Thunberg.
Schon in jungen Jahren stand er in Kontakt mit der akademischen Welt, da sein Onkel Johann Arrhenius Professor für Botanik und später Rektor der Landwirtschaftsschule in Ultuna war, während sein Vater als Landvermesser an der Universität von Uppsala arbeitete.
Mit dem Ziel, ihre wirtschaftliche Situation zu verbessern, zog die Familie 1860 nach Uppsala, nur ein Jahr nach der Geburt des kleinen Svante, der sich schon in jungen Jahren als Wunderkind erwies. Es wird angegeben, dass er bereits im Alter von drei Jahren alleine las und einfache mathematische Operationen löste.
Arrhenius studierte an der Uppsala Cathedral School, einem historisch angesehenen Campus, der 1246 gegründet wurde und den er 1876 mit hervorragenden Noten abschloss..
Mit 17 Jahren trat er in die Universität von Uppsala ein, wo er Mathematik, Physik und Chemie studierte. Fünf Jahre später zog er nach Stockholm, um unter Professor Erick Edlund (1819-1888) an der Königlich Schwedischen Akademie der Wissenschaften zu arbeiten..
Arrhenius half Edlund zunächst bei der Recherche, begann aber bald mit der Arbeit an seiner eigenen Doktorarbeit. Untersuchungen zur galvanischen Leitfähigkeit von Elektrolyten, die er 1884 an der Universität von Uppsala präsentierte.
Diese Forschung drehte sich um die Auflösung von Elektrolyten in wässrigen Lösungen und ihre Fähigkeit, positive und negative Ionen zu erzeugen, die Elektrizität leiten. Leider wurde die Theorie als fehlerhaft eingestuft, so dass die Forschung mit einer Mindestpunktzahl genehmigt und von ihren Klassenkameraden und Lehrern beanstandet wurde.
Neue Erfahrungen
Diese Ablehnung durch die wissenschaftliche Gemeinschaft hielt Arrhenius nicht auf, der Kopien seiner Dissertation an renommierte Wissenschaftler wie Rudolf Clausius (1822-1888), Julios Lothar Meyer (1830-1895), Wilhem Ostwald (1853-1932) und Jacobus Henricus van 't sandte Hoff. (1852-1811).
Arrhenius trainierte weiter und lernte von seinen Kollegen. Er erhielt ein Stipendium der Akademie der Wissenschaften, das es ihm ermöglichte, in Labors führender Forscher in Riga, Graz, Amsterdam und Leipzig zu reisen und zu arbeiten.
Er begann seine Tätigkeit als Lehrer im Jahr 1891 und unterrichtete Physik an der Universität Stockholm. Sechs Jahre später wurde er zum Rektor dieses Hochschulcampus ernannt.
Theorien
Theorie der elektrolytischen Dissoziation
Während seiner Zeit als Universitätsprofessor arbeitete Arrhenius weiter an der Erforschung der in seiner Doktorarbeit diskutierten wässrigen Lösungen. Diese neue Überprüfung seiner Daten und Experimente diente als Grundlage für die Präsentation seiner Theorie der elektrolytischen Dissoziation im Jahr 1889..
Arrhenius behauptete, ein Elektrolyt sei eine Substanz, die in einer wässrigen Lösung einen elektrischen Strom leiten könne.
Nach dem Auflösen dissoziierten diese Elektrolyte und erzeugten eine positive und eine negative Ladung, die er Ionen nannte. Der positive Teil dieser Ionen wurde als Kation und negatives Anion bezeichnet.
Er erklärte, dass die Leitfähigkeit einer Lösung von der Menge der konzentrierten Ionen in der wässrigen Lösung abhängt..
Die Lösungen, in denen diese Elektrolyte ionisiert wurden, wurden abhängig von der Art der negativen oder positiven Ladung, die sie bildeten, als Säuren oder Basen klassifiziert..
Diese Ergebnisse ermöglichten die Interpretation des bis dahin bekannten Verhaltens von Säuren und Basen und erklärten eine der wichtigsten Eigenschaften von Wasser: seine Fähigkeit, Substanzen aufzulösen.
Diese Forschung machte ihn 1903 des Nobelpreises für Chemie würdig, der ihn unter seinen in- und ausländischen Kollegen verankerte..
Zwei Jahre nach Erhalt dieser wichtigen Auszeichnung übernahm er die Leitung des kürzlich eingeweihten Nobel-Instituts für Physikalische Chemie, eine Position, die er bis zu seiner Pensionierung 1927 innehatte.
Arrhenius-Gleichung
Arrhenius schlug 1889 eine mathematische Formel vor, um die Abhängigkeit zwischen der Temperatur und der Geschwindigkeit einer chemischen Reaktion zu überprüfen.
Eine ähnliche Studie wurde 1884 vom Wissenschaftler van't Hoff initiiert, aber es war Arrhenius, der eine physikalische Begründung und die Interpretation der Gleichung hinzufügte und einen praktischeren Ansatz für diesen wissenschaftlichen Beitrag bot..
Ein Beispiel für diese Studie kann im Alltag beobachtet werden, wenn Lebensmittel im Kühlschrank gelagert werden, wo niedrige Temperaturen eine langsamere chemische Reaktion ermöglichen, die zu einer Verschlechterung führt, und daher für einen längeren Verzehr geeignet sind..
Die Arrhenius-Gleichung kann auf homogene Gasreaktionen in Lösung und auf heterogene Prozesse angewendet werden.
Arrhenius und Klimawandel
Vor mehr als hundert Jahren, als die globale Erwärmung nicht Gegenstand von Debatten und Bedenken war, begann Arrhenius bereits, Prognosen über die Zukunft des Lebens auf dem Planeten abzugeben..
1895 widmete er sich der Untersuchung des Zusammenhangs zwischen der Kohlendioxidkonzentration (CO)zwei) in der Atmosphäre und der Bildung von Gletschern.
Es kam zu dem Schluss, dass eine 50% ige Reduzierung von (COzwei) könnte einen Temperaturabfall des Planeten um 4 oder 5 ° C bedeuten, der eine massive Abkühlung erzeugen könnte, ähnlich der der Eiszeiten, durch die die Erde gegangen ist.
Auf der anderen Seite, wenn diese CO-Wertezwei erhöht um 50%, würde ein umgekehrtes Ergebnis auftreten, ein Temperaturanstieg zwischen 4 oder 5 ° C, der eine abnormale Erwärmung verursachen würde, mit verheerenden Folgen für das Erdklima.
Arrhenius stellte auch fest, dass fossile Brennstoffe und die unaufhörliche industrielle Aktivität des Menschen die Hauptursachen für diesen Anstieg der CO-Konzentration sindzwei atmosphärisch.
Seine Berechnungen sagten eine nachgewiesene Auswirkung auf das natürliche Gleichgewicht unseres Planeten voraus und machten Arrhenius zum ersten Mann, der formelle Forschungen zu diesem Thema durchführte..
Der Ursprung des Lebens und andere Beiträge
Die Themen seines Interesses waren sehr vielfältig. Er bot Beiträge auf dem Gebiet der Kosmologie mit einer Theorie über die Entstehung von Kometen an, die den Druck der Sonnenstrahlung auf ihre Bildung zurückführte; Neben einer Theorie über die Entwicklung der Sterne.
Die Studie über den Ursprung des Lebens wurde von diesem Wissenschaftler nicht übersehen, der in seiner Theorie der Panspermie feststellte, dass der Keim des Lebens im gesamten Universum verstreut ist und nur die notwendigen Bedingungen für die Entwicklung benötigt.
Eine sehr moderne Theorie, wenn man berücksichtigt, dass Wissenschaftler derzeit das Vorhandensein von interplanetarem Material in auf die Erde gefallenen Meteoriten untersuchen und die Möglichkeit, dass diese als Vehikel für den ersten Funken des Lebens auf dem Planeten gedient haben.
Arrhenius erhielt während seines Lebens mehrere Stellenangebote aus anderen Ländern, zog es jedoch immer vor, in Schweden zu arbeiten. Als Ausnahme gilt die Zeit, in der er an der University of California in den USA gearbeitet hat und die sein Buch verlassen hat Immunchemie (1907).
Theaterstücke
Arrhenius zeichnete sich auch als produktiver Schriftsteller aus und veröffentlichte wissenschaftliche Werke und Reden..
- Theoretische Elektrochemie (1900).
- Abhandlung über kosmische Physik (1903).
- Theorie der Chemie, der Erde und des Universums (1906).
- Immunochemistry (1907).
- Welten in der Schöpfung: Die Evolution des Universums (1908).
- Quantitative Gesetze in der biologischen Chemie (1915).
- Das Schicksal der Sterne (1915).
- Chemie und modernes Leben (1915).
- Theorie der Lösungen (1918).
Einige Texte wurden ausschließlich für die eingehende Analyse des Studiums und der Praxis der Chemie verfasst, aber er machte auch mehrere Veröffentlichungen einer Erzählung nicht nur für die akademische Gemeinschaft, sondern auch für die breite Öffentlichkeit leicht zu interpretieren..
Danksagung
Die herausragendste Auszeichnung, die Arrhenius erhielt, war zweifellos der Nobelpreis für Chemie, den er 1903 dank seiner Theorie der elektrolytischen Dissoziation erhielt und der ihn zum ersten Schweden machte, der eine solche Auszeichnung verdiente..
1902 verlieh ihm die Royal Society of London (Royal Society) die Davy-Medaille, und dieselbe Institution ernannte ihn 1911 zum ausländischen Mitglied.
Im selben Jahr erhielt er als erster die von der American Chemical Society verliehene Willard Gibbs-Medaille.
1914 erhielt er die Faraday-Medaille des britischen Instituts für Physik sowie eine Reihe von Auszeichnungen und akademischen Ehrentiteln, die von etwa zehn angesehenen europäischen Universitäten angeboten wurden.
Zu seinen Ehren wurden auch der Mondkrater Arrhenius und der Arrhenius-Krater des Mars benannt.
Persönliches Leben
Historiker behaupten, Arrhenius sei von großem menschlichen Geist gewesen. Tatsächlich bemühte er sich während des Ersten Weltkriegs, Wissenschaftlern, die zu Kriegsgefangenen gemacht worden waren, zu helfen und sie zu repatriieren..
Er heiratete zweimal, 1884, mit Sofia Rudbeck, seiner Schülerin und Assistentin, mit der er einen Sohn hatte. Einundzwanzig Jahre nach seiner ersten Ehe heiratete er María Johansson mit drei Kindern..
Er arbeitete unermüdlich bis zu seinem Tod in Stockholm am 2. Oktober 1927 im Alter von 68 Jahren..
Verweise
- Bernardo Herradon. (2017). Arrhenius, einer der Väter der modernen Chemie. Entnommen aus principia.io
- Elisabeth Crawford. (2015). Svante Arrhenius, schwedischer Chemiker. Entnommen von Britannica.com
- Miguel Barral. (2019). Svante Arrhenius, Der Mann, der den Klimawandel vorausgesehen hat. Entnommen aus bbvaopenmind.com
- Miguel G. Corral (2011). Meteoriten könnten den Beginn des Lebens zur Explosion bringen. Entnommen aus elmundo.es
- Svante Arrhenius. Entnommen aus newworldencyclopedia.org
- Francisco Armijo de Castro. (2012). Hundert Jahre mineralisch-medizinisches Wasser. Zwei Hydrologen: Antoine Lavoisier und Svante Arrhenius. Entnommen aus magazine.ucm.es



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.