
Materialsystemklassifikation, Phasen und Beispiele
Das Materialsysteme Sie sind alle diejenigen, die aus Materie bestehen und vom Rest des zu untersuchenden Universums isoliert sind. Materie ist überall und gibt den Wahrnehmungen des täglichen Lebens Form und wahre Bedeutung. Wenn Sie jedoch einen Teil der Materie untersuchen möchten, wird ihre Umgebung verachtet und wir sprechen von einem materiellen System..
Sie sind sehr variabel, da es reine und Verbundwerkstoffe sowie unterschiedliche Aggregatzustände und -phasen gibt. Wie definiert man die Grenze zwischen dem Materialsystem und seiner Umgebung? Es hängt alles von den Variablen ab, die berücksichtigt werden. In der Abbildung unten könnte beispielsweise jeder Süßigkeitenmarmor das untersuchte System sein..

Wenn jedoch die Farbvariable berücksichtigt werden soll, müssen alle Murmeln im Automaten berücksichtigt werden. Da die Maschine nicht von Interesse ist, ist dies die Umgebung der Murmeln. Das Materialsystem des Beispiels ergibt sich somit aus der Masse der Murmeln und ihren Eigenschaften (Kaugummi, Minze usw.)..
Chemisch sind Materialsysteme jedoch definiert als jede reine Substanz oder eine Mischung davon, die nach ihren physikalischen Aspekten klassifiziert ist..
Artikelverzeichnis
- 1 Klassifizierung
- 1.1 Homogenes Materialsystem
- 1.2 Heterogenes Materialsystem
- 2 Phasen
- 2.1 Phasendiagramm
- 3 Beispiele
- 4 Referenzen
Einstufung
Homogenes Materialsystem
Die zu untersuchende Materie kann ein einheitliches Erscheinungsbild aufweisen, bei dem ihre Eigenschaften unabhängig von der zu analysierenden Probe konstant bleiben. Mit anderen Worten: Diese Art von System zeichnet sich dadurch aus, dass auf den ersten Blick nur eine Phase der Materie vorliegt.
Reine Substanz und Verbindungen
Wenn eine reine Substanz analysiert wird, wird festgestellt, dass die physikochemischen Eigenschaften in den gleichen Werten und Ergebnissen übereinstimmen, selbst wenn viele Proben entnommen werden (und in verschiedenen geografischen Gebieten)..
Wenn beispielsweise eine Kalziumprobe mit einer aus Asien, Europa, Afrika und Amerika verglichen würde, hätten sie alle die gleichen Eigenschaften. Das gleiche würde passieren, wenn eine Probe von reinem Kohlenstoff entnommen würde.
Andererseits manifestiert eine reine Verbindung auch das oben erwähnte. Wenn garantiert wäre, dass ein Schiefer aus einem einzigen Material besteht, würde er als homogenes Materialsystem eingestuft.
Dies tritt jedoch bei einer Mineralprobe nicht auf, da sie im Allgemeinen Verunreinigungen von anderen assoziierten Mineralien enthält und in diesem Fall ein heterogenes Materialsystem ist. Ebenso fallen diese Materialsysteme wie Bäume, Steine, Berge oder Flüsse in die letztere Klassifikation..
Auflösung
Handelsüblicher Essig ist eine 5% ige wässrige Essigsäurelösung. Das heißt, 5 ml reine Essigsäure werden in 100 ml Wasser gelöst. Es sieht jedoch wie eine transparente Flüssigkeit aus, obwohl es sich in Wirklichkeit um zwei reine Verbindungen (Wasser und Essigsäure) handelt.
Heterogenes Materialsystem
Im Gegensatz zum homogenen System sind in dieser Systemklasse weder das Aussehen noch die Eigenschaften konstant und während ihrer gesamten Ausdehnung unregelmäßig..
Darüber hinaus kann es physikalischen oder chemischen Trenntechniken unterzogen werden, aus denen Phasen extrahiert werden, die jeweils als homogenes System betrachtet werden..
Phasen
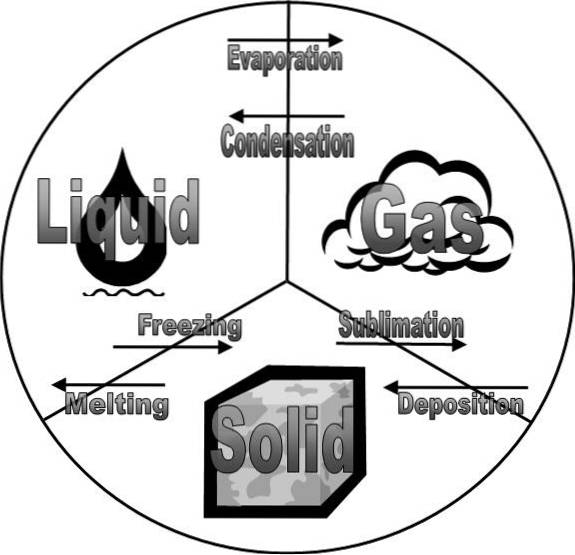
Das obere Bild zeigt die Zustände der Materie und ihre Veränderungen. Diese sind eng mit den Phasen der Materie verbunden, da sie, obwohl sie gleich sind, einige subtile Unterschiede aufweisen..
In diesem Fall sind die Phasen eines Materialsystems fest, flüssig und gasförmig. Mit anderen Worten, für bestimmte zu analysierende Stoffe kann jede der vorherigen Phasen übernommen werden.
Da die Wechselwirkungen in Festkörpern jedoch sehr stark sind und von Variablen wie Druck und Temperatur abhängen, kann ein System unterschiedliche feste Phasen aufweisen oder nicht.
Beispielsweise hat Verbindung X, die bei Raumtemperatur fest ist, Phase I; Wenn der Druck jedoch sehr hoch ist, ordnen sich seine Moleküle kompakter um, und dann tritt ein Übergang von Phase I zu fester Phase II auf..
Es gibt sogar andere Phasen wie III und IV, die sich bei unterschiedlichen Temperaturen von II ableiten. Somit kann das homogene Materialsystem von X einer scheinbaren festen Phase bis zu vier feste Phasen annehmen: I, II, III und IV.
Bei flüssigen und gasförmigen Systemen können die Moleküle in diesen Materiezuständen im Allgemeinen nur eine einzige Phase annehmen. Mit anderen Worten, es gibt möglicherweise keine Gasphase I und keine Gasphase II..
Phasendiagramm
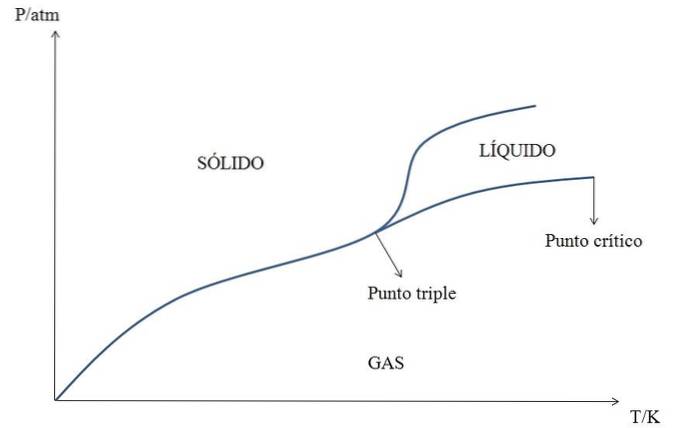
Es gibt viele Phasendiagramme: einige für eine einzelne Verbindung oder Substanz (wie im Bild oben) und andere für binäre Systeme (z. B. ein Salz in Wasser) oder ternäre Systeme (drei Komponenten)..
Das „einfachste“ von allen ist das Phasendiagramm für einen Stoff. Somit wird für die hypothetische Substanz Y ihre Phase als Funktion von Druck (y-Achse) und Temperatur (x-Achse) dargestellt..
Bei niedrigen Drücken ist es ein Gas, unabhängig von seiner Temperatur. Bei Erhöhung des Drucks wird Y-Gas jedoch in festem Y abgeschieden.
Bei Temperaturen über dem kritischen Punkt Y kondensiert Gas jedoch zu Flüssigkeit Y, und wenn der Druck ebenfalls erhöht wird (man steigt vertikal durch das Diagramm auf), verfestigt sich die Flüssigkeit.
Jede Linie repräsentiert das Gleichgewicht zwischen den beiden Phasen, die sie trennt: Festgas, Flüssiggas, Fest-Flüssig, Flüssig-Fest und Fest-Flüssig-Gas am Tripelpunkt.
Zusätzlich wird vom kritischen Punkt Y aus keine physikalische Unterscheidung zwischen der Gasphase und der flüssigen Phase gezeigt: Sie bildet ein sogenanntes überkritisches Fluid..
Beispiele

- Ein Ballon ist ein Materialsystem, da sein Inhalt gasförmig ist und daher chemischer Natur ist; Wenn das Gas weniger dicht als Luft ist, steigt der Ballon in den Himmel.
- Das Wasser-Öl-Binärsystem besteht aus zwei Phasen: einer aus Wasser und einer logischerweise aus Öl. Die Menge von beiden ist das heterogene System, während die einzelnen Schichten homogene Systeme sind. Wenn Sie das Öl extrahieren möchten, müssen Sie eine Flüssig-Flüssig-Extraktion mit einem organischen und flüchtigen Lösungsmittel durchführen..
- Ein Fest-Fest-System kann aus einer Mischung von Weißzucker und Braunzucker bestehen. Hier macht der Farbunterschied zwischen den Kristallen diesen Fall zu einem heterogenen System.
- Meerwasser ist ein weiteres Beispiel für ein homogenes Materialsystem. Es besteht aus einer Lösung vieler Ionen, die für seinen charakteristischen salzigen Geschmack verantwortlich sind. Wenn eine Meerwasserprobe in einem Behälter verdampfen würde, würde sie weiße Salze darin sedimentieren..
Verweise
- Ein System und seine Umgebung. Abgerufen am 27. Mai 2018 von: chem.libretexts.org
- Antonio de Ulloa. Materialsysteme. [PDF]. Abgerufen am 27. Mai 2018 von: 2.educarchile.cl
- Daniel J. Berger. (2001). Abgerufen am 27. Mai 2018 von: bluffton.edu
- Das System und die Umgebung in der Chemie. Abgerufen am 27. Mai 2018 von: chemteam.info
- Helmenstine, Anne Marie, Ph.D. (6. Februar 2018). Offene Systemdefinition in der Chemie. Abgerufen am 27. Mai 2018 von :oughtco.com
- Glen Research Center. Phasen der Materie. Abgerufen am 27. Mai 2018 von: grc.nasa.gov
- Alison H. (15.09.2006). Ballonstart. Abgerufen am 28. Mai 2018 von: flickr.com



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.