
Verseifungsreaktion und erhältliche Substanzen

Das Verseifung ist die basische Hydrolyse eines Esters. Dies bedeutet, dass der Ester irreversibel mit einer Base (NaOH oder KOH) unter Bildung von Alkohol und Natrium- oder Kaliumcarboxylaten reagiert. Das Wort bedeutet "Seifenherstellung" und ist in der Tat eine der ältesten chemischen Reaktionen der Menschheit..
In babylonischer Zeit perfektionierten sie mit Hilfe von Asche aus Holz, Pflanzen und tierischen Fetten die Kunst der Seifenherstellung. Warum tierisches Fett? Der Grund dafür ist, dass es reich an Glycerintriestern (Triglyceriden) ist und Holzasche eine Quelle für Kalium ist, das Grundmetall.
Andernfalls wird die Reaktion mit einer geringeren Ausbeute fortgesetzt, die jedoch ausreicht, um die Auswirkungen auf Farben und einige Oberflächen widerzuspiegeln. Dies ist der Fall bei Ölfarben, bei denen die Pigmente mit Öl (Esterquelle) gemischt werden..
Artikelverzeichnis
- 1 Verseifungsreaktion
- 1.1 Mechanismus
- 1.2 Kinetik
- 2 Substanzen, die durch Verseifung erhalten werden können
- 2.1 Lösungsmittelwirkung von Seifen
- 3 Referenzen
Verseifungsreaktion
Mechanismus
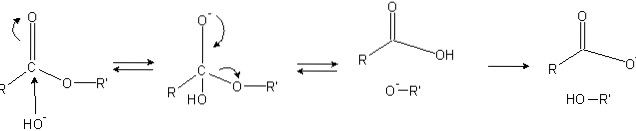
Ester haben eine Acylgruppe (O = C-R), die für nukleophile Angriffe wie OH anfällig ist-.
Da die Sauerstoffatome dem Kohlenstoffatom die Elektronendichte "stehlen", ist es teilweise positiv geladen, insbesondere bei Estern.
Folglich zieht diese positive Ladung negative Spezies an, die Elektronen zum Kohlenstoffatom beitragen können und einen nukleophilen Angriff verursachen (linke Seite des Bildes). Als Ergebnis wird ein tetraedrisches Intermediat gebildet (das zweite Molekül von links nach rechts).
Die negative Ladung des Sauerstoffs des tetraedrischen Zwischenprodukts ist das Produkt eines OH- Umgebung. Diese negative Ladung wird dann delokalisiert, um die Carbonylgruppe zu bilden, und dann die C-OR'-Bindung zum Brechen "gezwungen". Ebenso erzeugt diese Delokalisierung eine Carbonsäure RCOOH und ein Alkoxidion R'O-.
Da das Reaktionsmedium basisch ist, deprotoniert das Alkoxid schließlich ein Wassermolekül und die Carbonsäure reagiert mit einem anderen OH.- das Medium, das die Verseifungsprodukte erzeugt.
Kinetik
Die Geschwindigkeit der Verseifungsreaktion ist proportional zu den Konzentrationen der Reagenzien. Mit anderen Worten, wenn entweder die Konzentration des Esters (RCOOR ') oder der Base (NaOH) erhöht wird, läuft die Reaktion schneller ab.
Dies bedeutet auch Folgendes: Die Verseifungsrate ist relativ zum Ester erster Ordnung und relativ zur Base erster Ordnung. Das Obige kann mit der folgenden mathematischen Gleichung ausgedrückt werden:
Geschwindigkeit = k [RCOOR '] [NaOH]
Wobei k die Konstante oder der Geschwindigkeitskoeffizient ist, der bzw. der sich in Abhängigkeit von Temperatur oder Druck ändert; Das heißt, je höher die Wärme, desto höher die Verseifungsrate. Aus diesem Grund wird das Medium gekocht.
Da beide Reaktanten von der ersten kinetischen Ordnung sind, ist die Gesamtreaktion von der zweiten Ordnung.
Bei dem Verseifungsreaktionsmechanismus erfordert die Bildung des tetraedrischen Zwischenprodukts einen nukleophilen Angriff, an dem sowohl der Ester als auch die Base beteiligt sind..
Die Kinetik zweiter Ordnung spiegelt sich somit in dieser Tatsache wider, da sie in den bestimmenden (langsamen) Reaktionsschritt eingreift.
Substanzen, die durch Verseifung erhalten werden können

Die Hauptprodukte der Verseifung sind Alkohole und Salze von Carbonsäuren. In einem sauren Medium wird das jeweilige RCOOH erhalten, das durch Verseifung von Fetten und Ölen erhalten wird, die als Fettsäuren bekannt sind.
So bestehen Seifen aus Salzen der durch Verseifung hergestellten Fettsäuren. Kommst du mit welchen Kationen heraus? Sie können Na sein+, K.+, Mgzwei+, Vertrauen3+, usw.
Diese Salze sind wasserlöslich, werden jedoch durch die Einwirkung von NaCl, das der Mischung zugesetzt wird, ausgefällt, wodurch die Seife entwässert und von der wässrigen Phase getrennt wird. Die Verseifungsreaktion für ein Triglycerid ist wie folgt:
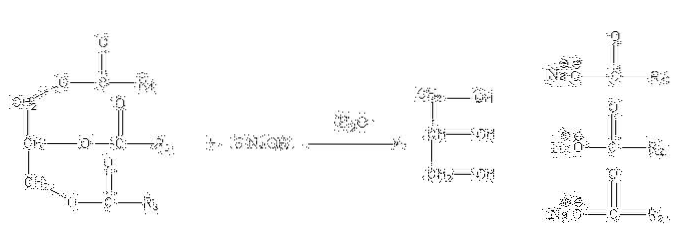
Glycerin ist das alkoholische "E" und Seife ist alle Salze der resultierenden Fettsäuren. Hier hat jede -R-Seitenkette unterschiedliche Längen und Ungesättigtheitsgrade. Folglich machen diese Ketten den Unterschied zwischen pflanzlichen Fetten und Ölen.
Der Schlüssel zur Herstellung von Seifen liegt dann in der Auswahl der besten Fette und Öle, genauer gesagt in der Auswahl verschiedener Triglyceridquellen..
Diese seifenweiße Masse kann Farbstoffe und andere organische Verbindungen in ihrer Struktur enthalten, was ihr angenehme Aromen und leuchtende Farben verleiht. Von hier aus wird das Spektrum der Möglichkeiten durch Kunst und Berufung in diesem Gewerbe gezähmt..
Die Verseifungsreaktion ist jedoch auch ein Syntheseweg von Carbonsäuren und Alkoholen, der nicht unbedingt mit Glycerin oder Seifen zu tun hat..
Beispielsweise erzeugt die basische Hydrolyse eines beliebigen Esters wie einfachem Ethylacetat Essigsäure und Ethanol..
Lösungsmittelwirkung von Seifen

Fettsäuresalze sind wasserlöslich, jedoch nicht so, wie Ionen solvatisiert werden. das heißt, umgeben von einer wässrigen Kugel. Bei Seifen verhindern ihre -R-Seitenketten theoretisch, dass sie sich in Wasser lösen.
Um dieser energetisch unangenehmen Position entgegenzuwirken, sind sie so ausgerichtet, dass diese Ketten in Kontakt kommen und einen unpolaren organischen Kern bilden, während die Polköpfe das Extrem (-COO) bilden- N / A+), interagieren mit Wassermolekülen und bilden eine "polare Hülle".
Das Obige ist im oberen Bild dargestellt, wo diese Art von Struktur gezeigt ist, die als Mizelle bekannt ist.
Die "schwarzen Schwänze" entsprechen den hydrophoben Ketten, die sich in einem organischen Kern verfangen, der durch die grauen Kugeln geschützt ist. Diese grauen Kugeln bilden den polaren Kürass, die -COO-Köpfe- N / A+.
Mizellen sind also Cluster (Agglomerationen) von Fettsäuresalzen. In diesen können sie Fett enthalten, das aufgrund seines unpolaren Charakters in Wasser unlöslich ist..
Wie haben sie das gemacht? Sowohl Fett- als auch -R-Ketten sind hydrophob, so dass beide eine hohe Affinität zueinander haben.
Wenn die Mizellen die Fette einschließen, interagiert das Wasser mit der polaren Hülle, wodurch die Löslichkeit der Seife ermöglicht wird. Ebenso sind die Mizellen negativ geladen, was zu gegenseitigen Abstoßungen führt und daher die Dispersion von Fett erzeugt..
Verweise
- Anne Marie Helmenstine, Ph.D. (03. Oktober 2017). Definition und Reaktion der Verseifung. Abgerufen am 24. April 2018 von :oughtco.com
- Francis A. Carey. Organische Chemie. Carbonsäuren. (sechste Ausgabe, Seiten 863-866). Mc Graw Hill.
- Graham Solomons T. W., Craig B. Fryhle. Organische Chemie. Lipide (10. Auflage, Seiten 1056-1058). Wiley plus.
- Wikipedia. (2018). Verseifung. Abgerufen am 24. April 2018 von: en.wikipedia.org
- Boyd C. (27. Februar 2015). Verstehe die Chemie und Geschichte der Seife. Abgerufen am 24. April 2018 von: chemservice.com
- Luca Laghi. (27. März 2007). Verseifung. Abgerufen am 24. April 2018 von: commons.wikimedia.org
- Amanda Crochet. (12. Mai 2015). Micelle (Graustufen). Abgerufen am 24. April 2018 von: commons.wikimedia.org


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.