
Bornitrid (BN) Struktur, Eigenschaften, Herstellung, Verwendung

Das Bornitrid Es ist ein anorganischer Feststoff, der durch Vereinigung eines Boratoms (B) mit einem Stickstoffatom (N) gebildet wird. Seine chemische Formel lautet BN. Es ist ein weißer Feststoff, der sehr widerstandsfähig gegen hohe Temperaturen ist und einen guten Wärmeleiter darstellt. Es wird zum Beispiel zur Herstellung von Labortiegeln verwendet.
Bornitrid (BN) ist gegen viele Säuren resistent, weist jedoch eine gewisse Angriffsschwäche durch Flusssäure und geschmolzene Basen auf. Es ist ein guter Isolator für Elektrizität.
Es wird in verschiedenen kristallinen Strukturen erhalten, von denen die wichtigsten hexagonal und kubisch sind. Die sechseckige Struktur ähnelt Graphit und ist rutschig, weshalb sie als Schmiermittel verwendet wird.
Die kubische Struktur ist fast so hart wie Diamant und wird zur Herstellung von Schneidwerkzeugen und zur Verbesserung der Zähigkeit anderer Materialien verwendet.
Bornitrid kann mikroskopisch kleine (extrem dünne) Röhrchen herstellen, die als Nanoröhrchen bezeichnet werden und medizinische Anwendungen haben, z. B. den Transport im Körper und die Freisetzung von Arzneimitteln gegen Krebstumoren..
Artikelverzeichnis
- 1 Struktur
- 2 Nomenklatur
- 3 Eigenschaften
- 3.1 Physikalischer Zustand
- 3.2 Molekulargewicht
- 3.3 Schmelzpunkt
- 3.4 Dichte
- 3.5 Löslichkeit
- 3.6 Chemische Eigenschaften
- 3.7 Andere physikalische Eigenschaften
- 4 Erhalten
- 5 Verwendungen
- 5.1 - Verwendung von BN-Dünnfilmen
- 5.2 - Verwendung von BN-Nanoröhren
- 6 Mögliche Toxizität von BN-Materialien
- 7 Referenzen
Struktur
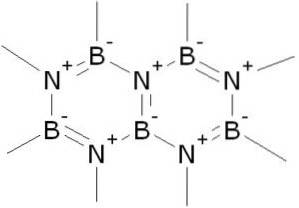
Bornitrid (BN) ist eine Verbindung, bei der Bor- und Stickstoffatome kovalent mit einer Dreifachbindung verbunden sind.
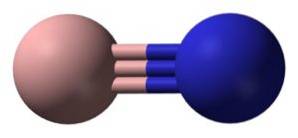
In fester Phase wird BN durch eine gleiche Anzahl von Bor- und Stickstoffatomen in Form von 6-gliedrigen Ringen gebildet..
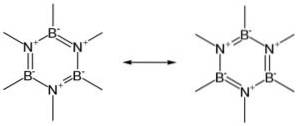
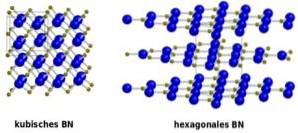
BN liegt in vier kristallinen Formen vor: hexagonal (h-BN) ähnlich wie Graphit, kubisch (c-BN) ähnlich wie Diamant, rhomboedrisch (r-BN) und Wurtzit (w-BN).
Die Struktur von h-BN ähnelt der von Graphit, dh es hat Ebenen hexagonaler Ringe mit alternierenden Bor- und Stickstoffatomen..
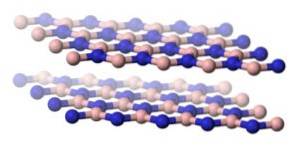
Zwischen den Ebenen von h-BN besteht ein großer Abstand, was darauf hindeutet, dass sie nur durch Van-der-Waals-Kräfte verbunden sind, bei denen es sich um sehr schwache Anziehungskräfte handelt und die Ebenen leicht übereinander gleiten können..
Aus diesem Grund fühlt sich h-BN nicht gut an..
Die Struktur von kubischem BN c-BN ist ähnlich wie bei Diamant.
Nomenklatur
Bornitrid
Eigenschaften
Körperlicher Status
Fettiger weißer Feststoff oder rutschig anzufassen.
Molekulargewicht
24,82 g / mol
Schmelzpunkt
Sublimiert bei ca. 3000 ºC.
Dichte
Hex BN = 2,25 g / cm3
Kubisches BN = 3,47 g / cm3
Löslichkeit
In heißem Alkohol schwer löslich.
Chemische Eigenschaften
Aufgrund der starken Bindung zwischen Stickstoff und Bor (Dreifachbindung) weist Bornitrid eine hohe Beständigkeit gegen chemische Angriffe auf und ist sehr stabil.
Es ist unlöslich in Säuren wie Salzsäure HCl, Salpetersäure HNO3 und Schwefelsäure H.zweiSW4. Es ist jedoch in geschmolzenen Basen wie Lithiumhydroxid LiOH, Kaliumhydroxid KOH und Natriumhydroxid NaOH löslich.
Es reagiert nicht mit den meisten Metallen, Gläsern oder Salzen. Reagiert manchmal mit Phosphorsäure H.3PO4. Es kann bei hohen Temperaturen der Oxidation widerstehen. BN ist an der Luft stabil, wird jedoch langsam durch Wasser hydrolysiert.
BN wird von Fluorgas F angegriffenzwei und durch Flusssäure HF.
Andere physikalische Eigenschaften
Es hat eine hohe Wärmeleitfähigkeit, eine hohe Wärmestabilität und einen hohen spezifischen elektrischen Widerstand, das heißt, es ist ein guter Isolator für Elektrizität. Hat eine große Oberfläche.
H-BN (hexagonales BN) fühlt sich ähnlich wie Graphit weich an.
Beim Erhitzen von h-BN auf erhöhte Temperatur und erhöhten Druck wandelt es sich in die kubische Form c-BN um, die extrem hart ist. Nach einigen Quellen ist es in der Lage, den Diamanten zu kratzen.
Materialien auf BN-Basis können anorganische Verunreinigungen (wie Schwermetallionen) und organische Verunreinigungen (wie Farbstoffe und Arzneimittelmoleküle) absorbieren..
Sorption bedeutet, dass es mit ihnen interagiert und sie adsorbieren oder absorbieren kann.
Erhalten
H-BN-Pulver wird durch die Reaktion zwischen Bortrioxid B hergestelltzweiODER3 oder Borsäure H.3BO3 mit NH Ammoniak3 oder mit Harnstoff NHzwei(CO) NHzwei unter Stickstoffatmosphäre N.zwei.
BN kann auch durch Umsetzen von Bor mit Ammoniak bei einer sehr hohen Temperatur erhalten werden..
Eine andere Art, es zuzubereiten, ist aus Diboran B.zweiH.6 und NH-Ammoniak3 unter Verwendung eines Inertgases und hoher Temperaturen (600-1080 ° C):
B.zweiH.6 + 2 NH3 → 2 BN + 6 H.zwei
Anwendungen
H-BN (hexagonales Bornitrid) hat aufgrund seiner Eigenschaften eine Vielzahl wichtiger Anwendungen:
-Als Festschmierstoff
-Als Zusatz für Kosmetika
-In elektrischen Hochtemperaturisolatoren
-In Tiegeln und Reaktionsgefäßen
-In Formen und Verdunstungsgefäßen
-Zur Wasserstoffspeicherung
-In der Katalyse
-Adsorption von Schadstoffen aus Abwasser
Es wird kubisches Bornitrid (c-BN) verwendet, dessen Härte fast der von Diamant entspricht:
-In Schneidwerkzeugen zur Bearbeitung von harten Eisenwerkstoffen wie Hartlegierungen aus Stahl, Gusseisen und Werkzeugstählen
-Verbesserung der Härte und Verschleißfestigkeit anderer harter Materialien wie bestimmter Keramiken für Schneidwerkzeuge.

- Verwendung von BN-Dünnfilmen
Sie sind sehr nützlich in der Technologie von Halbleiterbauelementen, die Komponenten elektronischer Geräte sind. Sie dienen zum Beispiel:
-Flache Dioden herstellen; Dioden sind Geräte, mit denen Elektrizität nur in eine Richtung zirkulieren kann
-In Metall-Isolator-Halbleiter-Speicherdioden wie Al-BN-SiOzwei-Ja
-In integrierten Schaltkreisen als Spannungsbegrenzer
-Erhöhung der Härte bestimmter Materialien
-Zum Schutz einiger Materialien vor Oxidation
-Erhöhung der chemischen Stabilität und der elektrischen Isolierung vieler Arten von Geräten
-In Dünnschichtkondensatoren

- Verwendung von BN-Nanoröhren
Nanoröhren sind Strukturen, die auf molekularer Ebene wie Röhren geformt sind. Es sind Röhren, die so klein sind, dass sie nur mit speziellen Mikroskopen gesehen werden können.
Hier sind einige der Eigenschaften von BN-Nanoröhren:
-Sie haben eine hohe Hydrophobizität, dh sie stoßen Wasser ab
-Sie haben eine hohe Beständigkeit gegen Oxidation und Hitze (sie können einer Oxidation bis zu 1000 ° C widerstehen).
-Sie weisen eine hohe Wasserstoffspeicherkapazität auf
-Strahlung absorbieren
-Sie sind sehr gute Isolatoren von Elektrizität
-Sie haben eine hohe Wärmeleitfähigkeit
-Aufgrund ihrer hervorragenden Oxidationsbeständigkeit bei hohen Temperaturen können sie zur Erhöhung der Oxidationsstabilität von Oberflächen eingesetzt werden..
-Aufgrund ihrer Hydrophobizität können sie zur Herstellung von superhydrophoben Oberflächen verwendet werden, dh sie haben keine Affinität zu Wasser und Wasser dringt nicht in sie ein.
-BN-Nanoröhren verbessern die Eigenschaften bestimmter Materialien, beispielsweise wurde sie verwendet, um die Härte und Bruchfestigkeit von Glas zu erhöhen.

In medizinischen Anwendungen
BN-Nanoröhren wurden als Träger für Krebsmedikamente wie Doxorubicin getestet. Bestimmte Zusammensetzungen mit diesen Materialien erhöhten die Effizienz der Chemotherapie mit dem Arzneimittel..
In mehreren Erfahrungen wurde gezeigt, dass BN-Nanoröhren das Potenzial haben, neue Medikamente zu transportieren und ordnungsgemäß freizusetzen.
Die Verwendung von BN-Nanoröhren in polymeren Biomaterialien wurde untersucht, um deren Härte, Abbaugeschwindigkeit und Haltbarkeit zu erhöhen. Dies sind Materialien, die beispielsweise in orthopädischen Implantaten verwendet werden.
Als Sensoren
BN-Nanoröhren wurden verwendet, um neuartige Vorrichtungen zum Nachweis von Feuchtigkeit, Kohlendioxid und CO zu bauenzwei und für klinische Diagnosen. Diese Sensoren haben eine schnelle Reaktion und eine kurze Erholungszeit gezeigt..
Mögliche Toxizität von BN-Materialien
Es gibt einige Bedenken hinsichtlich der möglichen toxischen Wirkungen von BN-Nanoröhren. Es gibt keinen klaren Konsens über ihre Zytotoxizität, da einige Studien zeigen, dass sie für Zellen toxisch sind, während andere das Gegenteil anzeigen..
Dies ist auf seine Hydrophobizität oder Unlöslichkeit in Wasser zurückzuführen, da es schwierig ist, Studien an biologischen Materialien durchzuführen..
Einige Forscher haben die Oberfläche von BN-Nanoröhren mit anderen Verbindungen beschichtet, die ihre Löslichkeit in Wasser begünstigen. Dies hat jedoch zu einer größeren Unsicherheit in den Erfahrungen geführt.
Obwohl die meisten Studien darauf hinweisen, dass die Toxizität gering ist, sollten schätzungsweise genauere Untersuchungen durchgeführt werden.
Verweise
- Xiong, J. et al. (2020). Hexagonales Bornitrid-Adsorbens: Synthese, Leistungsanpassung und Anwendungen. Journal of Energy Chemistry 40 (2020) 99-111. Von reader.elsevier.com wiederhergestellt.
- Mukasyan, A.S. (2017). Bornitrid. In prägnanter Enzyklopädie der sich selbst ausbreitenden Hochtemperatursynthese. Von sciencedirect.com wiederhergestellt.
- Kalay, S. et al. (2015). Synthese von Bornitrid-Nanoröhren und ihre Anwendungen. Beilstein J. Nanotechnol. 2015, 6, 84 & ndash; 102. Von ncbi.nlm.nih.gov wiederhergestellt.
- Arya, S.P.S. (1988). Herstellung, Eigenschaften und Anwendungen von Bornitrid-Dünnschichten. Thin Solid Films, 157 (1988) 267 & ndash; 282. Von sciencedirect.com wiederhergestellt.
- Zhang, J. et al. (2014). Kubische Bornitrid-haltige Keramikmatrix-Verbundwerkstoffe für Schneidwerkzeuge. Fortschritte bei Keramikmatrix-Verbundwerkstoffen. Von sciencedirect.com wiederhergestellt.
- Cotton, F. Albert und Wilkinson, Geoffrey. (1980). Fortgeschrittene Anorganische Chemie. Vierte Edition. John Wiley & Sons.
- Sudarsan, V. (2017). Materialien für feindliche chemische Umgebungen. In Materialien unter extremen Bedingungen. Von sciencedirect.com wiederhergestellt
- Dean, J.A. (Herausgeber) (1973). Langes Handbuch der Chemie. McGraw-Hill Company.
- Mahan, B.H. (1968). Universitätschemie. Interamerikanischer Bildungsfonds, S.A..



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.