
Struktur, Eigenschaften, Beispiele amphipathischer Moleküle
Das amphipathische oder amphiphile Moleküle Sie sind diejenigen, die gleichzeitig Affinität oder Abstoßung für ein bestimmtes Lösungsmittel fühlen können. Lösungsmittel werden chemisch als polar oder unpolar klassifiziert; hydrophil oder hydrophob. Somit können diese Arten von Molekülen Wasser "lieben", genauso wie sie es auch "hassen" können..
Nach der vorherigen Definition gibt es nur einen Weg, dies zu ermöglichen: Diese Moleküle müssen polare und unpolare Regionen innerhalb ihrer Strukturen aufweisen; Entweder sind sie mehr oder weniger homogen verteilt (wie zum Beispiel bei Proteinen) oder sie sind heterogen lokalisiert (bei Tensiden)

Tenside, auch Detergenzien genannt, sind vielleicht die bekanntesten amphipathischen Moleküle von allen seit jeher. Seit der Mensch von der seltsamen Physiognomie einer Blase fasziniert ist, die sich um die Herstellung von Seifen und Reinigungsmitteln kümmert, ist er immer wieder auf das Phänomen der Oberflächenspannung gestoßen.
Das Beobachten einer Blase ist dasselbe wie das Beobachten einer „Falle“, deren Wände, die durch die Ausrichtung amphipathischer Moleküle gebildet werden, den gasförmigen Inhalt der Luft behalten. Seine sphärischen Formen sind mathematisch und geometrisch am stabilsten, da sie die Oberflächenspannung der Luft-Wasser-Grenzfläche auf ein Minimum reduzieren..
Es wurden jedoch zwei weitere Eigenschaften von amphipathischen Molekülen diskutiert: Sie neigen dazu, sich zu assoziieren oder selbst zu organisieren, und einige geringere Oberflächenspannungen in Flüssigkeiten (diejenigen, die dies können, werden als Tenside bezeichnet)..
Aufgrund der hohen Assoziationstendenz eröffnen diese Moleküle ein Feld morphologischer (und sogar architektonischer) Untersuchungen ihrer Nanoaggregate und der Supramoleküle, aus denen sie bestehen. mit dem Ziel, Verbindungen zu entwickeln, die funktionalisiert werden können und auf unermessliche Weise mit Zellen und ihren biochemischen Matrices interagieren.
Artikelverzeichnis
- 1 Struktur
- 1.1 Intermolekulare Wechselwirkungen
- 1.2 Verschiedenes
- 2 Eigenschaften amphipathischer Moleküle
- 2.1 Verein
- 2.2 Physisch
- 3 Beispiele
- 4 Anwendungen
- 4.1 Zellmembranen
- 4.2 Dispergiermittel
- 4.3 Emulgatoren
- 4.4 Reinigungsmittel
- 4.5 Antioxidantien
- 5 Referenzen
Struktur
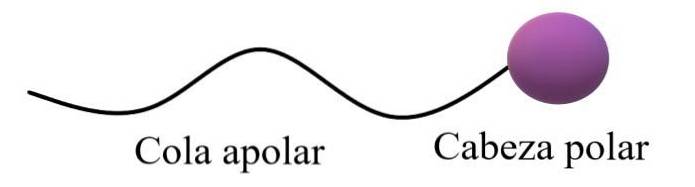
Amphiphile oder amphipathische Moleküle sollen eine polare Region und eine unpolare Region haben. Die unpolare Region besteht normalerweise aus einer gesättigten oder ungesättigten Kohlenstoffkette (mit Doppel- oder Dreifachbindungen), die als "unpolarer Schwanz" dargestellt wird; begleitet von einem „Polarkopf“, in dem sich die elektronegativsten Atome befinden.
Die obere allgemeine Struktur veranschaulicht die Kommentare im vorherigen Absatz. Der Polarkopf (violette Kugel) kann funktionelle Gruppen oder aromatische Ringe sein, die permanente Dipolmomente aufweisen und auch Wasserstoffbrückenbindungen bilden können. Daher sollte dort der höchste Sauerstoff- und Stickstoffgehalt liegen.
In diesem Polarkopf können auch ionische, negative oder positive Ladungen (oder beides gleichzeitig) vorhanden sein. Diese Region zeigt eine hohe Affinität zu Wasser und anderen polaren Lösungsmitteln..
Andererseits interagiert der apolare Schwanz aufgrund seiner vorherrschenden CH-Bindungen durch Londoner Streukräfte. Diese Region ist dafür verantwortlich, dass amphipathische Moleküle auch eine Affinität zu Fetten und unpolaren Molekülen in der Luft aufweisen (N.zwei, COzwei, Ar usw.).
In einigen Chemietexten wird das Modell für die obere Struktur mit der Form eines Lutschers verglichen.
Intermolekulare Wechselwirkungen
Wenn ein amphipathisches Molekül mit einem polaren Lösungsmittel, beispielsweise Wasser, in Kontakt kommt, üben seine Regionen unterschiedliche Wirkungen auf die Lösungsmittelmoleküle aus..
Zunächst versuchen die Wassermoleküle, den Polarkopf zu solvatisieren oder zu hydratisieren, wobei sie sich vom unpolaren Schwanz fernhalten. In diesem Prozess entsteht eine molekulare Störung.
Währenddessen neigen die Wassermoleküle um den unpolaren Schwanz dazu, sich so anzuordnen, als wären sie kleine Kristalle, wodurch sie Abstoßungen minimieren können. In diesem Prozess wird eine molekulare Ordnung erzeugt.
Zwischen Störungen und Ordnungen wird es einen Punkt geben, an dem das amphipathische Molekül versucht, mit einem anderen zu interagieren, was zu einem viel stabileren Prozess führt.
Verschiedenes
Beide werden durch ihre unpolaren Schwänze oder polaren Köpfe so angefahren, dass verwandte Regionen zuerst interagieren. Dies ist das Gleiche wie die Vorstellung, dass sich zwei "lila Lutscher" im obigen Bild nähern, indem sie ihre schwarzen Schwänze miteinander verflechten oder ihre beiden lila Köpfe verbinden..
Und so beginnt ein interessantes Assoziationsphänomen, bei dem mehrere dieser Moleküle nacheinander verbunden werden. Sie werden nicht willkürlich zugeordnet, sondern gemäß einer Reihe von Strukturparametern, die dazu führen, dass die unpolaren Schwänze in einer Art „unpolarem Kern“ isoliert werden, während die polaren Köpfe als polare Hülle freigelegt werden..
Es wird dann gesagt, dass eine kugelförmige Miscella geboren wurde. Während der Bildung der Miscela gibt es jedoch eine Vorstufe, die aus einer sogenannten Lipiddoppelschicht besteht. Dies und andere sind einige der vielen Makrostrukturen, die amphiphile Moleküle annehmen können.
Eigenschaften amphipathischer Moleküle
Verband

Wenn die unpolaren Schwänze als schwarze Einheiten und die polaren Köpfe als violette Einheiten betrachtet werden, versteht es sich, warum im oberen Bild die Rinde der Mispel violett und ihr Kern schwarz ist. Der Kern ist unpolar und seine Wechselwirkungen mit den Wasser- oder Lösungsmittelmolekülen sind Null..
Wenn andererseits das Lösungsmittel oder Medium unpolar ist, sind es die Polköpfe, die die Abstoßungen erleiden, und folglich befinden sie sich in der Mitte der Miscella; das heißt, es ist invertiert (A, unteres Bild).
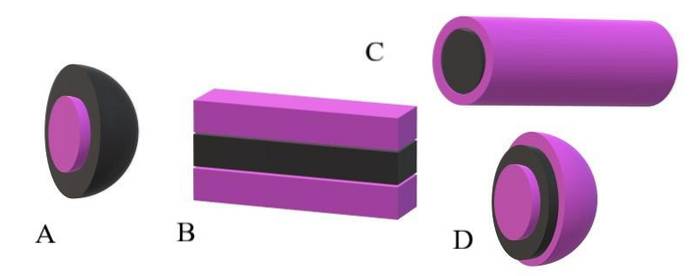
Es wird beobachtet, dass das invertierte Miscela eine schwarze unpolare Schale und einen violetten polaren Kern aufweist. Bevor sich jedoch Miscelas bilden, werden die amphiphilen Moleküle einzeln gefunden, wodurch sich die Reihenfolge der Lösungsmittelmoleküle ändert. Erhöhte Konzentration, sie beginnen sich in einer Struktur von einer oder zwei Schichten zu verbinden (B).
Von B aus beginnen sich die Plättchen zu krümmen, um D, ein Vesikel, zu bilden. Eine andere Möglichkeit, abhängig von der Form des apolaren Schwanzes in Bezug auf seinen polaren Kopf, besteht darin, dass sie sich verbinden, um eine zylindrische Miscella hervorzurufen (C)..
Nanoaggregate und Supramoleküle
Es gibt daher fünf Hauptstrukturen, die ein grundlegendes Merkmal dieser Moleküle offenbaren: ihre hohe Tendenz zur Assoziation und Selbstorganisation zu Supramolekülen, die sich zu Nanoaggregaten aggregieren..
Somit werden amphiphile Moleküle nicht allein, sondern in Verbindung gefunden..
Körperlich
Amphipathische Moleküle können neutral oder ionisch geladen sein. Diejenigen, die negative Ladungen haben, haben ein Sauerstoffatom mit einer negativen formalen Ladung in ihrem Polarkopf. Einige dieser Sauerstoffatome stammen aus funktionellen Gruppen wie: -COO-, -SW4-, -SW3- oder -PO4-.
Positive Ladungen stammen im Allgemeinen von Aminen, RNH3+.
Das Vorhandensein oder Fehlen dieser Ladungen ändert nichts an der Tatsache, dass diese Moleküle im Allgemeinen kristalline Feststoffe bilden; oder, wenn sie relativ leicht sind, werden sie als Öle gefunden.
Beispiele
Einige Beispiele für amphipathische oder amphiphile Moleküle werden nachstehend erwähnt:
-Phofolipide: Phosphatidylethanolamin, Sphingomyelin, Phosphatidylserin, Phosphatidylcholin.
-Cholesterin.
-Glykolipide.
-Natriumlaurylsulfat.
-Proteine (sie sind amphiphil, aber keine Tenside).
-Phenolische Fette: Cardanol, Cardole und Anacardsäuren.
-Cetyltrimethylammoniumbromid.
-Fettsäuren: Palmitinsäure, Linolsäure, Ölsäure, Laurinsäure, Stearinsäure.
-Langkettige Alkohole: 1-Dodecanol und andere.
-Amphiphile Polymere: wie ethoxylierte Phenolharze.
Anwendungen
Zellmembranen
Eine der wichtigsten Konsequenzen der Assoziationsfähigkeit dieser Moleküle ist, dass sie eine Art Wand bilden: die Lipiddoppelschicht (B).
Diese Doppelschicht dient zum Schutz und zur Regulierung des Eintritts und Austritts von Verbindungen in Zellen. Es ist dynamisch, da sich seine unpolaren Schwänze drehen und amphipathischen Molekülen helfen, sich zu bewegen..
Wenn diese Membran an zwei Enden angebracht ist, um sie vertikal zu haben, wird sie ebenfalls verwendet, um ihre Permeabilität zu messen; und damit werden wertvolle Daten für das Design von biologischen Materialien und synthetischen Membranen aus der Synthese neuer amphipathischer Moleküle mit unterschiedlichen Strukturparametern erhalten..
Dispergiermittel
In der Ölindustrie werden diese Moleküle und die daraus synthetisierten Polymere verwendet, um Asphaltene zu dispergieren. Der Schwerpunkt dieser Anwendung liegt auf der Hypothese, dass Asphaltene aus einem kolloidalen Feststoff bestehen, mit einer hohen Neigung zur Flockung und Sedimentation als braun-schwarzer Feststoff, der ernsthafte wirtschaftliche Probleme verursacht..
Amphipathische Moleküle tragen dazu bei, dass Asphaltene angesichts physikalisch-chemischer Veränderungen im Rohöl länger dispergiert bleiben..
Emulgatoren
Diese Moleküle helfen, zwei Flüssigkeiten zu mischen, die unter normalen Bedingungen nicht mischbar wären. In Eiscreme zum Beispiel helfen sie Wasser und Luft, zusammen mit Fett einen Teil desselben Feststoffs zu bilden. Zu den am häufigsten verwendeten Emulgatoren für diesen Zweck gehören solche, die von essbaren Fettsäuren abgeleitet sind.
Reinigungsmittel
Der amphiphile Charakter dieser Moleküle wird verwendet, um Fette oder unpolare Verunreinigungen einzufangen, die später gleichzeitig von einem polaren Lösungsmittel wie Wasser weggetragen werden..
Wie am Beispiel von Blasen, in denen Luft eingeschlossen war, fangen Waschmittel Fett in ihren Mizellen ein, die mit einer polaren Hülle effizient mit Wasser interagieren, um Schmutz zu entfernen..
Antioxidantien
Die Polköpfe sind von entscheidender Bedeutung, da sie die vielfältigen Verwendungsmöglichkeiten dieser Moleküle im Körper definieren.
Wenn sie beispielsweise eine Reihe von aromatischen Ringen (einschließlich Derivaten eines Phenolrings) und polaren Ringen aufweisen, die freie Radikale neutralisieren können, gibt es amphiphile Antioxidantien; und wenn ihnen auch toxische Wirkungen fehlen, werden neue Antioxidantien auf dem Markt verfügbar sein.
Verweise
- Alberts B., Johnson A., Lewis J., et al. (2002). Molekularbiologie der Zelle. 4. Auflage. New York: Garland Science; Die Lipiddoppelschicht. Wiederhergestellt von: ncbi.nlm.nih.gov
- Jianhua Zhang. (2014). Amphiphile Moleküle. Springer-Verlag Berlin Heidelberg, E. Droli, L. Giorno (Hrsg.), Encyclopedia of Membranes, DOI 10.1007 / 978-3-642-40872-4_1789-1.
- Sagte Joseph. (2019). Definition von amphipathischen Molekülen. Studie. Wiederhergestellt von: study.com
- Lehninger, A. L. (1975). Biochemie. (2. Auflage). Worth Publishers, inc.
- C. K. Mathews, K. E. van Holde und K. G. Ahern (2002). Biochemie. (3. Auflage). Pearson Addison Weshley.
- Helmenstine, Anne Marie, Ph.D. (31. März 2019). Was ist ein Tensid? Wiederhergestellt von :oughtco.com
- Domenico Lombardo, Michail A. Kiselev, Salvatore Magazù und Pietro Calandra (2015). Selbstorganisation von Amphiphilen: Grundkonzepte und Zukunftsperspektiven supramolekularer Ansätze. Fortschritte in der Festkörperphysik, vol. 2015, Artikel-ID 151683, 22 Seiten, 2015. doi.org/10.1155/2015/151683.
- Anankanbil S., Pérez B., Fernandes I., Magdalena K. Widzisz, Wang Z., Mateus N. und Guo Z. (2018). Eine neue Gruppe synthetischer phenolhaltiger amphiphiler Moleküle für Mehrzweckanwendungen: physikalisch-chemische Charakterisierung und Zelltoxizitätsstudie. Wissenschaftliche Berichte Band 8, Artikelnummer: 832.



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.