
Struktur, Biosynthese und Funktionen von Phosphatidylethanolamin
Das Phosphatidylethanolamin (PE) ist ein Glycerophospholipid, das in den Plasmamembranen prokaryotischer Organismen häufig vorkommt. Im Gegensatz dazu ist dies in eukaryotischen Zellmembranen nach Phosphatidylcholin das zweithäufigste Glycerophospholipid im Inneren der Plasmamembran..
Trotz der Häufigkeit von Phosphatidylethanolamin hängt seine Häufigkeit nicht nur vom Zelltyp ab, sondern auch vom Kompartiment und dem Moment des jeweiligen betrachteten Zelllebenszyklus..
Biologische Membranen sind Barrieren, die zelluläre Organismen definieren. Sie haben nicht nur Schutz- und Isolationsfunktionen, sondern sind auch der Schlüssel zur Etablierung von Proteinen, die für ihre optimale Funktion eine hydrophobe Umgebung benötigen..
Sowohl Eukaryoten als auch Prokaryoten haben Membranen, die hauptsächlich aus Glycerophospholipiden und in geringerem Maße aus Sphingolipiden und Sterolen bestehen..
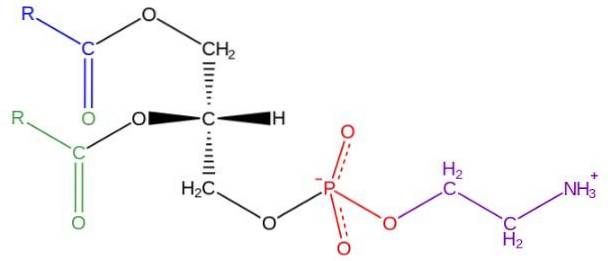
Glycerophospholipide sind amphipathische Moleküle, die auf einem L-Glycerin-Grundgerüst strukturiert sind, das an den Positionen sn-1 und sn-2 durch zwei Fettsäuren unterschiedlicher Länge und Sättigungsgrad verestert ist. In der Hydroxylgruppe der sn-3-Position wird es durch eine Phosphatgruppe verestert, an die wiederum verschiedene Arten von Molekülen gebunden werden können, aus denen die verschiedenen Klassen von Glycerophospholipiden hervorgehen.
In der zellulären Welt gibt es eine große Vielfalt von Glycerophospholipiden, am häufigsten sind jedoch Phosphatidylcholin (PC), Phosphatidylethanolamin (PE), Phosphatidylserin (PS), Phosphatidylinositol (PI), Phosphatidsäure (PA), Phosphatidylglycerin (PG) und Cardiolipin (CL).
Artikelverzeichnis
- 1 Struktur
- 2 Biosynthese
- 2.1 Kennedy Route
- 2.2 PSD-Pfad
- 3 Funktionen
- 4 Referenzen
Struktur
Die Struktur von Phosphatidylethanolamin wurde 1952 von Baer et al. Entdeckt. Wie experimentell für alle Glycerophospholipide bestimmt wurde, wird Phosphatidylethanolamin durch ein Glycerinmolekül gebildet, das an den Positionen sn-1 und sn-2 mit Säureketten zwischen 16 und 20 verestert ist Kohlenstoffatome.
Die in der sn-1-Hydroxylgruppe veresterten Fettsäuren sind im Allgemeinen gesättigt (ohne Doppelbindungen) mit einer maximalen Länge von 18 Kohlenstoffatomen, während die in der sn-2-Position verknüpften Ketten länger und mit einer oder mehreren Ungesättigtheiten (Doppelbindungen) sind..
Der Sättigungsgrad dieser Ketten trägt zur Elastizität der Membran bei, was einen großen Einfluss auf die Insertion und Sequestrierung von Proteinen in die Doppelschicht hat..
Phosphatidylethanolamin wird als nicht lamellares Glycerophospholipid angesehen, da es eine konische geometrische Form hat. Diese Form ergibt sich aus der geringen Größe seiner polaren Gruppe oder seines "Kopfes" im Verhältnis zu der der Fettsäureketten, aus denen die hydrophoben "Schwänze" bestehen..
Der "Kopf" oder die polare Gruppe von Phosphatidylethanolamin hat einen zwitterionischen Charakter, dh er hat Gruppen, die unter bestimmten pH-Bedingungen positiv und negativ geladen werden können..
Diese Eigenschaft ermöglicht es ihm, Wasserstoffbrücken mit einer großen Anzahl von Aminosäureresten zu binden, und seine Ladungsverteilung ist eine wesentliche Determinante für die Domänentopologie vieler integraler Membranproteine..
Biosynthese
In eukaryotischen Zellen ist die Synthese von Strukturlipiden geografisch begrenzt, wobei die Hauptbiosynthesestelle das endoplasmatische Retikulum (ER) und in geringerem Maße der Golgi-Apparat ist..
Es gibt vier unabhängige Biosynthesewege für die Herstellung von Phosphatidylethanolamin: (1) den CDP-Ethanolamin-Weg, auch als Kennedy-Weg bekannt; (2) den PSD-Weg für die Phosphatidylserin (PS) -Decarboxylierung; (3) Acylierung von Lyso-PE und (4) Basenwechselreaktionen der polaren Gruppe anderer Glycerophospholipide.
Kennedy Route
Die Phosphatidylethanolamin-Biosynthese auf diesem Weg ist auf ER beschränkt, und es wurde gezeigt, dass sie in Hamsterleberzellen der Hauptproduktionsweg ist. Es besteht aus drei aufeinanderfolgenden enzymatischen Schritten, die durch drei verschiedene Enzyme katalysiert werden.
Im ersten Schritt werden Phosphoethanolamin und ADP dank der Wirkung der Ethanolaminkinase hergestellt, die die ATP-abhängige Phosphorylierung von Ethanolamin katalysiert..
Im Gegensatz zu Pflanzen sind weder Säugetiere noch Hefen in der Lage, dieses Substrat zu produzieren. Daher muss es über die Nahrung aufgenommen oder aus dem Abbau bereits vorhandener Phosphatidylethanolamin- oder Sphingosinmoleküle gewonnen werden..
Phosphoethanolamin wird von CTP: Phosphoethanolamin-Cytidyltransferase (ET) verwendet, um die Hochenergieverbindung CDP: Ethanolamin und ein anorganisches Phosphat zu bilden.
1,2-Diacylglycerolethanolaminphosphotransferase (ETP) verwendet die in der CDP-Ethanolaminbindung enthaltene Energie, um Ethanolamin kovalent an ein in die Membran eingefügtes Diacylglycerinmolekül zu binden, wodurch Phosphatidylethanolamin entsteht..
Route PSD
Diese Route funktioniert sowohl bei Prokaryoten als auch bei Hefen und Säugetieren. In Bakterien kommt es in der Plasmamembran vor, in Eukaryoten jedoch in einem Bereich des endoplasmatischen Retikulums, der eng mit der Mitochondrienmembran verwandt ist.
Bei Säugetieren wird der Weg durch ein einziges Enzym, Phosphatidylserin-Decarboxylase (PSD1p), katalysiert, das in die Mitochondrienmembran eingebettet ist, deren Gen vom Kern kodiert wird. Die Reaktion beinhaltet die Decarboxylierung von PS zu Phosphatidylethanolamin.
Die verbleibenden zwei Wege (PE-Lysoacylierung und polargruppenabhängiger Calciumaustausch) treten im endoplasmatischen Retikulum auf, tragen jedoch nicht wesentlich zur gesamten Phosphatidylethanolaminproduktion in eukaryotischen Zellen bei..
Eigenschaften
Glycerophospholipide haben drei Hauptfunktionen in der Zelle, darunter die Strukturfunktionen Energiespeicherung und Zellsignalisierung..
Phosphatidylethanolamin ist mit der Verankerung, Stabilisierung und Faltung mehrerer Membranproteine sowie den Konformationsänderungen verbunden, die für die Funktion vieler Enzyme erforderlich sind.
Es gibt experimentelle Hinweise darauf, dass Phosphatidylethanolamin als entscheidendes Glycerophospholipid im späten Stadium der Telophase während der Bildung des kontraktilen Rings und der Bildung des Fragmoplasten, der die Teilung der Membran der beiden Tochterzellen ermöglicht, vorgeschlagen wird..
Es spielt auch eine wichtige Rolle bei allen Prozessen der Fusion und Spaltung (Vereinigung und Trennung) der Membranen sowohl des endoplasmatischen Retikulums als auch des Golgi-Apparats..
In E. coli wurde gezeigt, dass Phosphatidylethanolamin für die korrekte Faltung und Funktion des Enzyms Lactosepermease notwendig ist, weshalb vermutet wurde, dass es eine Rolle als molekulares „Chaperon“ spielt..
Phosphatidylethanolamin ist der Hauptdonor des Ethanolaminmoleküls, das für die posttranslationale Modifikation zahlreicher Proteine wie GPI-Anker erforderlich ist.
Dieses Glycerophospholipid ist der Vorläufer zahlreicher Moleküle mit enzymatischer Aktivität. Darüber hinaus können aus seinem Stoffwechsel stammende Moleküle sowie Diacylglycerin, Phosphatidsäure und einige Fettsäuren als Second Messenger fungieren. Darüber hinaus ist es ein wichtiges Substrat für die Herstellung von Phosphatidylcholin..
Verweise
- Brouwers, J.F.H.M., Vernooij, E.A.A.M., Tielens, A.G.M. & van Golde, L.M.G. (1999). Schnelle Trennung und Identifizierung von Phosphatidylethanolamin-Molekülspezies. Journal of Lipid Research, 40 (1), 164 & ndash; 169. Von jlr.org wiederhergestellt
- E. Calzada, J. M. McCaffery & S. M. Claypool (2018). In der inneren Mitochondrienmembran produziertes Phosphatidylethanolamin ist für die Hefe-Cytochrom-bc1-Komplexfunktion 3 essentiell. BioRxiv, 1, 46.
- Calzada, E., Onguka, O. & Claypool, S. M. (2016). Phosphatidylethanolamin-Stoffwechsel in Gesundheit und Krankheit. International Review of Cell and Molecular Biology (Vol. 321). Elsevier Inc..
- Gibellini, F. & Smith, T. K. (2010). Die Kennedy-Pathway-de-novo-Synthese von Phosphatidylethanolamin und Phosphatidylcholin. IUBMB Life, 62 (6), 414 & ndash; 428.
- Harayama, T. & Riezman, H. (2018). Verständnis der Vielfalt der Membranlipidzusammensetzung. Nature Reviews Molecular Cell Biology, 19 (5), 281 & ndash; 296.
- Luckey, M. (2008). Membranstrukturbiologie: mit biochemischen und biophysikalischen Grundlagen. Cambrudge University Press. Von cambrudge.org wiederhergestellt
- J. M. Seddon, G. Cevc, R. D. Kaye & D. Marsh (1984). Röntgenbeugungsstudie zum Polymorphismus hydratisierter Diacyl- und Dialkylphosphatidylethanolamine. Biochemistry, 23 (12), 2634 & ndash; 2644.
- A. M. Sendecki, M. F. Poyton, A. J. Baxter, T. Yang & P. S. Cremer (2017). Unterstützte Lipiddoppelschichten mit Phosphatidylethanolamin als Hauptkomponente. Langmuir, 33 (46), 13423 & ndash; 13499.
- van Meer, G., Voelker, D. R. & Feignenson, G. W. (2008). Membranlipide: Wo sie sind und wie sie sich verhalten. Nature Reviews, 9, 112-124.
- Vance, J. E. (2003). Molekular- und Zellbiologie des Phosphatidylserin- und Phosphatidylethanolamin-Metabolismus. In K. Moldave (Hrsg.), Progress Nucleic Acid Research and Molecular Biology (S. 69-111). Akademische Presse.
- Vance, J. E. (2008). Phosphatidylserin und Phosphatidylethanolamin in Säugetierzellen: zwei metabolisch verwandte Aminophospholipide. Journal of Lipid Research, 49 (7), 1377-1387.
- Vance, J. E. & Tasseva, G. (2013). Bildung und Funktion von Phosphatidylserin und Phosphatidylethanolamin in Säugetierzellen. Biochimica et Biophysica Acta - Molekular- und Zellbiologie von Lipiden, 1831 (3), 543-554.
- Watkins, S. M., Zhu, X. & Zeisel, S. H. (2003). Phosphatidylethanolamin-N-Methyltransferase-Aktivität und Cholin aus der Nahrung regulieren den Lipidfluss im Leberplasma und den Stoffwechsel essentieller Fettsäuren bei Mäusen. The Journal of Nutrition, 133 (11), 3386-3391.



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.