
Sialinsäurestruktur, Funktionen und Krankheiten
Das Sialinsäuren Sie sind Monosaccharide mit neun Kohlenstoffatomen. Sie gehören zur Familie der Neuraminsäurederivate (5-Amino-3,5-didesoxy-D-glycero-D-galacto-nonulosonsäure) und sind in der Natur, insbesondere im Tierreich, weit verbreitet.
Sie treten normalerweise nicht als freie Moleküle auf, sondern sind durch α-Glucosidbindungen an Kohlenhydratmoleküle oder andere Sialinsäuremoleküle gebunden und können dann terminale oder interne Positionen innerhalb einer linearen Kohlenhydratkette einnehmen.
Der Begriff „Sialinsäure“ wurde erstmals 1957 von Gunnar Blix geprägt, obwohl frühere Berichte anderer Forscher darauf hinweisen, dass seine Entdeckung ein oder zwei Jahrzehnte früher zurückliegt, als sie als Teil von Sialo-Mucin-Glykoproteinen und Sialo-Sialo-Sialo-Singolipiden (Gangliosiden) beschrieben wurden ).
Sialinsäuren kommen in vielen Naturreichen vor. Sie wurden in einigen Viren, pathogenen Bakterien, Protozoen, Krebstieren, Plattwürmern, Insekten und Wirbeltieren wie Fischen, Amphibien, Vögeln und Säugetieren nachgewiesen. Im Gegenteil, sie wurden nicht in Pilzen, Algen oder Pflanzen gefunden..
Artikelverzeichnis
- 1 Struktur
- 2 Funktionen
- 2.1 Rolle bei Zelladhäsionsprozessen
- 2.2 Rolle in der Lebensdauer von Blutzellenkomponenten
- 2.3 Rollen im Immunsystem
- 2.4 Andere Funktionen
- 3 Krankheiten
- 4 Referenzen
Struktur
Sialinsäuren kommen hauptsächlich im terminalen Teil von Oberflächenglykoproteinen und Glykolipiden vor und verleihen diesen Glykokonjugaten eine große Vielfalt. Differenzielle "Sialylierungs" -Muster sind Produkte der Expression von gewebespezifischen Glycosyltransferasen (Sialyltransferasen).
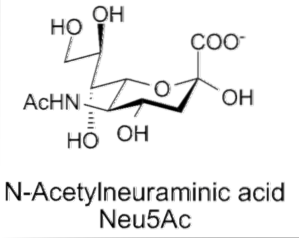
Strukturell gehören Sialinsäuren zu einer Familie von etwa 40 natürlichen Derivaten der Neuraminsäure, die N-acyliert sind, wodurch zwei "Eltern" -Strukturen entstehen: N-Acetylneuraminsäure (Neu5Ac) oder N-Glycolylneuraminsäure (Neu5Gc).
Seine strukturellen Eigenschaften umfassen das Vorhandensein einer Aminogruppe (die modifiziert werden kann) an Position 5 und einer Carboxylgruppe an Position 1, die bei physiologischem pH ionisiert werden kann. Ein desoxygenierter C-3-Kohlenstoff und ein Glycerinmolekül an der C-6-Position.
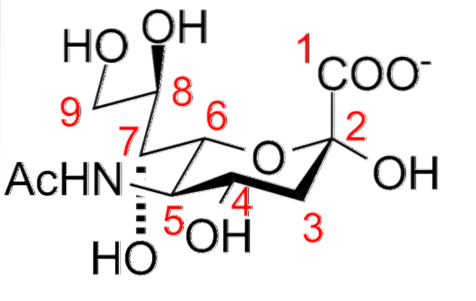
Viele Derivate entstehen durch Substitution der Hydroxylgruppen an den Positionen C-4, C-7, C-8 und C-9 durch Acetyl-, Glykol-, Lactyl-, Methyl-, Sulfat- und Phosphatanteile; sowie die Einführung von Doppelbindungen zwischen C-2 und C-3.
In der linearen Endposition beinhaltet die Bindung eines Sialinsäureanteils an eine Oligosaccharidkette eine α-Glucosidbindung zwischen der Hydroxylgruppe des anomeren C-2-Kohlenstoffs der Sialinsäure und den Hydroxylgruppen der C-3, C-Kohlenstoffe 4 oder C-6 des Monosaccharidanteils.
Diese Bindungen können zwischen Galactoseresten, N-Acetylglucosamin, N-Acetylgalactosamin und in einigen einzigartigen Gangliosiden Glucose bestehen. Sie können durch N-glycosidische oder O-glycosidische Bindungen auftreten.
Eigenschaften
Es wird angenommen, dass Sialinsäuren parasitären Organismen helfen, im Wirtsorganismus zu überleben. Beispiele hierfür sind Säugetierpathogene, die Sialinsäurestoffwechselenzyme produzieren (Sialidasen oder N-Acetylneuramin-Lyasen)..
Es gibt keine Säugetierspezies, für die das Vorhandensein von Sialinsäuren nicht als Teil von Glykoproteinen im Allgemeinen, Serumglykoproteinen, der Schleimhaut, als Teil von Zelloberflächenstrukturen oder als Teil komplexer Kohlenhydrate berichtet wurde.
Sie wurden in sauren Oligosacchariden in der Milch und im Kolostrum von Menschen, Rindern, Schafen, Hunden und Schweinen sowie als Teil des Urins von Ratten und Menschen gefunden..
Rolle bei Zelladhäsionsprozessen
Glykokonjugate mit Sialinsäureanteilen spielen eine wichtige Rolle beim Informationsaustausch zwischen benachbarten Zellen sowie zwischen Zellen und ihrer Umgebung..
Das Vorhandensein von Sialinsäure in Zellmembranen trägt zur Bildung einer negativen Ladung auf der Oberfläche bei, was positive Auswirkungen auf einige elektrostatische Abstoßungsereignisse zwischen Zellen und einigen Molekülen hat..
Zusätzlich gibt die negative Ladung den Sialinsäuren in der Membran eine Funktion beim Transport positiv geladener Ionen..
Es wurde berichtet, dass die Bindung des Endothels und des Epithels an die glomeruläre Basalmembran durch Sialinsäure erleichtert wird, und dies beeinflusst auch den Kontakt zwischen diesen Zellen..
Rolle in der Lebensdauer von Blutzellenkomponenten
Sialinsäure hat wichtige Funktionen als Teil von Glycophorin A in der Plasmamembran von Erythrozyten. Einige Studien haben gezeigt, dass der Gehalt an Sialinsäure umgekehrt proportional zum Alter dieser Zellen ist.
Mit Neuraminidaseenzymen behandelte Erythrozyten, die für den Abbau von Sialinsäure verantwortlich sind, verringern ihre Halbwertszeit im Blutkreislauf drastisch von 120 Tagen auf einige Stunden. Der gleiche Fall wurde bei Blutplättchen beobachtet.
Thrombozyten verlieren ihre Adhäsions- und Aggregationskapazität in Abwesenheit von Sialinsäure in ihren Oberflächenproteinen. In Lymphozyten spielt Sialinsäure auch eine wichtige Rolle bei der Zelladhäsion und -erkennung sowie bei der Wechselwirkung mit Oberflächenrezeptoren..
Funktionen im Immunsystem
Das Immunsystem kann anhand der Erkennung der in den Membranen vorhandenen Sialinsäuremuster zwischen eigenen und eindringenden Strukturen unterscheiden.
Sialinsäure sowie die Enzyme Neuraminidase und Sialyltransferase besitzen wichtige regulatorische Eigenschaften. Die terminalen Anteile von Sialinsäure in Plasmamembranglykokonjugaten haben Funktionen der Maskierung oder als Membranrezeptoren..
Darüber hinaus haben verschiedene Autoren die Möglichkeit angesprochen, dass Sialinsäure antigene Funktionen hat, dies ist jedoch noch nicht mit Sicherheit bekannt. Die Maskierungsfunktionen von Sialinsäureresten sind jedoch bei der Zellregulation sehr wichtig..
Die Maskierung kann eine direkte oder indirekte Schutzfunktion haben, abhängig davon, ob der Sialinsäureanteil den antigenen Kohlenhydratrest direkt bedeckt oder ob es eine Sialinsäure in einem benachbarten Glykokonjugat ist, die den Antigenanteil maskiert..
Einige Antikörper besitzen Neu5Ac-Reste, die virusneutralisierende Eigenschaften aufweisen, da diese Immunglobuline die Adhäsion von Viren an nur konjugierte (Glykokonjugate mit Teilen von Sialinsäure) auf der Zellmembran verhindern können.
Andere Funktionen
Im Darmtrakt spielen Sialinsäuren eine ebenso wichtige Rolle, da sie Teil der Mucine sind, die Schmier- und Schutzeigenschaften haben, die für den gesamten Organismus essentiell sind..
Darüber hinaus sind Sialinsäuren auch in den Membranen von Bronchial-, Magen- und Darmepithelzellen vorhanden, wo sie an Transport-, Sekretions- und anderen Stoffwechselprozessen beteiligt sind..
Krankheiten
Es ist bekannt, dass zahlreiche Krankheiten Anomalien im Sialinsäurestoffwechsel beinhalten, und diese sind als Sialidose bekannt. Zu den bekanntesten zählen Sialurie und Morbus Salla, die durch eine Urinausscheidung mit großen Mengen an freien Sialinsäuren gekennzeichnet sind.
Andere Krankheiten einer immunologischen Ordnung haben mit Veränderungen von anabolen und katabolen Enzymen zu tun, die mit dem Metabolismus von Sialinsäure zusammenhängen und eine aberrante Anreicherung von Glykokonjugaten mit Teilen von Sialinsäure verursachen..
Einige Krankheiten, die mit Blutfaktoren zusammenhängen, sind ebenfalls bekannt, wie beispielsweise die Thrombozytopenie, die aus einer Abnahme des Thrombozytenspiegels im Blut besteht, wahrscheinlich verursacht durch einen Mangel an Sialinsäure in der Membran..
Die Von-Willebrand-Krankheit entspricht einem Defekt in der Fähigkeit von Thrombozyten, an den Glykokonjugaten der subendothelialen Membran der Blutgefäßwand zu haften, der durch Defizite oder Defizite bei der Glykosylierung oder Sialylierung verursacht wird.
Glanzmanns Thrombasthenie ist eine weitere angeborene Störung der Thrombozytenaggregation, deren Wurzel das Vorhandensein defekter Glykoproteine in der Membran der Thrombozyten ist. Es wurde gezeigt, dass Defekte in diesen Glykoproteinen mit einem verringerten Neu5Ac-Gehalt verbunden sind.
Verweise
- J. Clayden, N. Greeves, S. Warren & P. Wothers (2001). Organische Chemie (1. Aufl.). New York: Oxford University Press.
- Demchenko, A. V. (2008). Handbuch der chemischen Glykosylierung: Fortschritte in der Stereoselektivität und therapeutischen Relevanz. Wiley-VCH.
- Rosenberg, A. (1995). Biologie der Sialinsäuren. New York: Springer Science + Business Media, LLC.
- Schauer, R. (1982). Sialinsäuren: Chemie, Stoffwechsel und Funktion. Springer-Verlag Wien New York.
- Traving, C. & Schauer, R. (1998). Struktur, Funktion und Metabolismus von Sialinsäuren. CMLS Cellular and Molecular Life Sciences, 54, 1330-1349.



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.