
Peressigsäurestruktur, Eigenschaften, Herstellung, Verwendung
Das Peressigsäure ist eine flüssige organische Verbindung, deren chemische Formel C istzweiH.4ODER3. Es ist das Peroxid der Essigsäure, daher ist es auch als Peroxyessigsäure bekannt. Sein Molekül ähnelt dem von Essigsäure CH3COOH aber mit einem zusätzlichen Sauerstoff am Carboxyl.
Es gehört zur Klasse der organischen Peroxide, bei denen es sich um künstliche Moleküle handelt. Die keimtötenden und sterilisierenden Eigenschaften seiner wässrigen Lösungen sind seit 1902 bekannt. Diese Wirkung kann in einigen Fällen bei Konzentrationen von nur 0,001% ausgeübt werden..

Diese Eigenschaft macht es in Kliniken und Krankenhäusern weit verbreitet, um medizinische Geräte zu sterilisieren, mit dem zusätzlichen Vorteil, dass seine Zersetzungsprodukte für den Menschen nicht toxisch sind..
PAA-Lösungen oxidieren stark, eine Eigenschaft, die zum Bleichen von Papierzellstoff oder in Wäschereien verwendet wurde. Es wird auch zur Durchführung chemischer Reaktionen angewendet, bei denen diese Eigenschaft erforderlich ist, wie Epoxidierung und Hydroxylierung..
Seine oxidierende und desinfizierende Wirkung wird in Reinigungsgeräten eingesetzt, in denen Lebensmittel und Getränke verarbeitet werden. Darüber hinaus ist es für einige Metalle ätzend und sollte bei Lagerung von organischen oder leicht oxidierbaren Verbindungen ferngehalten werden..
Beachten Sie, dass seine konzentrierten Lösungen explosiv sein können, weshalb es vorzugsweise verdünnt hergestellt und an kalten Orten gelagert werden sollte. Seine ätzende Kraft wirkt sich auch auf die menschliche Haut, die Schleimhaut und das Gewebe aus. Daher muss es mit Vorsicht und Schutzausrüstung behandelt werden.
Artikelverzeichnis
- 1 Struktur
- 2 Nomenklatur
- 3 Eigenschaften
- 3.1 Physikalischer Zustand
- 3.2 Molekulargewicht
- 3.3 Siedepunkt
- 3.4 Flammpunkt
- 3.5 Selbstentzündungstemperatur
- 3.6 Dichte
- 3.7 Viskosität
- 3.8 Brechungsindex
- 3.9 Löslichkeit
- 3,10 pH
- 3.11 Dissoziationskonstante
- 3.12 Chemische Eigenschaften
- 4 Erhalten
- 5 Verwendungen
- 5.1 In der Medizin als Sterilisationsmittel für Geräte
- 5.2 In der Abwasserbehandlung
- 5.3 In der Lebensmittelindustrie
- 5.4 In der Zellstoff- und Papierindustrie
- 5.5 Bei der Herstellung anderer chemischer Verbindungen
- 5.6 Bei der Rückgewinnung von Polymeren zum Recycling
- 5.7 In Wäschereien
- 6 Risiken
- 7 Referenzen
Struktur
Peroxyessigsäure hat ein Molekül, das Essigsäure sehr ähnlich ist, jedoch einen zusätzlichen Sauerstoff in der Struktur der -COOH-Gruppe aufweist, da es 3 Sauerstoffatome anstelle von zwei aufweist.
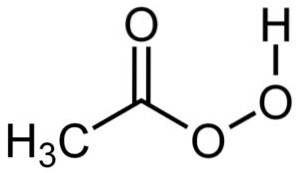
Nomenklatur
- Peressigsäure
- Peroxyessigsäure
- Ethanoperoxonsäure
- PAA Peroxiessigsäure).
Eigenschaften
Körperlicher Status
Klare farblose Flüssigkeit mit scharfem Essiggeruch.
Molekulargewicht
76,05 g / mol
Siedepunkt
110 ºC (mit Explosion)
Flammpunkt
40,5 ºC (Open-Cup-Methode)
Selbstentzündungstemperatur
200 ºC (es ist die Temperatur, bei der es spontan brennt)
Dichte
1,226 g / cm3 bei 15 ºC
Viskosität
3,280 cP bei 25,6 ° C.
Brechungsindex
1,3974 bei 20 ºC
Löslichkeit
Es ist in jedem Verhältnis mit Wasser mischbar. Es ist in polaren organischen Lösungsmitteln wie Ethanol löslich. In aromatischen Lösungsmitteln schwer löslich. Sehr gut löslich in Ether und Schwefelsäure.
pH
Weniger als 2.
Dissoziationskonstante
pKzu = 8,20 bei 25 ºC (es ist schwächer als Essigsäure mit pKzu = 4,8)
Chemische Eigenschaften
Als Säure ist PAA viel schwächer als die Säure, aus der es stammt, Essigsäure..
Es hat ein hohes Potential als Oxidationsmittel. Es ist sehr reaktiv, was die Lagerung erschwert, und dies hat seine Verwendung eingeschränkt..
Seine Abbauprodukte sind Essigsäure CH3COOH, Sauerstoff O.zwei, Wasserstoffperoxid H.zweiODERzwei und Wasser H.zweiO. Die H.zweiODERzwei wiederum wird es zu Wasser und Sauerstoff abgebaut. Alle diese Verbindungen sind umweltfreundlich.
Es ist ein Epoxidierungs- und Hydroxylierungsmittel für olefinische Bindungen (C = C-Doppelbindungen). Dies bedeutet, dass es aktiv an der Bildung von Epoxiden in Doppelbindungen organischer Moleküle und an der Addition von -OH-Gruppen an diesen beteiligt ist..
PAA ist ätzend gegenüber einigen Metallen wie glattem Stahl, verzinktem Eisen, Kupfer, Messing und Bronze. Andere Metalle wie Edelstahl, reines Aluminium und verzinntes Eisen sind beständig.
Greift synthetische und natürliche Kautschuke an und extrahiert den Weichmacher aus einigen Vinylpolymeren.
Es hat einen stechenden und stechenden Geruch, der an Essigsäure erinnert (Essigsäure ist der Hauptbestandteil von Essig)..
Erhalten
Durch Umsetzen von Eisessig (wasserfrei, d. H. Ohne Wasser) mit Wasserstoffperoxid H.zweiODERzwei in Gegenwart einer Mineralsäure (wie Schwefelsäure H.zweiSW4) wird ein Teil der Essigsäure oxidiert und es werden wässrige Lösungen von Peressigsäure, Essigsäure und H erhaltenzweiODERzwei.

Die H.zweiSW4 wirkt als Katalysator oder Beschleuniger der Reaktion. Es werden Stabilisierungsmittel wie Pyridin-2,6-dicarbonsäure verwendet.
Wenn diese Lösungen destilliert werden, kann eine höhere Konzentration an Peressigsäure erhalten werden..
Es kann auch durch Oxidation von Acetaldehyd CH erhalten werden3CHO mit Ozon O.3, oder durch Reaktion von Essigsäureanhydrid (CH3CO)zweiOder mit H.zweiODERzwei.
Eine andere Möglichkeit, es genau dort einzusetzen, wo es benötigt wird, ist die Zugabe von Tetraacetylethylendiamin (TAED) zu einer alkalischen Lösung von H.zweiODERzwei.
Anwendungen
In der Medizin als Sterilisationsmittel für Geräte
PAA wirkt als Desinfektionsmittel für medizinische Geräte in Kliniken, Krankenhäusern, Arzt- und Zahnarztpraxen.
Einige Quellen berichten, dass seine Wirkung gegen Mikroorganismen allgemein wie folgt klassifiziert werden kann: Bakterien> Viren> Bakteriensporen> Protozoenzysten. Dies bedeutet, dass es wirksamer gegen Bakterien und weniger wirksam gegen Protozoen-Zysten ist..
In Studien zur bakteriziden Wirkung von PAA und anderen hochwirksamen Desinfektionsmitteln gegen Staphylococcus aureus Y. Pseudomonas aeruginosa In Endoskopiegeräten erwies sich PAA als am schnellsten in seiner mikrobiziden Wirkung.
Das Staphylococcus aureus Es kann Weichteilinfektionen, Hautinfektionen, Lungenentzündung und Herzgewebsinfektionen verursachen. Das Pseudomonas aeruginosa kann zu einer Lungenentzündung führen.
Bakterien bilden durch eine dicke Schicht extrazellulärer Proteine, Polysaccharide und Nukleinsäuren Biofilme, die sie vor äußeren Reizen oder Stress schützen..
Diese Biofilme sind sehr resistent gegen gängige Antibiotika und Desinfektionsmittel. In Geräten wie Endoskopen neigen sie aufgrund unzureichender oder ineffektiver Reinigungs- und Desinfektionsroutinen dazu, sich in den engen Kanälen dieser zu bilden.
PAA greift diese Biofilme wahrscheinlich durch Oxidation der empfindlicheren molekularen Bindungen von Proteinen, Enzymen und anderen Metaboliten an. Dies führt zum Abbau der Zellwände von Keimen, ihren Sporen und Zysten..
Darüber hinaus kann PAA durch das Eindringen in die Zelle essentielle Enzyme oxidieren und den Transport von Molekülen und lebenswichtigen biochemischen Prozessen beeinträchtigen.
Die Desinfektionszeiten sind seit einigen Jahren festgelegt, aber während bestimmter Studien wurde beobachtet, dass die Behandlung mit PAA bereits nach 5 Minuten Veränderungen in der Form der Zellen verursachte, wobei sich Taschen oder Ausbuchtungen in der Zellwand der Zellen bildeten Zusammenbruch der Zellstrukturen der Mikroorganismen nach 30 Minuten.
Obwohl sich die PAA durch ihre Geschwindigkeit auszeichnete, haben die Forscher empfohlen, die in den Reinigungs- und Desinfektionsprotokollen festgelegten Zeiten neu zu bewerten und sie für die meisten hochwirksamen Antiseptika zu verlängern, um ihre Gesamtwirksamkeit sicherzustellen..
Einer der negativen Aspekte von PAA ist, dass es einige Krankheitserreger gibt, gegen die es nicht sehr wirksam ist, wie z Giardia lamblia und von Cryptosporidium parvum (Parasiten, die Durchfall oder andere Darmerkrankungen verursachen können).
In der Abwasserbehandlung
Die desinfizierende Wirkung von PAA in kommunalen oder industriellen Abwässern wird seit mehr als 30 Jahren untersucht.

Zu seinen Vorteilen gehört das breite Spektrum seiner keimtötenden Wirkung auch in Gegenwart organischer Stoffe sowie die Tatsache, dass keine umweltschädlichen Nebenprodukte entstehen..
Die Wirksamkeit seiner Wirkung scheint unter anderem von der Menge der im Abwasser vorhandenen organischen Substanz, der Art und Menge der zu eliminierenden Mikroorganismen, der PAA-Konzentration im zu behandelnden Wasser, dem pH-Wert und der Dauer von abzuhängen die Behandlung..
In einigen Fällen hat sich gezeigt, dass PAA zur Desinfektion von Abwasser in tropischen Klimazonen besser als Natriumhypochlorit ist und neben vielen anderen Krankheitserregern gegen das Cholera-Virus wirksam ist..
Einer der negativen Punkte ist jedoch, dass aufgrund der nach der Desinfektion verbleibenden Essigsäure das Abwasser mit organischer Substanz beladen ist, was das Risiko eines neuen Wachstums von Mikroorganismen erhöht..
Andererseits ist es ein teures Produkt, so dass es aufgrund dieses Aspekts noch nicht sehr wettbewerbsfähig ist, beispielsweise mit Natriumhypochlorit..
In der Lebensmittelindustrie
Da es ein starkes Oxidationsmittel ist, ist es bei niedrigen Temperaturen sehr wirksam gegen Mikroorganismen und dies hat zu seiner breiten Verwendung als Bakterizid und Fungizid in der Lebensmittel- und Getränkeverarbeitung geführt..
Dies umfasst Fleisch- und Geflügelverarbeitungsbetriebe, Molkereien, Brauereien, Weingüter oder Weingüter sowie Produktionsstätten für Erfrischungsgetränke. An all diesen Stellen wird die PAA angewendet, da sie sich ideal zur Reinigung eignet vor Ort (an dem Ort).
Enzyme in einigen Lebensmitteln wie Peroxidase und Katalase, die Wasserstoffperoxid H deaktivierenzweiODERzwei, Sie haben keine schädliche Wirkung auf Peressigsäure. Proteinreste tun dir auch nicht weh.
Aufgrund der Tatsache, dass PAA in Lebensmitteln in Essigsäure und Wasserstoffperoxid zerfällt, gilt es als sicher für Anwendungen, bei denen Lebensmittel nicht gespült werden..
Es dient als Desinfektions- und Sterilisationsmittel für Edelstahl- und Glastanks, Rohre und Tankwagen, die zum Transport und zur Lagerung von Getränken dienen.

Seine Eigenschaft, ungiftige Produkte zu erzeugen und in hoher Verdünnung keine Aromen oder Gerüche zu erzeugen, bedeutet für diese Industrien Zeit- und Geldersparnis.
In der Zellstoff- und Papierindustrie
Peressigsäure ist ein wichtiges chlorfreies Mittel in der Bleichtechnologie in der Papierzellstoffindustrie..
Einige Autoren betrachten Peressigsäure als aktiviertes Derivat von H.zweiODERzwei, wobei einer der Wasserstoffatome davon durch eine Acylgruppe CH ersetzt wurde3C (= O)-.
Infolgedessen reagiert Peressigsäure stärker mit organischen Substraten als H.zweiODERzwei und dass es in Oxidationsreaktionen unter moderateren Bedingungen als mit H verwendet werden kannzweiODERzwei.
Unter neutralen oder mäßig alkalischen Bedingungen wird das Peracetation CH3C (= O) OO- ist ein starkes Nucleophil (das von elektronenarmen Atomen angezogen wird) und entfernt selektiv Chromophore oder farbige Verbindungen, die in Papierzellstoff vorhanden sind.
Dies ermöglicht diesen Industrien ein sehr wirksames Bleichmittel, dessen Rückstände ihre wässrigen Abwässer nicht verunreinigen..
Bei der Herstellung anderer chemischer Verbindungen
Peressigsäure dient als Oxidationsmittel zur Herstellung von Epoxidverbindungen, als Katalysator zur Herstellung von Polyesterharzen und zur Gewinnung von Caprolactam und Glycerin.
Bei der Rückgewinnung von Polymeren zum Recycling
Einige Forscher haben es geschafft, nützliche Materialien durch Behandlung bestimmter polymerer Abfälle mit PAA-Lösungen wiederzugewinnen..
Das Verfahren wird durch Oxidation bestimmter kohlefaserverstärkter Polymerabfälle aus Luft- und Raumfahrtaktivitäten mit Lösungen von Eisessig und Wasserstoffperoxid durchgeführt.
Auf diese Weise wird Peressigsäure erzeugt vor Ort, Dadurch wird das Epoxidharz zu 97% abgebaut, wobei die Kohlefaser intakt bleibt.
Dann werden durch Destillation mehr als 90% der Essigsäure gewonnen, was zu einer weiteren Zersetzung des Polymers führt, das wiedergewinnbare aliphatische und phenolische Verbindungen erzeugt..
Kohlefaser wird sauber erhalten und behält ihre Länge und Zugfestigkeit bei, vergleichbar mit Frischfasern.

Das Verfahren wird unter milden Bedingungen ohne gasförmige Emissionen durchgeführt, was es umweltfreundlich macht.
In Wäschereien
Peressigsäure wird aufgrund ihrer Oxidationskraft von farbigen Verbindungen beim Bleichen von Wäsche verwendet. In diesen Fällen wird die Mischung von Tetraacetylethylendiamin mit H.zweiODERzwei in alkalischem Medium, um es vor Ort zu erhalten.
Sein Anwendungsbereich ist sehr breit, da er in hartem Wasser oder solchen mit einem hohen Anteil an Calcium- und Magnesiumsalzen bei einem pH-Wert zwischen 3,0 und 7,5 und Temperaturen von 0 bis 40 ºC eingesetzt werden kann..
Risiken
Peressigsäure oder PAA können stark ätzend sein. Es ist stark reizend für Haut und Augen.
Wenn seine Lösungen aufgenommen werden, verursacht es Korrosion der Schleimhäute von Mund, Rachen, Speiseröhre und Magen-Darm-Trakt, was zu Schmerzen und Schluckbeschwerden führt..
Wenn die Dämpfe eingeatmet werden, tritt eine Reizung der Atemwege auf, und wenn die Einatmung verlängert wird, tritt ein Ödem in der Lunge auf..
Lösungen, die mehr als 15% PAA enthalten, zeigen ein gewisses Maß an Instabilität und Explosivität, und Stöße oder Schütteln sollten vermieden werden. Sie können sich explosionsartig zersetzen. Wenn die Konzentration von PAA in Lösung 56% überschreitet, kann es aufgrund des heftigen Verdampfens von Essigsäure zur Detonation kommen.
Hitze sollte vermieden werden. Es gilt als brennbare Flüssigkeit. Seine Zersetzung ist bei einer Explosion bei 110 ºC heftig. Es sollte an kühlen Orten, vorzugsweise unter Kühlung, oder an sehr gut belüfteten Orten gelagert werden..
Es oxidiert stark und ist daher bei Kontakt mit organischen Stoffen gefährlich. Bei Lagerung muss es von anderen Verbindungen isoliert werden, insbesondere von organischen, brennbaren, brennbaren oder oxidierbaren Verbindungen. Es muss von Säuren, Laugen und Schwermetallen getrennt werden.
Wenn es zur Zersetzung erhitzt wird, gibt es scharfe und reizende Dämpfe ab, die Augen, Nase und Rachen reizen..
Wenn es verschüttet wird, darf es nicht in die Kanalisation fließen, da dies eine Brand- oder Explosionsgefahr darstellt..
Als vorbeugende Maßnahmen für die Handhabung empfehlen wir Gummihandschuhe und Schutzkleidung, einen Gesichtsschutz oder Augenschutz (Brille oder Schutzbrille), Atemschutz und essen, trinken oder rauchen Sie nicht, während Sie mit ihren Lösungen arbeiten..
Verweise
- UNS. Nationalbibliothek für Medizin. (2019). Peressigsäure. Wiederhergestellt von: pubchem.ncbi.nlm.nih.gov
- Das, M. et al. (2018). Eine effiziente Methode zum Recycling von CFK-Abfällen mit Peressigsäure. ACS Sustainable Chemistry & Engineering. Von pubs.acs.org wiederhergestellt.
- Chino, T. et al. (2017). Morphologische bakterizide, schnell wirkende Wirkungen von Peressigsäure, einem hochwirksamen Desinfektionsmittel, gegen Staphylococcus aureus und Pseudomonas aeruginosa Biofilme in Schläuchen. Antibiotikaresistente Infektionskontrolle. 2017: 6: 122. Von ncbi.nlm.nih.gov wiederhergestellt.
- Pan, G.X. et al. (1999). Reaktivität von Ferulasäure und ihren Derivaten gegenüber Wasserstoffperoxid und Peressigsäure. J. Agric. Food Chem. 1999, 47, 3325 & ndash; 3331. Von pubs.acs.org wiederhergestellt.
- Kitis, Mehmet. (2004). Desinfektion von Abwasser mit Peressigsäure: eine Überprüfung. Environment International 30 (2004) 47-55. Von sciencedirect.com wiederhergestellt.



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.