
Hypobrome Säureeigenschaften, Struktur, Verwendung

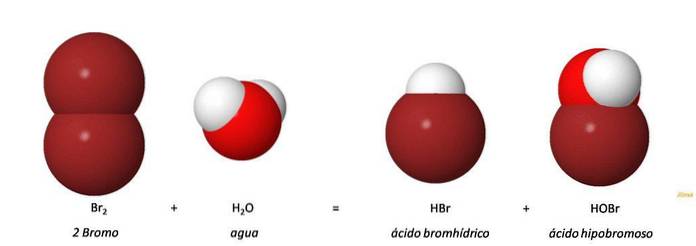
Das hypobrome Säure (HOBr, HBrO) ist eine anorganische Säure, die durch Oxidation des Bromidanions (Br-) hergestellt wird. Die Zugabe von Brom zu Wasser ergibt Bromwasserstoffsäure (HBr) und hypobrome Säure (HOBr) durch eine Disproportionierungsreaktion. Br2 + H2O = HOBr + HBr
Hypobrome Säure ist eine sehr schwache, etwas instabile Säure, die bei Raumtemperatur als verdünnte Lösung vorliegt. Es wird in warmblütigen Wirbeltierorganismen (einschließlich Menschen) durch die Wirkung des Enzyms Eosinophile Peroxidase produziert.
Die Entdeckung, dass hypobrome Säure die Kollagen-IV-Aktivität regulieren kann, hat viel Aufmerksamkeit auf sich gezogen..
Artikelverzeichnis
- 1 Struktur
- 1.1 2D
- 1.2 3D
- 2 Physikalische und chemische Eigenschaften
- 3 Verwendungen
- 4 Biomolekulare Wechselwirkungen
- 5 Referenzen
Struktur
2D
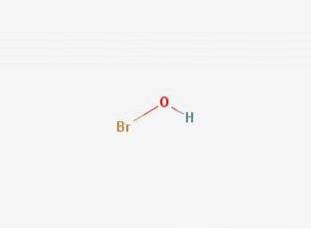
3D

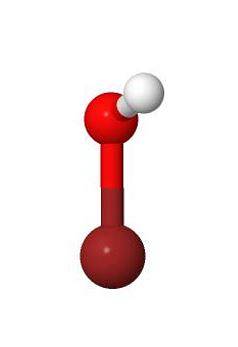
Physikalische und chemische Eigenschaften
- Aussehen gelbe Feststoffe: gelbe Feststoffe.
- Aussehen: gelbe Feststoffe.
- Molekulargewicht: 96,911 g / mol.
- Siedepunkt: 20-25 ° C..
- Dichte: 2,470 g / cm³.
- Säure (pKa): 8,65.
- Die chemischen und physikalischen Eigenschaften von hypobromer Säure ähneln denen anderer Hypohalogenite..
- Es kommt als verdünnte Lösung bei Raumtemperatur.
- Hypobromit-Feststoffe haben eine gelbe Farbe und einen besonderen aromatischen Geruch.
- Es ist ein starkes Bakterizid und Wasserdesinfektionsmittel.
- Es hat einen pKa von 8,65 und dissoziiert teilweise in Wasser bei pH 7.
Anwendungen
- Hypobrome Säure (HOBr) wird aufgrund ihrer Fähigkeit, die Zellen vieler Krankheitserreger abzutöten, als Bleichmittel, Oxidationsmittel, Deodorant und Desinfektionsmittel verwendet.
- Es wird von der Textilindustrie als Bleich- und Trocknungsmittel verwendet.
- Wird auch in Whirlpools und Spas als keimtötendes Mittel verwendet.
Biomolekulare Wechselwirkungen
Brom ist bei Tieren als ionisches Bromid (Br-) allgegenwärtig, aber bis vor kurzem war seine wesentliche Funktion unbekannt..
Neuere Forschungen haben gezeigt, dass Brom für die Architektur der Basalmembran und die Gewebeentwicklung essentiell ist.
Das Enzym Peroxidain verwendet HOBr zur Vernetzung von Sulfilimin, das in den Kollagen-IV-Gerüsten der Basalmembran vernetzt ist..
Hypobrome Säure wird in warmblütigen Wirbeltierorganismen durch die Wirkung des Enzyms Eosinophile Peroxidase (EPO) produziert..
EPO erzeugt HOBr aus H2O2 und Br- in Gegenwart einer Plasmakonzentration von Cl-.
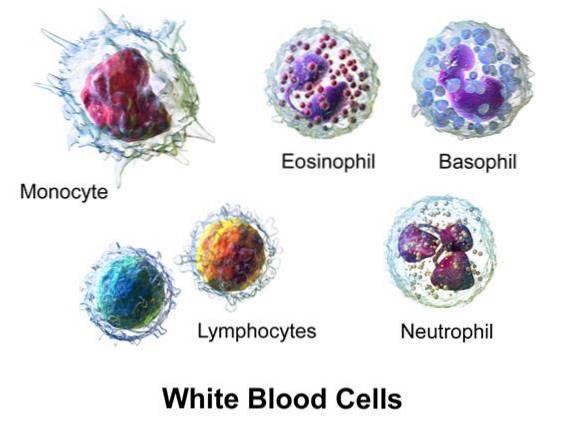
Myeloperoxidase (MPO) erzeugt aus Monozyten und Neutrophilen Hypochlorsäure (HOCl) aus H2O2 und Cl-.
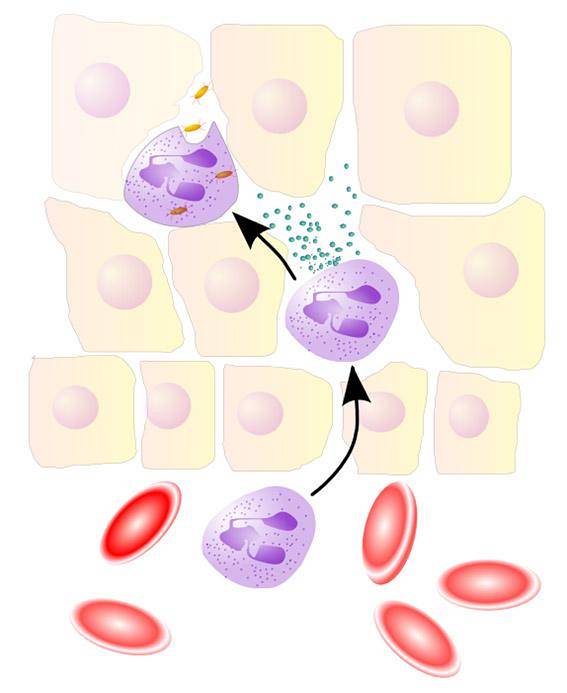
EPO und MPO spielen eine wichtige Rolle bei den Abwehrmechanismen des Wirts gegen Krankheitserreger unter Verwendung von HOBr bzw. HOCl.
Das MPO / H2O2 / Cl- System in Gegenwart von Br- erzeugt ebenfalls HOBr durch Umsetzung des gebildeten HOCl mit Br-. HOBr ist mehr als ein starkes Oxidationsmittel, es ist ein starkes Elektrophil.
Die Plasmakonzentration von Br- ist mehr als 1000-mal niedriger als die des Chloridanions (Cl-). Folglich ist die endogene Produktion von HOBr im Vergleich zu HOCl ebenfalls geringer.
HOBr ist jedoch signifikant reaktiver als HOCl, wenn die Oxidierbarkeit der untersuchten Verbindungen nicht relevant ist. Daher könnte die Reaktivität von HOBr eher mit seiner elektrophilen Stärke als mit seiner Oxidationskraft zusammenhängen (Ximenes, Morgon & de Souza, 2015)..
Obwohl sein Redoxpotential niedriger als das von HOCl ist, reagiert HOBr schneller mit Aminosäuren als HOCl.
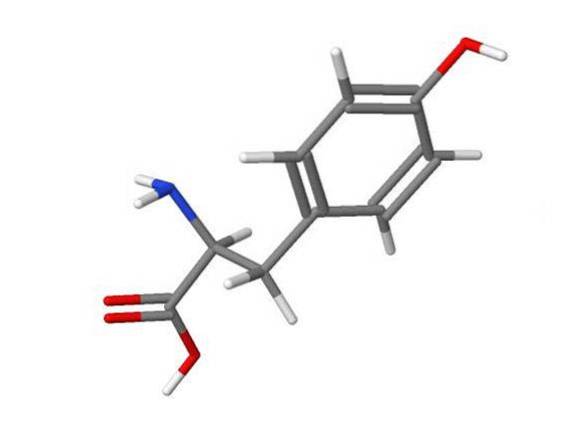
Die Halogenierung des Tyrosinrings durch HOBr ist 5000-mal schneller als die von HOCl.
HOBr reagiert auch mit Nukleosidnukleobasen und DNA.
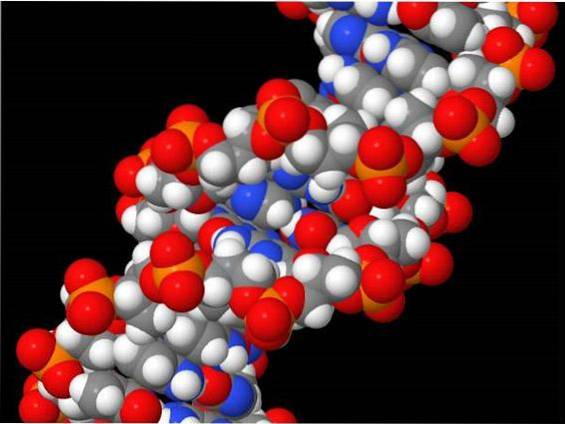
2'-Desoxycytidin, Adenin und Guanin erzeugen 5-Brom-2'-desoxycytidin, 8-Bromadenin und 8-Bromoguanin in EPO / H2O2 / Br- und MPO / H2O2 / Cl- / Br- Systemen (Suzuki, Kitabatake und Koide) , 2016).
McCall et al. (2014) haben gezeigt, dass Br ein erforderlicher Cofaktor für die Bildung von Sulfilimin-Vernetzungen ist, die durch das Enzym Peroxidasin katalysiert werden, eine posttranslationale Modifikation, die für die Architektur von Kollagen IV der Basalmembranen und die Entwicklung von Geweben wesentlich ist..
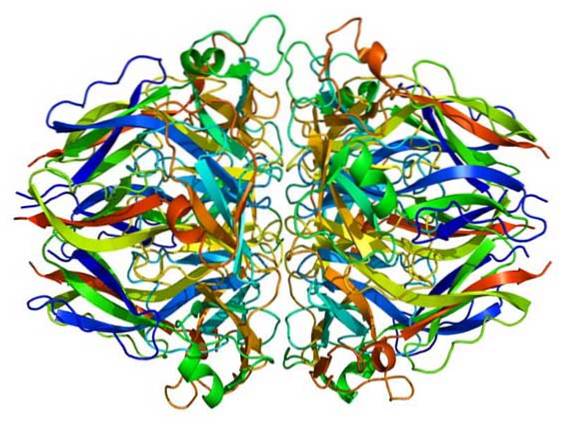
Basalmembranen sind spezialisierte extrazelluläre Matrizen, die wichtige Vermittler der Signalübertragung und der mechanischen Unterstützung von Epithelzellen sind..
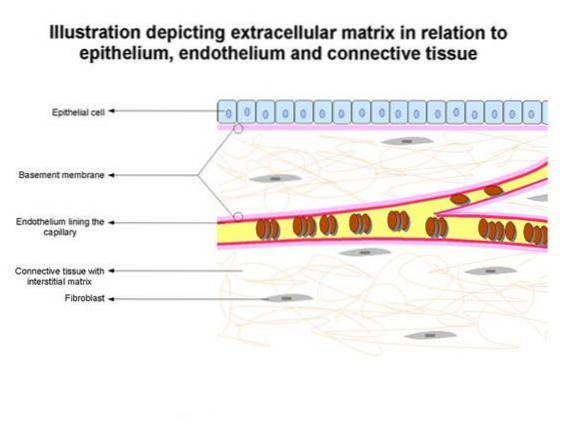
Basalmembranen definieren unter anderem die Architektur des Epithelgewebes und erleichtern die Gewebereparatur nach einer Verletzung..
In die Basalmembran ist ein mit Sulfilimin vernetztes Kollagen-IV-Gerüst eingebettet, das die Matrixfunktionalität in mehrzelligen Geweben aller Tiere verleiht..
Kollagen IV-Gerüste bieten mechanische Festigkeit, dienen als Ligand für Integrine und andere Zelloberflächenrezeptoren und interagieren mit Wachstumsfaktoren, um Signalgradienten zu etablieren..
Sulfilimin (Sulfimid) ist eine chemische Verbindung, die eine Schwefel-Stickstoff-Doppelbindung enthält. Sulfiliminbindungen stabilisieren die in der extrazellulären Matrix gefundenen Kollagen-IV-Stränge.
Diese Bindungen verbinden kovalent die Methionin 93 (Met93) - und Hydroxylysin 211 (Hyl211) -Reste benachbarter Polypeptidstränge, um ein größeres Kollagen-Trimer zu bilden..
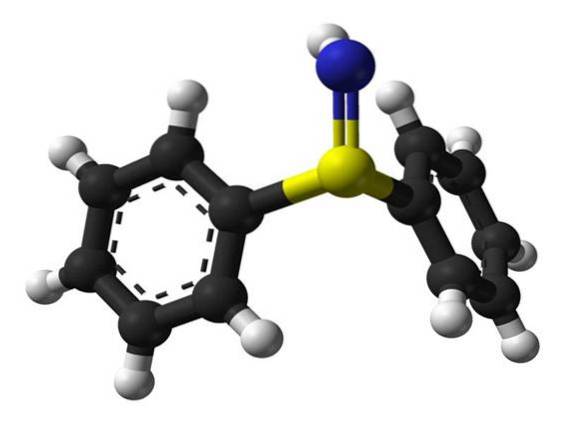
Peroxidain bildet aus Bromid bzw. Chlorid hypobrome Säure (HOBr) und Hypochlorsäure (HOCl), die die Bildung von Sulfiliminvernetzungen vermitteln können..
Das in hypobrome Säure umgewandelte Bromid bildet ein Zwischenprodukt des Bromsulfoniumions (S-Br), das an der Bildung von Vernetzungen beteiligt ist.
McCall et al. (2014) haben gezeigt, dass ein Br-Mangel in der Nahrung bei der Drosophila-Fliege tödlich ist, während ein Br-Ersatz seine Lebensfähigkeit wiederherstellt.
Sie stellten auch fest, dass Brom aufgrund seiner Rolle bei der Bildung von Sulfiliminbindungen und Kollagen IV, das für die Bildung von Basalmembranen und die Entwicklung von Geweben von entscheidender Bedeutung ist, ein essentielles Spurenelement für alle Tiere ist..
Verweise
- ChemIDplus, (2017). 3D-Struktur von 13517-11-8 - Hypobrome Säure [Bild] Abgerufen von nih.gov.
- ChemIDplus, (2017). 3D-Struktur von 60-18-4 - Tyrosin [USAN: INN] [Bild] Abgerufen von nih.gov.
- ChemIDplus, (2017). 3D-Struktur von 7726-95-6 - Brom [Bild] Abgerufen von nih.gov.
- ChemIDplus, (2017). 3D-Struktur von 7732-18-5 - Wasser [Bild] Aus nih.gov wiederhergestellt.
- Emw, (2009). Protein COL4A1 PDB 1li1 [Bild] Von wikipedia.org wiederhergestellt.
- Mills, B. (2009). Diphenylsulfimid-aus-xtal-2002-3D-Kugeln [Bild] Von wikipedia.org wiederhergestellt.
- PubChem, (2016). Hypobrome Säure [Bild] Abgerufen von nih.gov.
- Steane, R. (2014). Das DNA-Molekül - dreidimensional drehbar [Bild] Aus biotopics.co.uk wiederhergestellt
- Thormann, U. (2005). NeutrophilerAktion [Bild] Von wikipedia.org wiederhergestellt.



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.