
Gallussäurestruktur, Eigenschaften, Gewinnung, Verwendung

Das Gallussäure ist eine organische Verbindung der Summenformel C.6H.zwei(OH)3COOH, das zur Kategorie der Polyphenole gehört. Es wird als kristallines Pulver mit einer weißen Farbe erkannt, die nahezu hellgelb ist..
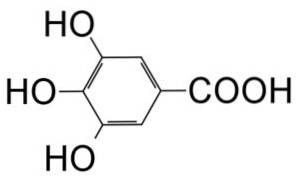
Es ist eine Trihydroxybenzoesäure, die durch einen Benzolring gebildet wird, an den eine Carbonsäuregruppe (-COOH) und 3 Hydroxylgruppen (-OH) in den Positionen 3, 4 und 5 des Rings gebunden sind..
In der Natur ist es weit verbreitet, da es ein Produkt ist, das in erheblichen Mengen in Pflanzen und Pilzen gebildet wird. Es existiert frei oder an die Tannine der meisten Pflanzenarten gebunden, wobei Walnüsse, Trauben, Divi-Divi-Pflanzen, Eichenrinde, Granatapfel oder seine Wurzeln, Sumachpflanzen und Tee hervorstechen..

Es ist auch in Honig, Kakao, verschiedenen Beeren, Mango und anderem Obst und Gemüse sowie in einigen Getränken wie Wein- und Teeaufgüssen enthalten..
In Pflanzengeweben liegt es in Form eines Esters oder Gallats vor. Die Menge, in der es gefunden wird, hängt von äußeren Reizen ab, wie der Menge an UV-Strahlung, die die Pflanze erhalten hat, chemischem Stress und mikrobiellen Infektionen..
Bei Trauben und Wein kommt es auf die Rebsorte, Verarbeitung und Lagerung an. In grünem Tee ist der Gehalt an Gallaten hoch, aber Kakao enthält mehr als grüner Tee und Rotwein.
Chemisch verhält es sich wie ein Reduktionsmittel. Es ist adstringierend und antioxidativ. Es wurde auch in blauen Schreibtinten verwendet und wird üblicherweise in der pharmazeutischen Industrie verwendet..
Es hat ein großes Potenzial für medizinische Anwendungen, da es aufgrund seiner vielfältigen Eigenschaften von Gallussäure und seinen Derivaten ein vielversprechendes therapeutisches Mittel in der Präventivmedizin ist.
Artikelverzeichnis
- 1 Struktur
- 2 Nomenklatur
- 3 Eigenschaften
- 3.1 Physikalischer Zustand
- 3.2 Molekulargewicht
- 3.3 Schmelzpunkt
- 3.4 Dichte
- 3.5 Löslichkeit
- 3.6 Dissoziationskonstante
- 3.7 Chemische Eigenschaften
- 3.8 Andere Eigenschaften
- 4 Erhalten
- 5 Verwendungen
- 5.1 - In Tinten und Farbstoffen
- 5.2 - In medizinischen Anwendungen
- 5.3 - In potenziellen medizinischen Anwendungen
- 5.4 - In veterinärmedizinischen Anwendungen
- 5.5 - In verschiedenen Anwendungen
- 5.6 - Nützlichkeit in natürlichen Gewässern
- 6 Referenzen
Struktur
Gallussäure kristallisiert aus absolutem Methanol oder aus Chloroform in Form von weißen Nadeln. Kristallisiert in Wasser in Form von seidigen Nadeln aus seinem Monohydrat.
Nomenklatur
- Gallussäure.
- 3,4,5-Trihydroxybenzoesäure.
Eigenschaften
Körperlicher Status
Feste, kristalline Nadeln.
Molekulargewicht
170,12 g / mol.
Schmelzpunkt
Es zersetzt sich bei 235-240 ºC und erzeugt Pyrogallol und COzwei
Dichte
1,694 g / cm3
Löslichkeit
In Wasser: mäßig löslich.
- 1 g in 87 ml Wasser
- 1 g in 3 ml kochendem Wasser
In Ethanol: 1 g in 6 ml Alkohol.
In Diethylether: 1 g in 100 ml Ether.
In Glycerin: 1 g in 10 ml Glycerin.
In Aceton: 1 g in 5 ml Aceton.
Praktisch unlöslich in Benzol, Chloroform und Leichtbenzin.
Dissoziationskonstante
K.1 4,63 x 10-3 (bei 30 ºC).
K.zwei 1,41 x 10-9
Chemische Eigenschaften
Gallussäurelösungen, insbesondere Alkalimetallsalze, absorbieren Sauerstoff und werden an der Luft braun.
Gallussäure ist ein starkes Reduktionsmittel, das Gold- oder Silbersalze zum Metall reduzieren kann. Es ist im Allgemeinen nicht kompatibel mit Chloraten, Permanganat, Ammoniak, Bleiacetat, Alkalihydroxiden, Alkalicarbonaten, Silbersalzen und Oxidationsmitteln..
Gallussäure bildet mit Eisen (II) -Salzen einen tiefblauen Komplex.
In Gallussäure ist die Hydroxylgruppe (-OH) an Position 4 am chemisch reaktivsten.
Andere Eigenschaften
Es muss vor Licht geschützt werden, da es es photochemisch abbaut.
Es ist ein milder lokaler Reizstoff. Das Einatmen von Staub kann Nase und Rachen beeinträchtigen und der Kontakt mit Augen und Haut führt zu Reizungen..
Toxizitätsstudien an Mäusen zeigen, dass Gallussäure, die bis zu einem Gehalt von 5000 mg / kg aufgenommen wird, für diese Tiere nicht toxisch ist. Es wird als wenig toxisch angesehen und bestätigt die Sicherheit seiner Verwendung.
Erhalten
Gallussäure wird durch alkalische oder saure Hydrolyse der Tannine von Nüssen oder Pflanzenmaterialien erhalten, die reich an diesen Verbindungen sind..
Die Hydrolyse kann auch enzymatisch unter Verwendung von Schimmelpilzkulturbrühen wie z Penicillium glaucum oder der Aspergillus niger, die Tannase enthalten, ein Enzym, das das Tanninmolekül bricht oder spaltet.
Ein anderer Weg, um Gallussäure zu erhalten, ist von p-Hydroxybenzoesäure durch Sulfonierung und alkalische Fusion, wodurch die Addition der anderen zwei -OH-Gruppen in das Molekül erreicht wird..
Anwendungen
- In Tinten und Farbstoffen
Gallussäure wird bei der Herstellung von Anthragalol und Pyrogallol verwendet, die Zwischenprodukte bei der Herstellung von Farbstoffen wie Gallocyanin und Galoflavin sind. Es ist wiederum ein Rohstoff für die Synthese von Oxazinderivaten, die auch als Farbstoffe verwendet werden..
Gallussäure ist bei der Herstellung von Schreibtinten sehr wichtig, da sie mit Eisen einen blauen Komplex bildet. Diese Tinten enthalten hauptsächlich eine Mischung aus Gallussäure, Eisensulfat (FeSO)4) und Gummi arabicum.
Eisengallussäuretinten waren unverzichtbare Materialien zum Schreiben von Dokumenten, Zeichnen von Plänen und Vorbereiten von schriftlichen Materialien..

- In medizinischen Anwendungen
Es wird als intestinales Adstringens und Blutstillungsmittel (styptisch) eingesetzt. Gallussäure ist der Rohstoff für die Gewinnung von Rufigalol, einem Malariamittel..
Aufgrund seiner chemischen Reduktionskapazität wird Gallussäure bei der Herstellung von pharmazeutischen Produkten verwendet..
- In potenziellen medizinischen Anwendungen
Gegen Krebs
Gallussäure wurde als Hauptverantwortlicher für die Antikrebseigenschaften mehrerer Pflanzenextrakte identifiziert.
Im Gegensatz zu seiner besonderen antioxidativen Wirkung wurde festgestellt, dass es prooxidative Eigenschaften bei der Induktion der Apoptose von Krebszellen aufweisen kann. Apoptose ist die ordnungsgemäße Zerstörung geschädigter Zellen, die durch denselben Organismus verursacht werden.
Es gibt Hinweise darauf, dass Gallussäure und Gallate in schnell wachsenden Tumorzellen eine selektive Apoptose induzieren und gesunde Zellen intakt lassen. Darüber hinaus wurde berichtet, dass es die Angiogenese und folglich die Krebsinvasion und Metastasierung verlangsamt.
Gallussäure-Antikrebsaktivität wurde bei Leukämie, Prostata-, Lungen-, Magen-, Bauchspeicheldrüsen- und Darmkrebs, Brust-, Gebärmutterhals- und Speiseröhrenkrebs gefunden.
Gegen verschiedene Pathologien
In mehreren Studien wurde gezeigt, dass es antimykotische, antibakterielle, antivirale, antiallergische, entzündungshemmende, antimutagene, Anti-Cholesterin-, Antiobesitäts- und immunmodulatorische Aktivität aufweist.
Gallussäure ist ein guter Kandidat zur Bekämpfung von Parodontitis (Zahnfleischerkrankungen).
Es zeigt auch ein neuroprotektives, kardioprotektives, hepatoprotektives und nephroprotektives Potential. Beispielsweise haben mehrere Studien an Herzgewebe bei Ratten bestätigt, dass Gallussäure eine schützende Wirkung auf das Myokard gegen oxidativen Stress ausübt.
Als zelluläres Anti-Aging-Mittel
Gallussäure bietet einen wirksamen Schutz gegen oxidative Schäden, die durch reaktive Spezies verursacht werden, die häufig in biologischen Systemen wie Hydroxylradikalen (OH) vorkommen.), Superoxid (O.zwei.) und Peroxyl (ROO.).
Es wurde festgestellt, dass es vom Verdauungstrakt schneller absorbiert wird als die meisten Polyphenole. Und es ist eines von denen mit der höchsten antioxidativen Kapazität.
Zusätzlich behaupten einige Forscher, dass Gallussäure von Niosomen transportiert werden kann, um ihre Anti-Aging-Aktivität zu erhöhen. Das Niosom ist ein molekulares System zur kontrollierten Freisetzung von Arzneimitteln anstelle des Körpers, der es benötigt.
Diese Eigenschaften geben ihm ein hohes Potenzial gegen Zellalterung..
- In veterinärmedizinischen Anwendungen
Es wurde als intestinales Adstringens bei Tieren verwendet.
- In verschiedenen Anwendungen
Gallussäure wird bei der Herstellung seiner Ester wie Methylgallat, Propylgallat, Octylgallat und Laurylgallat verwendet..
Diese Derivate werden häufig als Antioxidationsmittel und Konservierungsmittel in verarbeiteten Lebensmitteln und in Lebensmittelverpackungsmaterialien verwendet, um Ranzigwerden und oxidativen Abbau zu verhindern. Die genannten Derivate werden auch in der Kosmetik eingesetzt.
Gallussäure wird als fotografischer Entwickler und bei der Herstellung von Papier verwendet. Darüber hinaus wird es in großem Umfang zur Stabilisierung von Kollagen beim Ledergerben eingesetzt..
Als analytisches Reagenz ist Gallussäure ideal als Standard zur Bestimmung des Phenolgehalts von Pflanzenextrakten, und die Ergebnisse werden als Gallussäureäquivalente ausgedrückt..
Es wird auch in Tests zur Bestimmung von freien Mineralsäuren, Dihydroxyaceton und Alkaloiden verwendet..
- Nützlichkeit in natürlichen Gewässern
Gallussäure, die in Grundwasserleitern in Pflanzenmaterial natürlich vorkommt, ist eine der Faktoren, die für die Nährstoffverfügbarkeit von Fe (II) verantwortlich sind, die für das Wachstum aquatischer Arten erforderlich ist.
Dies liegt daran, dass es in der Lage ist, unter aeroben Bedingungen eine hohe Konzentration an gelöstem Eisen (II) aufrechtzuerhalten. Dies liegt daran, dass es mit oxidationsbeständigem Fe (II) einen Komplex bildet..

Verweise
- M. Sajid et al. (2019). Nanopartikelbasierte Abgabe von Phytomedizin: Herausforderungen und Chancen. Im neuen Look der Phytomedizin. Kapitel 23. Von sciencedirect.com wiederhergestellt.
- Windholz, M.; Budavari, S.; Blumetti, R. F. und Otterbein, E. (Herausgeber) (1983). Der Merck-Index. Zehnte Ausgabe. Merck & CO., Inc..
- CRC Handbuch für Chemie und Physik. 75th 1994. CRC Press, Inc..
- Ullmanns Enzyklopädie der Industriechemie. (1990). Fünfte Ausgabe. Band A13. VCH Verlagsgesellschaft mbH.
- Badhani, B; Sharma, N. und Kakkar, R. (2015). Gallussäure: Ein vielseitiges Antioxidans mit vielversprechenden therapeutischen und industriellen Anwendungen. RSC-Fortschritte. Von rsc.org wiederhergestellt.
- Zanwar, Anand A. et al. (2014). Rolle der Gallussäure bei Herz-Kreislauf-Erkrankungen. In Polyphenolen in der menschlichen Gesundheit und Krankheit. Kapitel 80. Von sciencedirect.com wiederhergestellt.
- Nowak, R. et al. (2014). Pflanzenpolyphenole als chemopräventive Mittel. In Polyphenolen in der menschlichen Gesundheit und Krankheit. Kapitel 97. Von sciencedirect.com wiederhergestellt.



Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.