
Sauerstoffkreislaufeigenschaften, Reservoire und Stufen

Das Sauerstoffkreislauf bezieht sich auf die Kreislaufbewegung von Sauerstoff auf der Erde. Es ist ein gasförmiger biogeochemischer Kreislauf. Sauerstoff ist nach Stickstoff das zweithäufigste Element in der Atmosphäre und nach Wasserstoff das zweithäufigste Element in der Hydrosphäre. In diesem Sinne ist der Sauerstoffkreislauf mit dem Wasserkreislauf verbunden..
Die Kreislaufbewegung von Sauerstoff umfasst die Produktion von Disauerstoff oder molekularem Zwei-Atom-Sauerstoff (O.zwei). Dies geschieht aufgrund der Hydrolyse während der Photosynthese, die von den verschiedenen photosynthetischen Organismen durchgeführt wird..

Das Özwei Es wird von lebenden Organismen in der Zellatmung verwendet und erzeugt Kohlendioxid (CO)zwei), wobei letzterer einer der Rohstoffe für den Photosynthesevorgang ist.
Andererseits tritt in der oberen Atmosphäre eine Photolyse (durch Sonnenenergie aktivierte Hydrolyse) von Wasserdampf auf, die durch ultraviolette Strahlung der Sonne verursacht wird. Wasser zersetzt sich und setzt Wasserstoff frei, der in der Stratosphäre verloren geht, und Sauerstoff wird in die Atmosphäre integriert.
Durch Wechselwirkung eines Moleküls von O.zwei Mit einem Sauerstoffatom wird Ozon (O.3). Ozon bildet die sogenannte Ozonschicht.
Artikelverzeichnis
- 1 Funktionen
- 1.1 Herkunft
- 1.2 Primitive Atmosphäre
- 1.3 Energien, die den Zyklus antreiben
- 1.4 Beziehung zu anderen biogeochemischen Kreisläufen
- 2 Stauseen
- 2.1 Geosphäre
- 2.2 Atmosphäre
- 2.3 Hydrosphäre
- 2.4 Kryosphäre
- 2.5 Lebende Organismen
- 3 Stufen
- 3.1 -Umweltstadium von Reservoir und Quelle: Atmosphäre-Hydrosphäre-Kryosphäre-Geosphäre
- 3.2 - Photosynthesestadium
- 3.3 -Atmosphärische Rückkehrstufe
- 3.4 -Respirationsstadium
- 4 Bedeutung
- 5 Änderungen
- 5.1 Treibhauseffekt
- 6 Referenzen
Eigenschaften
Sauerstoff ist ein nichtmetallisches chemisches Element. Seine Ordnungszahl ist 8, dh es hat 8 Protonen und 8 Elektronen in seinem natürlichen Zustand. Unter normalen Temperatur- und Druckbedingungen liegt es in Form von farblosem und geruchlosem Disauerstoffgas vor. Seine Summenformel lautet O.zwei.
Das Özwei enthält drei stabile Isotope: 16ODER, 17Oder und 18O. Die vorherrschende Form im Universum ist die 16O. Auf der Erde macht es 99,76% des gesamten Sauerstoffs aus. Das 18Oder entspricht 0,2%. Die Form 17Oder ist es sehr selten (~ 0,04%).
Quelle
Sauerstoff ist das dritthäufigste Element im Universum. Isotopenproduktion 16Oder es begann in der ersten Generation der solaren Heliumverbrennung, die nach dem Urknall auftrat.
Die Etablierung des Kohlenstoff-Stickstoff-Sauerstoff-Nukleosynthesezyklus in späteren Sterngenerationen hat die vorherrschende Sauerstoffquelle auf den Planeten bereitgestellt..
Hohe Temperaturen und Drücke erzeugen Wasser (H.zweiO) im Universum durch Erzeugung der Reaktion von Wasserstoff mit Sauerstoff. Wasser ist Teil der Zusammensetzung des Erdkerns.
Magma-Aufschlüsse geben Wasser in Form von Dampf ab und dieser tritt in den Wasserkreislauf ein. Wasser wird durch Photolyse durch Photosynthese in Sauerstoff und Wasserstoff sowie durch ultraviolette Strahlung in den oberen Bereichen der Atmosphäre zersetzt..
Primitive Atmosphäre
Die primitive Atmosphäre vor der Entwicklung der Photosynthese durch Cyanobakterien war anaerob. Für lebende Organismen, die an diese Atmosphäre angepasst waren, war Sauerstoff ein giftiges Gas. Noch heute verursacht eine Atmosphäre aus reinem Sauerstoff irreparable Schäden an den Zellen.
Die Photosynthese entstand in der Evolutionslinie der heutigen Cyanobakterien. Dies begann vor ungefähr 2,3 bis 2,7 Milliarden Jahren die Zusammensetzung der Erdatmosphäre zu verändern..
Die Proliferation von photosynthetisierenden Organismen veränderte die Zusammensetzung der Atmosphäre. Das Leben entwickelte sich zur Anpassung an eine aerobe Atmosphäre.
Energien, die den Kreislauf antreiben
Die Kräfte und Energien, die den Sauerstoffkreislauf antreiben, können geothermisch sein, wenn Magma Wasserdampf ausstößt, oder es kann aus Sonnenenergie stammen.
Letzteres liefert die grundlegende Energie für den Photosynthesevorgang. Chemische Energie in Form von Kohlenhydraten aus der Photosynthese treibt wiederum alle lebenden Prozesse durch die Nahrungskette. Auf die gleiche Weise erzeugt die Sonne eine unterschiedliche Planetenerwärmung und verursacht Meeres- und atmosphärische Strömungen..
Beziehung zu anderen biogeochemischen Kreisläufen
Aufgrund seiner Häufigkeit und hohen Reaktivität verbindet sich der Sauerstoffkreislauf mit anderen Kreisläufen wie COzwei, Stickstoff (N.zwei) und den Wasserkreislauf (H.zweiODER). Dies gibt ihm einen multizyklischen Charakter.
Die Stauseen von O.zwei und COzwei Sie sind durch Prozesse verbunden, bei denen organische Stoffe entstehen (Photosynthese) und zerstört (Atmung und Verbrennung). Kurzfristig sind diese Oxidations-Reduktions-Reaktionen die Hauptursache für die Variabilität der O-Konzentration.zwei in der Atmosphäre.
Denitrifizierende Bakterien erhalten Sauerstoff für ihre Atmung aus Nitraten im Boden und setzen Stickstoff frei.
Stauseen
Geosphäre
Sauerstoff ist einer der Hauptbestandteile von Silikaten. Daher macht es einen wichtigen Teil des Erdmantels und der Erdkruste aus..
- Erdkern: Im flüssigen Außenmantel des Erdkerns befinden sich neben Eisen noch andere Elemente, einschließlich Sauerstoff.
- Boden: In den Räumen zwischen Partikeln oder Poren des Bodens wird die Luft diffundiert. Dieser Sauerstoff wird von der Bodenmikrobiota verwendet.
Atmosphäre
21% der Atmosphäre besteht aus Sauerstoff in Form von Disauerstoff (O.zwei). Die anderen Formen der Anwesenheit von Luftsauerstoff sind Wasserdampf (H.zweiO), Kohlendioxid (COzwei) und Ozon (O.3).
- Wasserdampf: Die Wasserdampfkonzentration ist variabel, abhängig von der Temperatur, dem atmosphärischen Druck und den atmosphärischen Zirkulationsströmen (Wasserkreislauf)..
- Kohlendioxid: der COzwei Es macht ungefähr 0,03% des Luftvolumens aus. Seit Beginn der industriellen Revolution hat die CO-Konzentration zugenommenzwei in der Atmosphäre um 145%.
- Ozon: ist ein Molekül, das in geringer Menge in der Stratosphäre vorhanden ist (0,03 - 0,02 Volumenteile pro Million).
Hydrosphäre
71% der Erdoberfläche sind mit Wasser bedeckt. Mehr als 96% des auf der Erdoberfläche vorhandenen Wassers ist in den Ozeanen konzentriert. 89% der Masse der Ozeane besteht aus Sauerstoff. Der COzwei Es wird auch in Wasser gelöst und unterliegt einem Austauschprozess mit der Atmosphäre..
Kryosphäre
Die Kryosphäre bezieht sich auf die Masse an gefrorenem Wasser, die bestimmte Bereiche der Erde bedeckt. Diese Eismassen enthalten ungefähr 1,74% des Wassers in der Erdkruste. Andererseits enthält Eis unterschiedliche Mengen an eingeschlossenem molekularem Sauerstoff.
ODERlebende Organismen
Die meisten Moleküle, aus denen die Struktur von Lebewesen besteht, enthalten Sauerstoff. Andererseits ist ein hoher Anteil an Lebewesen Wasser. Daher ist die terrestrische Biomasse auch eine Sauerstoffreserve.
Stufen
Im Allgemeinen umfasst der Kreislauf, dem Sauerstoff als chemisches Mittel folgt, zwei große Bereiche, die seinen Charakter als biogeochemischer Kreislauf ausmachen. Diese Bereiche sind in vier Stufen vertreten.
Das Geoumweltgebiet umfasst die Verschiebungen und Eindämmungen von Sauerstoff in der Atmosphäre, der Hydrosphäre, der Kryosphäre und der Geosphäre. Dies umfasst die Umweltphase des Reservoirs und der Quelle sowie die Phase der Rückkehr in die Umwelt..
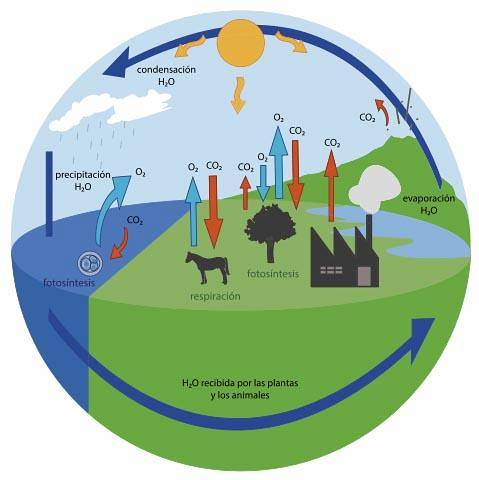
Der biologische Bereich umfasst auch zwei Stadien. Sie sind mit Photosynthese und Atmung verbunden.
-Umweltstadium des Reservoirs und der Quelle: Atmosphäre-Hydrosphäre-Kryosphäre-Geosphäre
Atmosphäre
Die Hauptquelle für Luftsauerstoff ist die Photosynthese. Es gibt aber auch andere Quellen, aus denen Sauerstoff in die Atmosphäre gelangen kann..
Einer davon ist der flüssige Außenmantel des Erdkerns. Sauerstoff gelangt durch Vulkanausbrüche in Form von Wasserdampf in die Atmosphäre. Wasserdampf steigt in die Stratosphäre auf, wo er infolge energiereicher Sonnenstrahlung einer Photolyse unterzogen wird und freier Sauerstoff erzeugt wird..
Andererseits gibt die Atmung Sauerstoff in Form von CO abzwei. Verbrennungsprozesse, insbesondere industrielle Prozesse, verbrauchen ebenfalls molekularen Sauerstoff und tragen CO beizwei in die Atmosphäre.
Beim Austausch zwischen Atmosphäre und Hydrosphäre gelangt in Wassermassen gelöster Sauerstoff in die Atmosphäre. Der CO seinerseitszwei Atmosphärisch wird in Wasser als Kohlensäure gelöst. In Wasser gelöster Sauerstoff stammt hauptsächlich aus der Photosynthese von Algen und Cyanobakterien.
Stratosphäre
In den oberen Ebenen der Atmosphäre hydrolysiert energiereiche Strahlung Wasserdampf. Kurzwellige Strahlung aktiviert O-Molekülezwei. Diese werden in freie Sauerstoffatome (O) aufgeteilt..
Diese freien O-Atome reagieren mit O-Molekülenzwei und Ozon produzieren (O.3). Diese Reaktion ist reversibel. Aufgrund der Wirkung von ultravioletter Strahlung ist O.3 zerfällt wieder in freie Sauerstoffatome.
Sauerstoff als Bestandteil der atmosphärischen Luft ist Teil verschiedener Oxidationsreaktionen und wird Teil verschiedener terrestrischer Verbindungen. Eine wichtige Senke für Sauerstoff ist die Oxidation von Gasen aus Vulkanausbrüchen..
Hydrosphäre
Die größte Wasserkonzentration auf der Erde sind die Ozeane, in denen es eine gleichmäßige Konzentration an Sauerstoffisotopen gibt. Dies ist auf den ständigen Austausch dieses Elements mit der Erdkruste durch hydrothermale Zirkulationsprozesse zurückzuführen..
An den Grenzen der tektonischen Platten und der ozeanischen Grate wird ein konstanter Prozess des Gasaustauschs erzeugt.
Kryosphäre
Landeismassen, einschließlich polarer Eismassen, Gletscher und Permafrost, sind eine wichtige Senke für Sauerstoff in Form von Festkörperwasser..
Geosphäre
Ebenso ist Sauerstoff am Gasaustausch mit dem Boden beteiligt. Dort bildet es das lebenswichtige Element für die Atmungsprozesse von Bodenmikroorganismen..
Eine wichtige Senke im Boden sind die Prozesse der Mineraloxidation und der Verbrennung fossiler Brennstoffe..
Der Sauerstoff, der Teil des Wassermoleküls ist (H.zweiO) folgt dem Wasserkreislauf bei den Verdampfungs-, Transpirations- und Kondensationsfällungsprozessen.
-Photosynthesestadium
Die Photosynthese findet in Chloroplasten statt. Während der Lichtphase der Photosynthese wird ein Reduktionsmittel benötigt, dh eine Elektronenquelle. Das Mittel ist in diesem Fall Wasser (H.zweiODER).
Durch die Entnahme von Wasserstoff (H) aus Wasser wird Sauerstoff (O.zwei) als Abfallprodukt. Wasser gelangt über die Wurzeln aus dem Boden in die Pflanze. Bei Algen und Cyanobakterien stammt es aus der aquatischen Umwelt.
Der gesamte molekulare Sauerstoff (O.zwei), das während der Photosynthese erzeugt wird, stammt aus dem im Prozess verwendeten Wasser. CO wird bei der Photosynthese verbrauchtzwei, Sonnenenergie und Wasser (H.zweiO) und Sauerstoff wird freigesetzt (O.zwei).
-Atmosphärische Rücklaufstufe
Das Özwei Bei der Photosynthese entstehende Stoffe werden bei Pflanzen durch Stomata in die Atmosphäre ausgestoßen. Algen und Cyanobakterien geben es durch Membrandiffusion an die Umwelt zurück. In ähnlicher Weise geben Atmungsprozesse Sauerstoff in Form von Kohlendioxid (CO) an die Umwelt zurückzwei).
-Atmungsstadium
Um ihre lebenswichtigen Funktionen zu erfüllen, müssen lebende Organismen die durch die Photosynthese erzeugte chemische Energie wirksam machen. Diese Energie wird bei Pflanzen in Form komplexer Kohlenhydratmoleküle (Zucker) gespeichert. Der Rest der Organismen bezieht es aus der Nahrung
Der Prozess, bei dem Lebewesen chemische Verbindungen entfalten, um die erforderliche Energie freizusetzen, wird als Atmung bezeichnet. Dieser Prozess findet in Zellen statt und hat zwei Phasen; eine aerobe und eine anaerobe.
Die aerobe Atmung findet in den Mitochondrien bei Pflanzen und Tieren statt. Bei Bakterien wird es im Zytoplasma durchgeführt, da ihnen Mitochondrien fehlen.
Das Grundelement für die Atmung ist Sauerstoff als Oxidationsmittel. Die Atmung verbraucht Sauerstoff (O.zwei) und CO wird freigesetztzwei und Wasser (H.zweiO), nützliche Energie zu erzeugen.
Der COzwei und Wasser (Wasserdampf) werden durch Stomata in Pflanzen freigesetzt. Bei Tieren COzwei es wird durch die Nase und / oder den Mund und das Wasser durch Schweiß freigesetzt. In Algen und Bakterien COzwei wird durch Membrandiffusion freigesetzt.
Photorespiration
In Pflanzen entwickelt sich in Gegenwart von Licht ein Prozess, der Sauerstoff und Energie verbraucht, der als Photorespiration bezeichnet wird. Die Photorespiration nimmt aufgrund der Zunahme der CO-Konzentration mit zunehmender Temperatur zu.zwei in Bezug auf die Konzentration von O.zwei.
Die Photorespiration stellt eine negative Energiebilanz für die Pflanze her. Verbrauchen Sie O.zwei und chemische Energie (durch Photosynthese erzeugt) und setzt CO freizwei. Aus diesem Grund haben sie evolutionäre Mechanismen entwickelt, um dem entgegenzuwirken (C4- und CAN-Metabolismus)..
Bedeutung
Heute ist die überwiegende Mehrheit des Lebens aerob. Ohne die Zirkulation von O.zwei Im Planetensystem wäre das Leben, wie wir es heute kennen, unmöglich.
Darüber hinaus macht Sauerstoff einen erheblichen Anteil der Luftmassen der Erde aus. Daher trägt es zu den damit verbundenen atmosphärischen Phänomenen und ihren Folgen bei: unter anderem erosive Effekte, Klimaregulierung..
Direkt erzeugt es Oxidationsprozesse im Boden, von vulkanischen Gasen und auf künstlichen Metallstrukturen..
Sauerstoff ist ein Element mit einer hohen Oxidationskapazität. Obwohl Sauerstoffmoleküle sehr stabil sind, weil sie eine Doppelbindung bilden, hat Sauerstoff eine hohe Reaktivitätskapazität, da er eine hohe Elektronegativität (Fähigkeit, Elektronen anzuziehen) aufweist. Aufgrund dieser hohen Elektronegativität greift Sauerstoff in viele Oxidationsreaktionen ein.
Änderungen
Die überwiegende Mehrheit der in der Natur ablaufenden Verbrennungsprozesse erfordert die Beteiligung von Sauerstoff. Ebenso bei denen, die vom Menschen erzeugt werden. Diese Prozesse erfüllen sowohl positive als auch negative Funktionen in anthropischer Hinsicht.
Die Verbrennung fossiler Brennstoffe (Kohle, Öl, Gas) trägt zur wirtschaftlichen Entwicklung bei, stellt jedoch gleichzeitig aufgrund ihres Beitrags zur globalen Erwärmung ein ernstes Problem dar.
Große Waldbrände beeinträchtigen die biologische Vielfalt, obwohl sie in einigen Fällen Teil natürlicher Prozesse in bestimmten Ökosystemen sind.
Treibhauseffekt
Die Ozonschicht (O.3) in der Stratosphäre ist der Schutzschild der Atmosphäre gegen das Eindringen von überschüssiger ultravioletter Strahlung. Diese hochenergetische Strahlung erhöht die globale Erwärmung.
Andererseits ist es stark mutagen und schädlich für lebendes Gewebe. Bei Menschen und anderen Tieren ist es krebserregend.
Die Emission verschiedener Gase bewirkt die Zerstörung der Ozonschicht und erleichtert somit den Eintritt von ultravioletter Strahlung. Einige dieser Gase sind Fluorchlorkohlenwasserstoffe, Fluorchlorkohlenwasserstoffe, Ethylbromid, Stickoxide aus Düngemitteln und Halone..
Verweise
- Anbar AD, Y Duan, TW Lyon, GL Arnold, B. Kendall, RA Creaser, AJ Kaufman, WG Gordon, S. Clinton, J. Garvin und R. Buick (2007) Ein Hauch von Sauerstoff vor dem großen Oxidationsereignis? Science 317: 1903 & ndash; 1906.
- Bekker A, HD Holland, PL Wang, D Rumble, HJ Stein, JL Hannah, LL Coetzee und NJ Beukes. (2004) Datierung des Anstiegs von Luftsauerstoff. Nature 427: 117 & ndash; 120.
- Farquhar J und DT Johnston. (2008) Der Sauerstoffkreislauf der terrestrischen Planeten: Einblicke in die Verarbeitung und Geschichte von Sauerstoff in Oberflächenumgebungen. Reviews in Mineralogy and Geochemistry 68: 463-492.
- Keeling RF (1995) Der atmosphärische Sauerstoffkreislauf: Die Sauerstoffisotope des atmosphärischen COzwei und O.zwei und der O.zwei/ N.zwei Reviws of Geophysics, Ergänzung. USA: Nationaler Bericht an die Internationale Union für Geodäsie und Geophysik 1991-1994. pp. 1253-1262.
- Purves WK, D Sadava, GH Orians und HC Heller (2003) Life. Die Wissenschaft der Biologie. 6th Edt. Sinauer Associates, Inc. und WH Freeman and Company. 1044 p.


Bisher hat noch niemand einen Kommentar zu diesem Artikel abgegeben.